STÉRILISER LES POTS MASON AU FOUR : GUIDE TECHNIQUE COMPLET
La stérilisation des pots Mason au four représente une méthode accessible et efficace pour assurer la sécurité alimentaire lors de la conservation domestique. Cette technique, bien que différente des méthodes traditionnelles à l’eau bouillante, offre des avantages spécifiques pour la préparation de contenants destinés aux conserves maison. Dans ce guide exhaustif, nous explorerons en détail cette méthode, ses applications, ses limites et les meilleures pratiques pour garantir des résultats optimaux.
1. Principes fondamentaux de la stérilisation au four
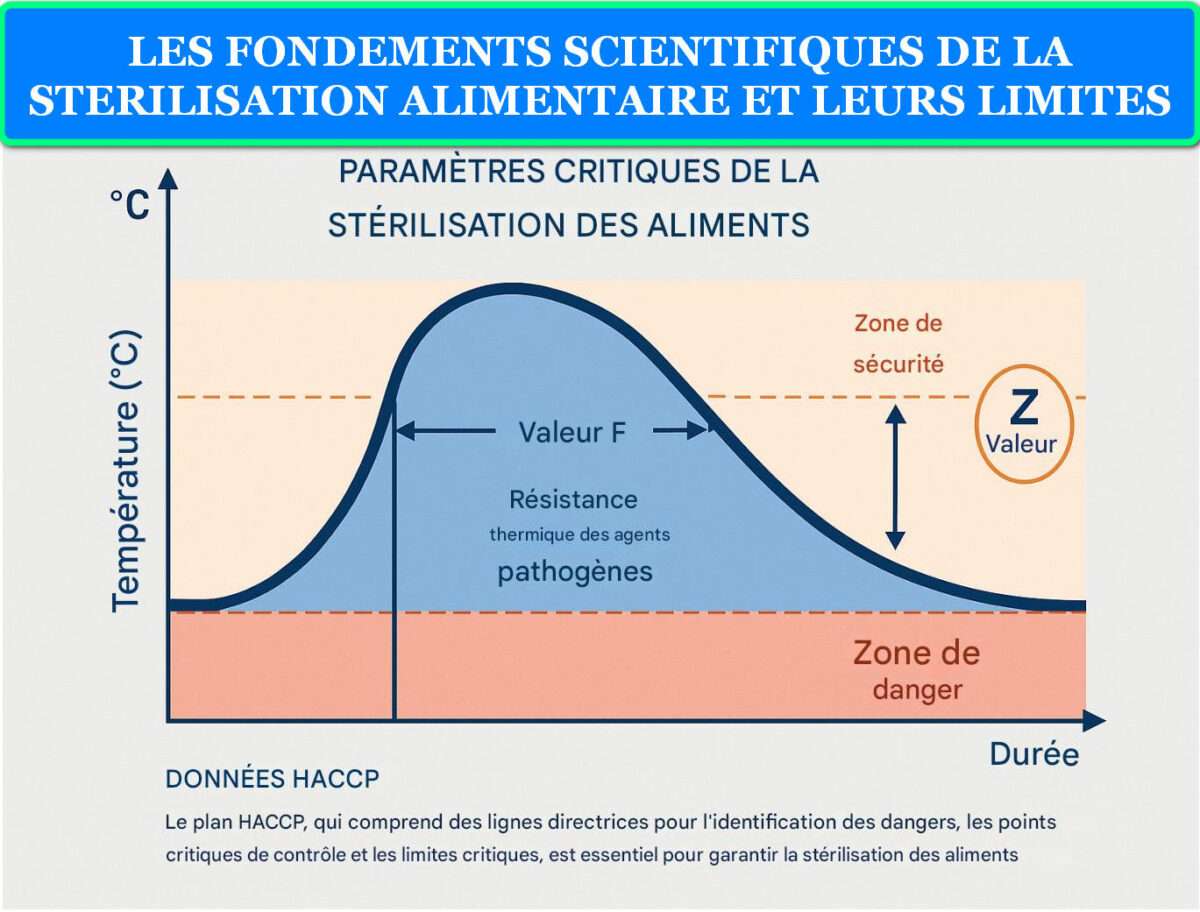
La stérilisation au four repose sur l’utilisation de la chaleur sèche pour éliminer les micro-organismes pathogènes présents sur les surfaces des pots Mason et leurs accessoires. Contrairement à la stérilisation par chaleur humide, cette méthode utilise des températures élevées (généralement entre 140°C et 180°C) pendant des durées spécifiques pour atteindre l’efficacité antimicrobienne requise.
Le processus de stérilisation au four suit les principes de la thermodynamique appliquée à la destruction microbienne. La relation temps-température est cruciale : plus la température est élevée, plus le temps de traitement nécessaire est réduit. Cette relation suit généralement une courbe logarithmique, où chaque augmentation de 10°C divise approximativement par deux le temps nécessaire pour atteindre le même niveau de stérilisation.
Les avantages de cette méthode incluent la facilité de mise en œuvre avec un équipement domestique standard, la capacité de traiter plusieurs pots simultanément, et l’absence de manipulation d’eau bouillante. Cependant, il est essentiel de comprendre que cette technique présente certaines limitations, notamment en termes de pénétration de la chaleur et d’uniformité du traitement thermique.
2. Matériel nécessaire et préparation

2.1 Équipement principal
Le matériel requis pour une stérilisation efficace au four comprend plusieurs éléments essentiels. En premier lieu, un four domestique capable de maintenir des températures stables entre 140°C et 180°C est indispensable. La précision du thermostat est cruciale, car des variations de température peuvent compromettre l’efficacité du processus.
- Pots Mason : Utilisez exclusivement des pots en verre borosilicate ou verre trempé, résistants aux chocs thermiques. Les pots en verre ordinaire peuvent se fissurer sous l’effet des changements de température.
- Couvercles métalliques : Les couvercles doivent être neufs ou en parfait état, sans déformation ni corrosion. Les couvercles usagés peuvent présenter des défauts d’étanchéité.
- Joints d’étanchéité : Vérifiez l’intégrité des joints en caoutchouc ou silicone. Remplacez systématiquement les joints présentant des signes d’usure, de durcissement ou de fissuration.
- Thermomètre de four : Un thermomètre indépendant permet de vérifier la précision du thermostat du four et d’assurer un contrôle température optimal.
- Gants de protection thermique : Indispensables pour manipuler les pots chauds sans risque de brûlure.
- Grilles de refroidissement : Permettent un refroidissement uniforme et graduel des pots après stérilisation.
2.2 Préparation préliminaire

La préparation minutieuse des pots constitue une étape fondamentale du processus. Commencez par un nettoyage approfondi à l’eau chaude savonneuse, en utilisant une brosse à récurer pour éliminer tous résidus alimentaires ou dépôts calcaires. Rincez abondamment à l’eau claire pour éliminer toute trace de détergent.
L’inspection visuelle est cruciale : examinez chaque pot sous un éclairage adequat pour détecter d’éventuelles fissures, éclats ou défauts du verre. Un pot endommagé peut exploser sous l’effet de la chaleur et compromettre la sécurité de l’opération. De même, vérifiez le filetage du col des pots pour vous assurer qu’il n’est pas déformé ou endommagé.
Le séchage complet est impératif avant la mise au four. L’humidité résiduelle peut provoquer un choc thermique et endommager les pots. Utilisez un torchon propre et sec, ou laissez sécher à l’air libre sur une surface propre. Évitez l’utilisation de papier absorbant qui pourrait laisser des résidus de fibres.
3. Processus de stérilisation détaillé
3.1 Paramètres de température et durée
Attention : Les paramètres suivants sont spécifiquement adaptés à la stérilisation des contenants vides. Pour la stérilisation de conserves alimentaires, des protocoles différents et plus stricts s’appliquent.
| Température du four | Durée de traitement | Type de contenant | Efficacité antimicrobienne |
|---|---|---|---|
| 140°C | 60 minutes | Pots 250ml-500ml | Stérilisation standard |
| 160°C | 30 minutes | Pots 250ml-1L | Stérilisation renforcée |
| 180°C | 15 minutes | Tous formats | Stérilisation intensive |
3.2 Placement dans le four

Le positionnement des pots dans le four revêt une importance capitale pour assurer une stérilisation homogène. Placez les pots sur la grille centrale du four, en veillant à maintenir un espacement minimum de 2,5 cm entre chaque pot. Cette distance permet une circulation d’air optimale et évite les zones de surchauffe ou de sous-chauffage.
Les couvercles et joints doivent être traités séparément des pots. Disposez-les sur une plaque de cuisson en métal, face interne vers le haut, pour maximiser l’exposition à la chaleur. Cette séparation évite également les déformations dues à la dilatation thermique différentielle entre le verre et le métal.

3.3 Contrôle du processus
Le contrôle rigoureux des paramètres durant le processus de stérilisation est essentiel pour garantir l’efficacité du traitement. Utilisez un thermomètre de four indépendant pour vérifier la stabilité de la température. Les variations ne doivent pas excéder ±5°C par rapport à la température cible.
Le préchauffage du four à la température désirée avant l’introduction des pots est crucial. Cette étape peut prendre 15 à 20 minutes selon le type de four. N’introduisez les pots qu’une fois la température stabilisée pour éviter les chocs thermiques et assurer un traitement uniforme dès le début du cycle.
Durant le traitement, évitez d’ouvrir la porte du four, car cela provoquerait des fluctuations de température importantes. Si une vérification s’avère nécessaire, utilisez l’éclairage interne du four et limitez l’ouverture au strict minimum.
4. Inspection et vérification post-stérilisation

4.1 Refroidissement contrôlé
Le refroidissement des pots après stérilisation doit être graduel pour éviter les chocs thermiques susceptibles de provoquer des fissures ou des bris. Éteignez le four et laissez les pots refroidir à l’intérieur pendant 10 à 15 minutes avec la porte entrouverte. Cette étape permet une diminution progressive de la température.
Retirez ensuite les pots du four en utilisant des gants de protection thermique appropriés. Placez-les sur une grille de refroidissement ou une surface isolante, en évitant le contact direct avec des surfaces froides comme un plan de travail en pierre ou en métal. Un torchon épais peut servir d’isolant thermique.
4.2 Contrôles d’intégrité
Une fois les pots refroidis à température ambiante (environ 30-45 minutes), procédez à un examen minutieux de leur intégrité. Inspectez visuellement chaque pot à la recherche de fissures, même microscopiques, qui pourraient compromettre l’étanchéité future. Portez une attention particulière aux zones de contrainte comme le col et le fond du pot.
Testez l’étanchéité des couvercles en effectuant un assemblage à vide avec les joints. Le couvercle doit se visser facilement sans forcer, et le joint doit se positionner correctement dans sa gorge. Un joint déformé par la chaleur doit être remplacé immédiatement.
Vérifiez l’absence de déformation des couvercles métalliques. Une déformation, même légère, peut affecter l’étanchéité et compromettre la conservation des aliments. Les couvercles présentant des signes de gauchissement ou de déformation doivent être écartés.
5. Conservation et stockage optimal

5.1 Conditions de stockage
Le stockage des pots stérilisés requiert des précautions spécifiques pour maintenir leur stérilité jusqu’à l’utilisation. Entreposez les pots dans un environnement propre, sec et à l’abri de la poussière. Un placard fermé ou une armoire dédiée constitue l’espace de stockage idéal.
La température de stockage doit être stable, idéalement entre 10°C et 25°C, avec une humidité relative inférieure à 70%. Les variations importantes de température et d’humidité peuvent affecter l’intégrité des joints et favoriser la condensation à l’intérieur des pots.
Évitez l’exposition directe à la lumière solaire qui peut dégrader certains composants des joints et affecter la transparence du verre. Utilisez des étagères en matériaux non corrosifs et facilement nettoyables, comme l’acier inoxydable ou le plastique alimentaire.
5.2 Durée de conservation de la stérilité
La stérilité des pots Mason correctement traités et stockés peut être maintenue pendant plusieurs mois dans des conditions optimales. Cependant, il est recommandé d’utiliser les pots stérilisés dans un délai de 6 mois pour garantir une efficacité antimicrobienne maximale.
Avant utilisation, inspectez toujours visuellement les pots pour détecter toute contamination visible ou altération. En cas de doute sur l’intégrité de la stérilisation, répétez le processus plutôt que de risquer une contamination des aliments.
6. Avantages et inconvénients de la méthode
6.1 Avantages significatifs
La stérilisation au four présente plusieurs avantages pratiques qui en font une méthode attrayante pour de nombreux utilisateurs domestiques. La simplicité du processus constitue le premier atout : il suffit d’un four domestique standard et de quelques accessoires basiques pour réaliser une stérilisation efficace.
La capacité de traitement élevée représente un autre avantage majeur. Un four standard peut accueillir simultanément 12 à 20 pots selon leur taille, permettant de préparer de grandes quantités de contenants en une seule opération. Cette efficacité est particulièrement appréciée lors des périodes de conserves intensives.
L’absence de manipulation d’eau bouillante élimine les risques de brûlures par éclaboussures et simplifie considérablement la logistique de l’opération. Cette caractéristique rend la méthode accessible aux personnes ayant des limitations physiques ou peu d’expérience en conservation alimentaire.
Le contrôle précis des paramètres temps-température offre une reproductibilité excellente. Une fois les réglages optimisés pour un type de four donné, le processus peut être répété de manière cohérente avec des résultats prévisibles.
6.2 Limitations et inconvénients
Malgré ses avantages, la stérilisation au four présente certaines limitations qu’il convient de considérer. La pénétration de la chaleur sèche est moins efficace que celle de la vapeur d’eau, particulièrement pour les matières organiques complexes. Cette limitation peut affecter l’efficacité antimicrobienne dans certaines conditions.
La consommation énergétique est généralement plus élevée que les méthodes alternatives, en raison des températures élevées et des durées de traitement prolongées. Cette considération peut être importante dans une perspective de développement durable.
Les variations de température entre les différentes zones du four peuvent créer des conditions de stérilisation inégales. Cette hétérogénéité nécessite une attention particulière au placement des pots et peut limiter la capacité de traitement effective.
Enfin, cette méthode n’est pas appropriée pour tous les types de conserves alimentaires. Elle convient principalement à la stérilisation des contenants vides, mais ne peut remplacer les méthodes de stérilisation alimentaire spécialisées pour les conserves à haute acidité ou les plats préparés.
7. Erreurs courantes et prévention
7.1 Erreurs de température et de timing
L’une des erreurs les plus fréquentes consiste à se fier uniquement au thermostat du four sans vérification indépendante. Les thermostats domestiques peuvent présenter des écarts de précision de ±15°C à ±25°C, ce qui peut compromettre significativement l’efficacité de la stérilisation. L’utilisation d’un thermomètre de four séparé est donc indispensable.
Le non-respect des durées de traitement représente une autre erreur critique. Certains utilisateurs tentent d’accélérer le processus en augmentant la température au-delà des recommandations, risquant d’endommager les pots ou de créer des conditions de traitement inadéquates. D’autres réduisent arbitrairement les durées, compromettant l’efficacité antimicrobienne.
L’introduction de pots froids dans un four très chaud constitue une erreur majeure pouvant provoquer des chocs thermiques et des bris. Le préchauffage progressif ou l’introduction des pots dans un four froid qui monte ensuite en température représente la pratique recommandée.
7.2 Erreurs de manipulation et de préparation
L’utilisation de pots présentant des défauts mineurs (petites rayures, micro-fissures) représente un risque significatif. Ces défauts peuvent s’aggraver sous l’effet de la chaleur et provoquer des bris dangereux. Une inspection rigoureuse préalable est donc cruciale.
Le placement incorrect des pots dans le four, avec un espacement insuffisant, peut créer des zones de surchauffe localisée et compromettre l’uniformité du traitement. Cette erreur est particulièrement fréquente lorsque l’utilisateur tente de maximiser la capacité de traitement au détriment de la qualité.
L’omission du traitement séparé des couvercles et joints constitue une erreur classique. Ces éléments nécessitent un traitement spécifique en raison de leurs propriétés thermiques différentes et de leur rôle critique dans l’étanchéité finale.
7.3 Mesures préventives
La mise en place d’un protocole standardisé constitue la meilleure prévention contre les erreurs. Ce protocole doit inclure une check-list détaillée couvrant chaque étape du processus, de la préparation au stockage final.
La formation et la sensibilisation aux bonnes pratiques sont essentielles, particulièrement pour les utilisateurs novices. La compréhension des principes physiques sous-jacents permet une meilleure appropriation des procédures et une détection plus efficace des anomalies.
L’investissement dans un équipement de qualité (thermomètre précis, gants adaptés, grilles appropriées) représente un investissement rentable à long terme en termes de sécurité et d’efficacité.
8. Comparaison avec les méthodes alternatives
8.1 Stérilisation à l’eau bouillante
La méthode traditionnelle de stérilisation à l’eau bouillante demeure la référence en matière de conservation alimentaire domestique. Cette technique utilise la chaleur humide à 100°C pour détruire les micro-organismes, avec une efficacité antimicrobienne généralement supérieure à la chaleur sèche.
Les avantages de la méthode à l’eau bouillante incluent une pénétration thermique plus efficace, une température de traitement plus basse (économie d’énergie), et une validation scientifique plus extensive. Cette méthode est également recommandée par la plupart des organismes de sécurité alimentaire.
Cependant, elle présente des inconvénients pratiques : manipulation d’eau bouillante, capacité de traitement limitée par la taille des récipients, et nécessité d’équipements spécialisés (stérilisateur, pinces de manipulation). Le risque de brûlures par éclaboussures est également plus élevé.
8.2 Stérilisation à la vapeur
Les autoclaves domestiques ou stérilisateurs à vapeur représentent une solution intermédiaire entre les méthodes traditionnelles et la stérilisation au four. Ces appareils utilisent la vapeur sous pression pour atteindre des températures supérieures à 100°C avec une efficacité antimicrobienne maximale.
Cette méthode offre une excellente uniformité de traitement, des temps de cycle plus courts, et une efficacité antimicrobienne supérieure. Elle convient également au traitement des aliments acides et peu acides selon des protocoles validés.
L’inconvénient principal réside dans le coût d’acquisition de l’équipement et la complexité relative de mise en œuvre. La maintenance et l’étalonnage réguliers sont également nécessaires pour maintenir les performances optimales.
8.3 Méthodes chimiques
Les solutions de stérilisation chimique (hypochlorite de sodium, acide peracétique, ozone) offrent une alternative intéressante pour certaines applications. Ces méthodes ne nécessitent pas de chauffage et peuvent traiter des matériaux thermosensibles.
L’efficacité antimicrobienne peut être excellente avec des temps de contact appropriés. La consommation énergétique est minimale, et le traitement peut être réalisé à température ambiante.
Cependant, ces méthodes présentent des contraintes importantes : nécessité de rinçage complet pour éliminer les résidus chimiques, risques de corrosion des composants métalliques, et préoccupations environnementales liées à l’utilisation de produits chimiques.
9. Applications spécialisées et recommandations
9.1 Conservation de confitures et gelées
Pour la préparation de pots destinés aux confitures et gelées, la stérilisation au four présente des avantages particuliers. Ces préparations à haute teneur en sucre créent un environnement défavorable au développement microbien, réduisant les exigences de stérilisation strictes.
Utilisez une température de 160°C pendant 20 minutes pour des pots de 250 à 500 ml destinés aux confitures. Assurez-vous que les pots sont parfaitement secs avant utilisation, car l’humidité résiduelle peut affecter la texture et la conservation des confitures.
Remplissez les pots chauds avec la confiture encore chaude (85-90°C) pour créer un vide partiel lors du refroidissement. Cette technique améliore l’étanchéité et prolonge la durée de conservation.
9.2 Préparation pour conserves acides
Les conserves d’aliments acides (pH < 4,6) comme les cornichons, chutneys, et sauces tomates peuvent bénéficier de contenants stérilisés au four. L’acidité naturelle de ces préparations inhibe le développement des bactéries pathogènes dangereuses.
Pour ces applications, une stérilisation à 140°C pendant 45 minutes peut suffire, compte tenu de la protection supplémentaire offerte par l’acidité. Vérifiez toujours le pH de vos préparations avec des bandelettes ou un pH-mètre pour confirmer le niveau d’acidité requis.
9.3 Stockage de produits secs
La stérilisation au four excelle pour la préparation de pots destinés au stockage de produits secs : épices, herbes séchées, céréales, légumineuses. Ces applications ne nécessitent pas les standards stricts des conserves alimentaires humides.
Une température de 120°C pendant 30 minutes suffit généralement pour ces applications. Assurez-vous que les pots sont complètement refroidis et parfaitement secs avant le remplissage pour éviter la condensation qui pourrait favoriser le développement de moisissures.
10. Aspects réglementaires et normatifs
10.1 Réglementations nationales
La réglementation française en matière de conservation alimentaire domestique est principalement basée sur les recommandations de l’ANSES (Agence nationale de sécurité sanitaire de l’alimentation). Ces recommandations privilégient les méthodes validées scientifiquement, principalement la stérilisation à l’eau bouillante pour les conserves domestiques.
Bien que la stérilisation au four ne soit pas explicitement interdite pour la préparation de contenants, elle n’est pas non plus officiellement recommandée pour le traitement des conserves alimentaires. Cette nuance réglementaire doit être prise en compte dans l’évaluation des risques.
Pour les applications commerciales ou semi-commerciales, des standards plus stricts s’appliquent, nécessitant généralement l’utilisation de méthodes validées selon les normes HACCP et les réglementations européennes en vigueur.
10.2 Standards internationaux
Les standards internationaux ISO 11139 et ISO 17665 définissent les exigences pour la stérilisation par chaleur humide, mais ne couvrent pas spécifiquement la stérilisation par chaleur sèche des contenants alimentaires domestiques.
Les recommandations de l’USDA (United States Department of Agriculture) et du CDC (Centers for Disease Control) américains reconnaissent la stérilisation au four pour certaines applications spécifiques, mais avec des protocoles stricts et des limitations d’usage clairement définies.
Conclusion
La stérilisation des pots Mason au four représente une méthode accessible et pratique pour la préparation de contenants destinés à la conservation alimentaire domestique. Cette technique, bien que présentant certaines limitations par rapport aux méthodes traditionnelles, offre des avantages significatifs en termes de simplicité, de capacité de traitement et de sécurité de manipulation.
Le succès de cette méthode repose sur le respect scrupuleux des paramètres temps-température, une préparation minutieuse des contenants, et une compréhension claire des applications appropriées. Les erreurs courantes peuvent être évitées par la mise en place de protocoles standardisés et l’utilisation d’équipements de contrôle appropriés.
Il est essentiel de reconnaître que cette méthode convient principalement à la stérilisation de contenants vides et à certaines applications spécialisées. Pour la conservation d’aliments à risque élevé ou la production de conserves à longue durée de vie, les méthodes validées scientifiquement demeurent recommandées.
L’évolution des technologies domestiques et l’amélioration des connaissances en microbiologie alimentaire pourront à l’avenir élargir les applications de cette méthode. En attendant, son utilisation judicieuse dans le respect des bonnes pratiques peut contribuer efficacement à la sécurité et à la qualité des conserves domestiques.
La formation continue et l’information des utilisateurs restent cruciales pour maximiser les bénéfices de cette technique tout en minimisant les risques associés. L’investissement dans des équipements de qualité et le respect des protocoles établis constituent les clés du succès pour cette méthode de stérilisation alternative.
Rappel important : Cette méthode est recommandée pour la stérilisation de contenants vides uniquement. Pour la conservation d’aliments, consultez toujours les recommandations officielles des organismes de sécurité alimentaire et utilisez des méthodes validées scientifiquement.


















:max_bytes(150000):strip_icc()/SES-sterilize-jars-for-jams-and-preserves-435340-352de05aaf3c452bab5b37247b32ee16.jpg)





.jpg)