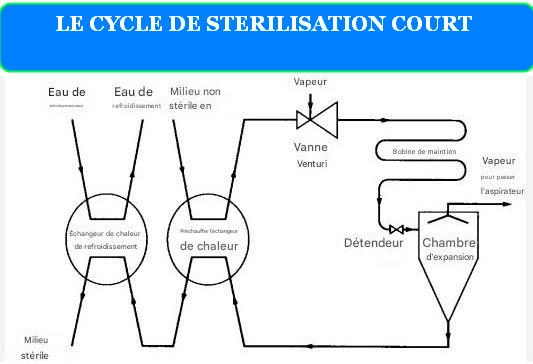
LE CYCLE DE STÉRILISATION COURT : UNE SOLUTION EFFICACE POUR LES AUTOCLAVES MODERNES

CHAPITRE 1 : INTRODUCTION – LE BESOIN DE RAPIDITÉ DANS LA STÉRILISATION MODERNE
Dans le contexte hospitalier contemporain marqué par une exigence croissante d’efficience opérationnelle et de rentabilité économique stricte, la gestion optimale du flux d’instruments chirurgicaux représente un défi majeur et permanent pour l’ensemble des établissements de santé à travers le monde entier. Les blocs opératoires modernes, véritables centres névralgiques des hôpitaux universitaires et des cliniques spécialisées, fonctionnent désormais sous une pression constante et multifactorielle visant à maximiser le nombre d’interventions chirurgicales réalisées quotidiennement tout en maintenant rigoureusement les standards de sécurité microbiologique les plus élevés imposés par les autorités sanitaires nationales et internationales.
Cette contrainte temporelle s’avère particulièrement critique dans un environnement où chaque minute d’immobilisation d’une salle opératoire représente un coût financier substantiel et mesurable. En Europe, le coût d’exploitation d’un bloc opératoire varie entre soixante et quatre-vingts euros par minute selon les spécialités chirurgicales concernées et la complexité des équipements utilisés. Aux États-Unis, ce coût atteint cinquante à soixante-dix dollars par minute, représentant une pression économique considérable pour les gestionnaires hospitaliers. Dans ce contexte, l’optimisation des processus de stérilisation devient un enjeu stratégique majeur pour la viabilité économique des établissements de soins.
L’évolution historique de la stérilisation par vapeur d’eau saturée remonte aux travaux pionniers de Charles Chamberland en 1879 et de Louis Pasteur dans les années 1880. Cette méthode, perfectionnée au cours du vingtième siècle, a établi les fondements scientifiques de la stérilisation moderne. Cependant, les protocoles traditionnels développés dans les années 1950 imposaient des cycles de stérilisation d’une durée totale de trente-cinq à quarante-cinq minutes, incluant les phases de conditionnement, de montée en température, de maintien du plateau thermique et de séchage final. Cette durée, bien que nécessaire pour garantir l’efficacité antimicrobienne, est devenue progressivement incompatible avec les exigences de rapidité imposées par la médecine moderne.
La problématique des cycles longs traditionnels se manifeste particulièrement dans plusieurs situations cliniques critiques. Lorsqu’un instrument chirurgical tombe accidentellement sur le sol pendant une intervention, l’attente de quarante-cinq minutes pour sa restérilisation peut compromettre le déroulement de l’acte chirurgical. De même, lorsqu’un plateau d’instrumentation se révèle incomplet une fois la procédure commencée, ou lorsqu’une urgence chirurgicale survient alors que tous les sets d’instruments de la spécialité sont en cours d’utilisation, cette contrainte temporelle devient inacceptable pour la sécurité du patient et l’efficacité du service.
C’est dans ce contexte exigeant qu’ont émergé les cycles de stérilisation courts, également appelés cycles flash ou IUSS (Immediate Use Steam Sterilization) selon la terminologie anglo-saxonne. Ces cycles révolutionnaires permettent de réduire drastiquement le temps de traitement à trois ou quatre minutes d’exposition effective, grâce à l’élévation de la température de stérilisation de cent vingt et un degrés Celsius à cent trente-quatre degrés Celsius. Cette innovation technologique majeure transforme radicalement la gestion des urgences chirurgicales en permettant de retraiter un instrument ou de compléter un plateau chirurgical en moins de quinze minutes au total.
L’impact économique des cycles de stérilisation courts s’avère considérable et mesurable. Dans un hôpital universitaire européen de mille lits réalisant environ cinquante à quatre-vingts cycles de stérilisation quotidiens, chaque minute gagnée sur la durée d’un cycle se traduit par une économie annuelle estimée à plusieurs dizaines de milliers d’euros. Cette économie prend en compte les coûts directs d’énergie et de main-d’œuvre, mais surtout les revenus générés par l’augmentation du nombre d’interventions chirurgicales possibles. L’optimisation du temps de stérilisation contribue directement à l’amélioration de la rentabilité opérationnelle des établissements de santé en permettant une rotation plus rapide des salles d’opération.
Cependant, cette révolution technologique soulève des enjeux complexes de sécurité microbiologique versus productivité qui nécessitent une approche scientifique rigoureuse. Les autorités sanitaires internationales, notamment la Food and Drug Administration aux États-Unis, l’Agence Nationale de Sécurité du Médicament en France, et le Ministry of Health, Labour and Welfare au Japon, ont établi des directives strictes encadrant l’utilisation des cycles courts. Ces cycles ne doivent être employés que dans des conditions très spécifiques, pour des instruments non emballés destinés à un usage immédiat, et ne conviennent pas à la stérilisation d’instruments implantables ou de dispositifs médicaux complexes comportant des lumières étroites.
CHAPITRE 2 : PRINCIPES TECHNIQUES DU CYCLE DE STÉRILISATION COURT

Le fonctionnement optimal des cycles de stérilisation courts repose fondamentalement sur des principes thermodynamiques précis et parfaitement maîtrisés qui permettent d’atteindre une efficacité stérilisante rigoureusement équivalente voire supérieure à celle des cycles standards traditionnels. La clé scientifique de cette performance remarquable réside dans l’application de la loi d’Arrhenius, établie en 1889 par le chimiste suédois Svante Arrhenius, qui décrit mathématiquement la relation exponentielle existant entre la température de traitement et l’efficacité léthale du procédé de stérilisation.
Cette loi fondamentale démontre qu’une élévation relativement modeste de la température de stérilisation entraîne une augmentation disproportionnée de la vitesse de destruction des microorganismes. Concrètement, chaque augmentation de dix degrés Celsius de la température de stérilisation multiplie par un facteur deux à trois la vitesse de destruction microbienne, permettant ainsi de réduire proportionnellement le temps d’exposition nécessaire pour obtenir le même niveau d’assurance stérile. Cette relation logarithmique constitue le fondement scientifique qui justifie l’efficacité des cycles de stérilisation courts.
Les paramètres critiques des cycles de stérilisation courts sont rigoureusement définis et contrôlés : température de cent trente-quatre degrés Celsius exactement, pression de deux virgule un à deux virgule deux bars au-dessus de la pression atmosphérique, et durée d’exposition de trois à quatre minutes précisément chronométrées. Ces valeurs ne sont pas arbitraires mais résultent de décennies de recherche en microbiologie appliquée visant à optimiser le compromis entre efficacité antimicrobienne et rapidité de traitement.
La comparaison directe entre les cycles standards et les cycles courts illustre parfaitement les bénéfices de cette approche. Un cycle standard traditionnel opère à cent vingt et un degrés Celsius pendant quinze minutes d’exposition, tandis qu’un cycle court atteint cent trente-quatre degrés Celsius pendant seulement trois à quatre minutes. Malgré cette réduction drastique du temps d’exposition, l’efficacité antimicrobienne demeure identique, voire supérieure, grâce à l’intensité thermique accrue.
L’indicateur biologique de référence utilisé pour valider l’efficacité des cycles de stérilisation est Geobacillus stearothermophilus, anciennement dénommé Bacillus stearothermophilus. Cette bactérie sporulée a été sélectionnée comme standard universel en raison de sa résistance thermique exceptionnelle. Sa valeur D, qui représente le temps nécessaire pour réduire de quatre-vingt-dix pourcent la population viable, varie de une virgule cinq à deux virgule cinq minutes à cent vingt et un degrés Celsius. À cent trente-quatre degrés Celsius, cette valeur D chute dramatiquement à zéro virgule deux à zéro virgule trois minute, confirmant l’efficacité accrue des températures élevées.
Le système de vide fractionné constitue un élément technique fondamental des cycles de stérilisation courts. Cette technologie sophistiquée utilise une séquence de trois à quatre impulsions alternées de vide poussé et d’injection de vapeur pour éliminer méthodiquement l’air résiduel présent dans la chambre de stérilisation et piégé dans les cavités complexes des instruments chirurgicaux. Cette élimination complète de l’air s’avère absolument critique car l’air possède une conductivité thermique cinquante fois inférieure à celle de la vapeur d’eau, constituant un obstacle majeur à la transmission uniforme de la chaleur.
La cinétique de montée en température dans les autoclaves modernes conçus pour les cycles courts atteint des performances remarquables. Ces équipements de nouvelle génération peuvent atteindre cent trente-quatre degrés Celsius en moins de deux minutes à partir de la température ambiante, grâce à des générateurs de vapeur surdimensionnés capables de fournir instantanément plusieurs dizaines de kilogrammes de vapeur par heure. Cette rapidité de montée s’avère essentielle pour minimiser le temps total du cycle et maximiser la productivité du service de stérilisation.
La phase de séchage rapide par vide pulsé représente l’une des innovations technologiques les plus significatives des cycles courts. Contrairement aux cycles standards qui nécessitent dix à vingt minutes de séchage pour éliminer complètement l’humidité des emballages textiles, les cycles courts destinés à des instruments non emballés réduisent cette phase à une ou deux minutes seulement. Cette réduction drastique est rendue possible par l’absence d’emballages absorbants et par l’utilisation de systèmes de vide pulsé perfectionnés.
Le calcul de la réduction logarithmique obtenue avec les cycles courts démontre leur supériorité théorique sur les cycles standards. Avec une exposition de trois à quatre minutes à cent trente-quatre degrés Celsius, la réduction logarithmique atteint douze à vingt logarithmes, largement supérieure aux six logarithmes minimum requis par les normes internationales. Cette marge de sécurité substantielle garantit une efficacité antimicrobienne absolue, même en présence de bioburden initial élevé ou de conditions légèrement dégradées.
CHAPITRE 3 : NORMES ET STANDARDS INTERNATIONAUX

La réglementation internationale des cycles de stérilisation courts s’articule autour d’un corpus normatif complexe et évolutif qui reflète l’importance stratégique de cette technologie pour la sécurité des patients et l’efficacité des soins hospitaliers. En Europe, la norme EN 13060:2015 constitue le référentiel technique fondamental qui régit la conception, la fabrication, l’installation et l’utilisation des petits stérilisateurs à vapeur d’eau. Cette norme établit une classification rigoureuse des autoclaves en trois catégories distinctes selon leurs capacités techniques et leurs domaines d’application spécifiques.
Les autoclaves de classe B (Big chamber) représentent le niveau technologique le plus élevé et sont spécifiquement conçus pour traiter tous types de charges, incluant les instruments pleins, creux, poreux et emballés. Ces équipements sophistiqués intègrent obligatoirement un système de vide fractionné en phase de conditionnement et un séchage par vide pulsé en fin de cycle. Les cycles courts sur ces autoclaves bénéficient de performances optimales grâce à cette technologie avancée de gestion du vide qui garantit une pénétration homogène de la vapeur dans toutes les cavités instrumentales.
Les autoclaves de classe S (Specified) sont conçus selon les spécifications définies par le fabricant pour traiter des charges particulières clairement identifiées. Cette catégorie intermédiaire permet une adaptation précise aux besoins spécifiques de certaines applications cliniques tout en maintenant un niveau de performance élevé. Les cycles courts sur les autoclaves classe S nécessitent une validation spécifique pour chaque type de charge traitée, conformément aux recommandations du fabricant et aux exigences réglementaires locales.
Les autoclaves de classe N (Non-vacuum) fonctionnent sans système de vide préalable et sont limités au traitement d’instruments pleins non emballés exclusivement. Bien que techniquement capables de réaliser des cycles courts, ces équipements présentent des limitations importantes en termes de pénétration de vapeur dans les instruments creux et nécessitent des précautions particulières lors de leur utilisation pour des applications critiques.
La norme européenne EN 13060:2015 impose des exigences spécifiques particulièrement strictes pour les cycles courts, notamment l’obligation de réaliser quotidiennement des tests de qualification instrumentale. Le test de Bowie & Dick, effectué avec un pack d’épreuve standardisé, vérifie l’efficacité du vide et la qualité de pénétration de la vapeur. Le test Helix, utilisant un tube spiral de longueur définie, contrôle spécifiquement la capacité de la vapeur à pénétrer dans les lumières étroites des instruments chirurgicaux complexes.
Au niveau international, la norme ISO 17665:2024 « Stérilisation des produits de santé – Chaleur humide » constitue la référence mondiale pour le développement, la validation et le contrôle de routine des procédés de stérilisation par vapeur d’eau. Cette norme de dernière génération, révisée en 2024, intègre les avancées technologiques les plus récentes et harmonise les exigences techniques à l’échelle planétaire. Elle définit précisément le concept de SAL (Sterility Assurance Level) qui doit être inférieur ou égal à 10⁻⁶, signifiant statistiquement qu’il existe moins d’une chance sur un million qu’un article traité demeure contaminé après stérilisation.
La norme ISO 17665:2024 distingue deux approches méthodologiques pour la validation des cycles de stérilisation : l’approche full-cycle qui valide l’ensemble du cycle de stérilisation incluant toutes ses phases, et l’approche partial-cycle qui se concentre uniquement sur la phase de stérilisation proprement dite. Pour les cycles courts, l’approche full-cycle est généralement privilégiée en raison de la réduction des marges de sécurité temporelles qui nécessite une validation exhaustive de toutes les phases du procédé.
Aux États-Unis, la réglementation fédérale 21 CFR Part 11 de la Food and Drug Administration établit les exigences applicables aux équipements de stérilisation utilisés dans l’industrie pharmaceutique. Cette réglementation impose des standards particulièrement stricts en matière de traçabilité électronique, de sécurité des données et de validation des systèmes informatisés. Les autoclaves utilisés pour les cycles courts dans les établissements pharmaceutiques américains doivent impérativement se conformer à ces exigences fédérales sous peine de sanctions réglementaires sévères.
L’Association for the Advancement of Medical Instrumentation (AAMI) publie la norme ST79:2023 « Immediate Use Steam Sterilization (IUSS) » qui constitue la référence technique spécifique aux cycles de stérilisation courts aux États-Unis. Cette norme détaille précisément les conditions d’utilisation acceptables, les limitations techniques, les exigences de formation du personnel et les protocoles de validation obligatoires. Elle insiste particulièrement sur le caractère exceptionnel de l’utilisation des cycles courts qui ne doivent jamais se substituer aux cycles standards pour les applications de routine.
Les Centers for Disease Control and Prevention (CDC) ont publié des directives complémentaires intitulées « Guidelines for Disinfection and Sterilization in Healthcare Facilities » qui précisent les bonnes pratiques d’utilisation des cycles courts dans le contexte hospitalier américain. Ces recommandations soulignent l’importance de la formation continue du personnel, de la maintenance préventive des équipements et de la surveillance microbiologique régulière des procédés.
Au Japon, le Ministry of Health, Labour and Welfare (MHLW) a établi une réglementation nationale spécifique qui s’articule autour de la Japanese QMS Ordinance (Quality Management System) et des directives techniques publiées par la Pharmaceuticals and Medical Devices Agency (PMDA). Cette réglementation nippone se caractérise par des exigences particulièrement rigoureuses en matière de documentation et de traçabilité, reflétant la culture japonaise de la qualité totale et de l’amélioration continue.
| Région | Norme principale | Température cycle court | Durée exposition | Fréquence validation |
|---|---|---|---|---|
| Europe | EN 13060:2015 | 134°C | 3-4 minutes | Tests quotidiens |
| International | ISO 17665:2024 | 132-134°C | 3-4 minutes | Selon validation |
| USA | AAMI ST79:2023 | 132°C (270°F) | 3 minutes | Mensuelle minimum |
| Japon | MHLW QMS | 134°C | 3-4 minutes | Trimestrielle |
CHAPITRE 4 : TYPES DE CYCLES COURTS ET APPLICATIONS

La technologie des cycles de stérilisation courts se décline en plusieurs variantes spécialisées, chacune optimisée pour des applications cliniques spécifiques et des contraintes opérationnelles particulières. Cette diversification technique répond à la nécessité d’adapter précisément les paramètres de stérilisation aux caractéristiques physiques et aux exigences de sécurité des différents types d’instruments et dispositifs médicaux traités dans les établissements de santé contemporains.
Le cycle flash non emballé représente la configuration la plus couramment utilisée dans la pratique hospitalière quotidienne. Ce cycle opère à une température de cent trente-deux à cent trente-quatre degrés Celsius pendant exactement trois minutes d’exposition effective. Il est spécifiquement conçu pour le traitement d’instruments métalliques nus, directement disposés dans la chambre de stérilisation sans aucun emballage protecteur. Cette absence d’emballage permet une transmission thermique optimale et une évacuation rapide de l’humidité résiduelle, mais impose une utilisation immédiate des instruments traités pour éviter toute recontamination environnementale.
Les instruments éligibles pour le cycle flash non emballé incluent principalement les instruments chirurgicaux métalliques pleins tels que les pinces, ciseaux, porte-aiguilles et écarteurs, ainsi que certains instruments creux de diamètre interne supérieur à cinq millimètres. Cette limitation dimensionnelle découle des contraintes physiques de pénétration de la vapeur dans les espaces confinés, où la présence d’air résiduel peut compromettre l’efficacité du traitement thermique.
Le cycle court emballé constitue une évolution technologique significative qui permet le traitement d’instruments conditionnés dans des conteneurs rigides perméables à la vapeur ou des emballages stériles spécialement conçus pour résister aux conditions thermiques extrêmes. Ce cycle opère à cent trente-quatre degrés Celsius pendant quatre minutes d’exposition, la minute supplémentaire compensant la résistance thermique additionnelle créée par l’emballage. Cette configuration présente l’avantage majeur de maintenir la stérilité des instruments après le cycle, permettant un stockage temporaire et un transport sécurisé vers les zones d’utilisation.
Les emballages compatibles avec les cycles courts emballés doivent impérativement répondre à des spécifications techniques rigoureuses. Ils doivent permettre une pénétration rapide de la vapeur, résister aux températures élevées sans dégradation, et faciliter l’évacuation de l’humidité durante la phase de séchage. Les conteneurs rigides métalliques perforés et les emballages papier-plastique haute température constituent les solutions les plus fréquemment utilisées dans cette application.
Le cycle Prion représente une catégorie très spécialisée développée spécifiquement pour la décontamination des protéines prioniques anormales responsables des encéphalopathies spongiformes transmissibles, notamment la maladie de Creutzfeldt-Jakob et ses variantes. Ce cycle extrême opère à cent trente-quatre degrés Celsius pendant dix-huit minutes d’exposition, durée exceptionnellement longue qui reflète la résistance extraordinaire de ces agents pathogènes non conventionnels aux traitements thermiques standards.
L’utilisation du cycle Prion demeure strictement encadrée par des protocoles spécifiques établis par les autorités sanitaires nationales et les sociétés savantes de neurochirurgie. En France, l’Agence Française de Sécurité Sanitaire des Produits de Santé a publié des recommandations détaillées qui imposent l’utilisation systématique de ce cycle pour tous les instruments ayant été en contact avec le système nerveux central de patients présentant des facteurs de risque de maladie à prions. Cette précaution exceptionnelle découle de la gravité absolue de ces pathologies et de l’absence actuelle de traitement curatif efficace.
Le cycle poreux constitue une innovation récente spécifiquement développée pour optimiser la stérilisation des charges mixtes comportant des éléments poreux tels que les textiles chirurgicaux, les compresses et les champs opératoires. Ce cycle utilise un système de vide pulsé renforcé qui alterne des phases de vide poussé et d’injection de vapeur pour garantir une pénétration homogène dans la structure fibreuse des matériaux poreux. La température de cent trente-quatre degrés Celsius est maintenue pendant trois virgule cinq à quatre minutes, avec une phase de séchage prolongée pour éliminer complètement l’humidité piégée dans les fibres textiles.
Les restrictions d’utilisation des cycles courts constituent un aspect fondamental de la sécurité microbiologique qui ne peut souffrir aucun compromis. L’interdiction formelle d’utilisation pour les dispositifs implantables découle du niveau de risque critique associé à ces articles qui, une fois implantés dans l’organisme, ne peuvent plus être retirés en cas de contamination microbienne. Les prothèses articulaires, les vis et plaques d’ostéosynthèse, les stimulateurs cardiaques et tous les dispositifs destinés à demeurer définitivement dans l’organisme doivent impérativement être stérilisés par des cycles standards offrant des marges de sécurité maximales.
L’interdiction d’utilisation pour les dispositifs comportant des lumières de diamètre inférieur à cinq millimètres résulte des limitations physiques de pénétration de la vapeur dans les espaces confinés. Les endoscopes rigides, les instruments de microchirurgie, les canules d’aspiration de petit calibre et les sondes urétérales nécessitent des temps d’exposition prolongés pour garantir que la vapeur atteigne effectivement toutes les surfaces internes. Les cycles courts ne fournissent pas ce temps de pénétration suffisant, créant un risque inacceptable de survie microbienne dans les zones non atteintes par la vapeur.
L’obligation d’usage immédiat constitue une contrainte opérationnelle majeure qui conditionne l’efficacité de l’ensemble du processus. Les instruments traités par cycles courts doivent être transférés directement de l’autoclave vers le champ opératoire dans un délai maximal de une heure, en utilisant des techniques de transport stérile rigoureusement validées. Cette contrainte temporelle exclut tout stockage, même temporaire, et impose une coordination parfaite entre les services de stérilisation centrale et les équipes chirurgicales utilisatrices.
| Type de cycle | Température | Durée | Emballage | Applications |
|---|---|---|---|---|
| Flash non emballé | 132-134°C | 3 minutes | Non | Instruments pleins métalliques |
| Court emballé | 134°C | 4 minutes | Oui | Conteneurs perméables |
| Prion | 134°C | 18 minutes | Selon protocole | Neurochirurgie à risque |
| Poreux | 134°C | 3,5-4 minutes | Oui | Textiles et charges mixtes |
CHAPITRE 5 : APPLICATIONS CLINIQUES INTERNATIONALES DÉTAILLÉES

Applications en Europe
La Charité de Berlin, l’un des plus prestigieux hôpitaux universitaires européens, constitue un modèle d’excellence dans l’implémentation des cycles de stérilisation courts à grande échelle. Avec plus de cent cinquante mille cycles de stérilisation réalisés annuellement, cet établissement allemand de renommée internationale a développé des protocoles particulièrement sophistiqués pour optimiser l’utilisation des cycles flash tout en maintenant les standards de sécurité les plus élevés. Le service de stérilisation centrale de la Charité traite quotidiennement environ quatre cents cycles, dont quinze à vingt pourcent sont des cycles courts dédiés aux urgences chirurgicales et aux situations de retraitement instrumental.
Le protocole flash de la Charité Berlin opère systématiquement à cent trente-quatre degrés Celsius pendant exactement trois minutes pour les instruments orthopédiques et traumatologiques, spécialités particulièrement consommatrices de cycles d’urgence en raison de la nature imprévisible des interventions d’urgence. L’hôpital a documenté un retour sur investissement remarquable avec une réduction de quarante pourcent du temps global de stérilisation, permettant une augmentation substantielle du nombre d’interventions chirurgicales réalisables quotidiennement dans les vingt-quatre blocs opératoires de l’établissement.
Les Centres Hospitaliers Universitaires français, notamment ceux de Lyon et de Paris, ont adopté massivement les cycles de stérilisation courts en stricte conformité avec la norme européenne EN 285 et les recommandations de l’Agence Française de Sécurité Sanitaire des Produits de Santé. Le CHU de Lyon, avec ses quatre sites hospitaliers et ses soixante-huit blocs opératoires, réalise approximativement deux cents cycles courts quotidiens, principalement pour les spécialités de chirurgie cardiaque, neurochirurgie et orthopédie où les besoins d’instrumentation d’urgence sont particulièrement fréquents et critiques.
La traçabilité électronique obligatoire impose à tous les établissements français un niveau de documentation exemplaire. Chaque cycle de stérilisation, qu’il soit standard ou court, fait l’objet d’un enregistrement informatisé exhaustif incluant les paramètres thermiques, les données de pression, l’identification de l’opérateur, la composition détaillée de la charge et les résultats des contrôles qualité. Cette documentation électronique, conservée pendant quinze ans minimum, permet une traçabilité complète en cas d’incident nosocomial ou de questionnement sur l’efficacité d’un traitement.
La formation continue du personnel de stérilisation constitue une priorité absolue dans tous les CHU français. Des programmes de certification professionnelle, validés par l’Association Française de Normalisation, garantissent que chaque technicien maîtrise parfaitement les spécificités techniques et les limitations des cycles courts. Cette formation théorique et pratique, renouvelée annuellement, couvre les aspects microbiologiques, thermodynamiques, réglementaires et opérationnels indispensables à une utilisation sécurisée de cette technologie avancée.
Le National Health Service britannique a élaboré des directives nationales particulièrement détaillées à travers le document de référence HTM 01-01 « Management and decontamination of surgical instruments used in acute care ». Ces recommandations officielles encadrent strictement l’utilisation des cycles courts dans l’ensemble des hôpitaux publics britanniques, imposant des protocoles standardisés pour garantir l’homogénéité des pratiques sur l’ensemble du territoire. Le NHS estime que l’optimisation des cycles de stérilisation contribue à une économie annuelle de plusieurs millions de livres sterling à l’échelle nationale, tout en améliorant significativement l’efficience opérationnelle des services chirurgicaux.
Applications au Japon
Le Tokyo Medical Center, établissement phare du système hospitalier japonais, a développé une approche particulièrement rigoureuse de l’implémentation des cycles courts, en parfaite cohérence avec les standards exigeants du Ministry of Health, Labour and Welfare japonais. Cet hôpital de huit cents lits, spécialisé dans les pathologies complexes et les techniques chirurgicales de pointe, réalise quotidiennement environ soixante-dix cycles de stérilisation, dont douze à quinze cycles courts réservés aux situations d’urgence strictement définies par des protocoles internes particulièrement détaillés.
La validation trimestrielle avec indicateurs biologiques constitue une spécificité japonaise qui dépasse largement les exigences internationales minimales. Chaque autoclave du Tokyo Medical Center fait l’objet d’une validation microbiologique exhaustive tous les trois mois, utilisant des souches de Geobacillus stearothermophilus certifiées et traçables. Cette fréquence exceptionnelle reflète la culture japonaise de la qualité totale et de l’amélioration continue, mais génère également des coûts opérationnels substantiels qui sont considérés comme un investissement indispensable dans la sécurité des patients.
La documentation électronique systématique mise en place au Tokyo Medical Center atteint un niveau de sophistication remarquable. Chaque cycle de stérilisation génère automatiquement un dossier électronique complet incluant les courbes de température et de pression en temps réel, les photographies numériques de la charge avant et après traitement, l’identification biométrique de l’opérateur et la signature électronique du responsable qualité. Cette traçabilité exhaustive, conservée pendant vingt ans, permet une analyse rétrospective complète en cas de questionnement sur l’efficacité d’un traitement ou d’investigation d’un incident nosocomial.
L’University of Tokyo Hospital, centre de recherche médicale de renommée mondiale, conduit actuellement plusieurs études cliniques prospectives sur l’optimisation des cycles courts pour le matériel endoscopique. Ces recherches, financées par le gouvernement japonais et menées en collaboration avec les principaux fabricants d’autoclaves, visent à développer des protocoles spécifiques pour les endoscopes rigides et souples qui représentent un défi technique majeur en raison de leurs lumières internes de très petit calibre et de leurs matériaux thermosensibles.
Applications aux États-Unis
La Mayo Clinic de Rochester, Minnesota, institution médicale légendaire et référence mondiale en matière d’excellence clinique, a mis en œuvre un programme ambitieux de réduction de l’utilisation des cycles IUSS (Immediate Use Steam Sterilization) qui constitue un modèle international. Ce programme, initié en 2018, a permis de réduire spectaculairement le taux d’utilisation des cycles courts de douze pourcent à trois pourcent en seulement deux années, grâce à une approche systémique combinant optimisation logistique, formation intensive du personnel et amélioration des processus opérationnels.
La formation intégrale de cent pourcent du personnel des blocs opératoires constitue un pilier fondamental de ce programme d’excellence. Chaque chirurgien, infirmière de bloc, aide-soignant et technicien de stérilisation a bénéficié d’une formation théorique et pratique de seize heures couvrant les principes microbiologiques, les limitations techniques, les protocoles d’utilisation et les alternatives organisationnelles aux cycles courts. Cette formation, certifiée par l’American Organization of Nurse Executives, est renouvelée annuellement et fait l’objet d’évaluations pratiques régulières pour garantir la maintenance des compétences.
Johns Hopkins Hospital de Baltimore, Maryland, pionnier historique de la médecine moderne et de la recherche biomédicale, applique rigoureusement les protocoles AAMI ST79 avec une interprétation particulièrement stricte des recommandations nationales. L’établissement réserve exclusivement l’utilisation des cycles flash aux urgences chirurgicales authentiques, définies comme des situations où le délai d’attente d’un cycle standard compromettrait directement la sécurité vitale du patient ou l’issue de l’intervention chirurgicale. Cette politique restrictive, validée par le comité de lutte contre les infections nosocomiales, maintient le taux d’utilisation des cycles courts en dessous de deux pourcent du total des cycles réalisés.
L’audit qualité mensuel mis en place à Johns Hopkins analyse systématiquement chaque utilisation de cycle court pour vérifier la justification clinique, la conformité procédurale et l’efficacité du traitement. Cet audit rétrospectif, conduit par une équipe multidisciplinaire incluant des microbiologistes, des chirurgiens et des spécialistes de stérilisation, génère des recommandations d’amélioration continue et alimente une base de données épidémiologique utilisée pour la recherche et l’enseignement médical.
La Cleveland Clinic de l’Ohio, classée régulièrement parmi les meilleurs hôpitaux américains, a investi massivement dans des autoclaves de nouvelle génération équipés de systèmes de monitoring en temps réel et d’intelligence artificielle prédictive. Ces équipements ultra-modernes, développés en partenariat avec les leaders technologiques du secteur, permettent une surveillance continue des paramètres critiques et une détection précoce des anomalies pouvant compromettre l’efficacité du traitement thermique.
• Charité Berlin : 150 000 cycles/an, 20% cycles courts, ROI +40%
• CHU Lyon : 73 000 cycles/an, 15% cycles courts, conformité EN 285
• Mayo Clinic : Réduction IUSS de 12% à 3% en 2 ans
• Johns Hopkins : <2% cycles courts, audit mensuel systématique
• Tokyo Medical Center : Validation trimestrielle, documentation 20 ans
CHAPITRE 6 : VALIDATION ET CONTRÔLE QUALITÉ

La validation et le contrôle qualité des cycles de stérilisation courts constituent des éléments absolument critiques qui conditionnent l’efficacité antimicrobienne et la sécurité des patients. Ces procédures rigoureuses, encadrées par des normes internationales strictes et des réglementations nationales contraignantes, doivent être impérativement maîtrisées et appliquées par tous les établissements utilisateurs de cette technologie avancée. L’approche scientifique de la validation repose sur une méthodologie éprouvée qui combine indicateurs biologiques, indicateurs chimiques et tests physiques pour garantir une assurance stérile optimale.
Les indicateurs biologiques représentent l’étalon-or de la validation microbiologique des procédés de stérilisation par vapeur d’eau. L’espèce de référence universellement adoptée est Geobacillus stearothermophilus, référencée ATCC 7953 dans la collection américaine de cultures types, anciennement dénommée Bacillus stearothermophilus. Cette bactérie sporulée thermoresistante a été sélectionnée comme standard international en raison de sa résistance thermique exceptionnelle qui dépasse celle de tous les microorganismes pathogènes susceptibles de contaminer les dispositifs médicaux dans les conditions normales d’utilisation hospitalière.
Les spores de Geobacillus stearothermophilus sont préparées selon des protocoles standardisés extrêmement rigoureux qui garantissent une population viable calibrée entre dix puissance cinq et dix puissance six unités formant colonies par indicateur. Cette standardisation permet une reproductibilité parfaite des tests de validation entre différents laboratoires et différents pays, condition indispensable à la comparabilité internationale des résultats et à l’harmonisation des pratiques de stérilisation hospitalière.
La lecture des indicateurs biologiques s’effectue après incubation pendant vingt-quatre à quarante-huit heures dans un milieu de culture spécialement formulé, généralement du bouillon trypcase-soja enrichi en nutriments favorisant la croissance bactérienne. L’observation de toute croissance microbienne, matérialisée par un changement de couleur ou un trouble du milieu de culture, indique un échec du cycle de stérilisation et impose l’interdiction absolue d’utilisation de tous les articles traités dans le cycle concerné, ainsi qu’une investigation approfondie des causes de dysfonctionnement.
La norme ISO 11138-1:2017 « Stérilisation des produits de santé – Indicateurs biologiques » établit les spécifications techniques détaillées pour la production, la standardisation, l’étiquetage et l’utilisation des indicateurs biologiques. Cette norme impose notamment l’utilisation d’indicateurs témoins positifs non traités et d’indicateurs témoins négatifs stérilisés par d’autres moyens pour valider la fiabilité du test et exclure tout faux positif ou faux négatif qui pourrait compromettre l’interprétation des résultats.
Les indicateurs chimiques constituent un complément indispensable aux indicateurs biologiques en fournissant une réponse immédiate sur l’efficacité apparente du cycle de stérilisation. Ces dispositifs colorimériques sophistiqués changent de couleur sous l’effet combiné de la température, de l’humidité et du temps, permettant une évaluation instantanée de l’exposition thermique subie par la charge. La classification internationale des indicateurs chimiques, établie par la norme ISO 11140, distingue six classes selon leurs capacités de réponse et leurs domaines d’application spécifiques.
Les indicateurs chimiques de classe 5, également appelés indicateurs intégrateurs, constituent l’outil de référence pour la surveillance des cycles courts. Ces dispositifs sophistiqués intègrent mathématiquement l’exposition temps-température et répondent à tous les paramètres critiques du cycle de stérilisation. Leur réponse colorimétrique reflète fidèlement l’efficacité thermique du traitement et permet une détection immédiate des anomalies de température, de durée ou de pénétration de vapeur.
Les indicateurs chimiques de classe 6, dits émulateurs de cycle, sont spécifiquement calibrés pour répondre aux paramètres exacts d’un cycle de stérilisation particulier. Pour les cycles courts, ces indicateurs sont programmés pour réagir uniquement lorsque la combinaison température-temps-humidité correspond précisément aux valeurs cibles de cent trente-quatre degrés Celsius pendant trois à quatre minutes en présence de vapeur saturée. Cette spécificité exceptionnelle en fait des outils de surveillance particulièrement adaptés aux cycles courts où les marges de tolérance sont réduites.
Les tests de Bowie & Dick constituent une procédure quotidienne obligatoire pour tous les autoclaves équipés de systèmes de vide préalable, catégorie qui inclut la totalité des équipements modernes capables de réaliser des cycles courts. Ce test, développé dans les années 1960 par les microbiologistes britanniques J. H. Bowie et J. Dick, utilise un pack d’épreuve standardisé constitué de textiles absorbants et d’un indicateur chimique central pour évaluer l’efficacité du vide et la qualité de pénétration de la vapeur dans les charges poreuses.
La fréquence quotidienne obligatoire des tests de Bowie & Dick, imposée par la norme européenne EN 285, reflète l’importance critique de cette vérification pour la sécurité microbiologique des cycles de stérilisation. Tout résultat anormal de ce test, caractérisé par un changement de couleur non homogène ou incomplet de l’indicateur chimique, impose l’arrêt immédiat de l’utilisation de l’autoclave et la conduite d’investigations techniques approfondies pour identifier et corriger la cause du dysfonctionnement.
Les tests d’intégrité technique des autoclaves complètent la surveillance microbiologique par une approche préventive visant à détecter précocement les anomalies de fonctionnement susceptibles de compromettre l’efficacité des cycles futurs. Le leak test, ou test de fuite, vérifie l’étanchéité de la chambre de stérilisation et des circuits de vapeur en mesurant la vitesse de remontée en pression après création d’un vide poussé. Toute fuite excessive compromet l’efficacité du vide fractionné et doit être immédiatement réparée.
Le vacuum test, ou test d’efficacité du vide, évalue les performances de la pompe à vide et la perméabilité des filtres d’évacuation en mesurant le niveau de vide atteint et sa stabilité dans le temps. Ce test, réalisé quotidiennement avant le premier cycle de production, garantit que le système de vide est capable d’éliminer efficacement l’air résiduel, condition indispensable à la pénétration homogène de la vapeur dans toutes les cavités instrumentales.
La documentation électronique exhaustive constitue une exigence réglementaire absolue qui conditionne la traçabilité et l’auditabilité des procédés de stérilisation. Chaque cycle, qu’il soit standard ou court, doit faire l’objet d’un enregistrement informatisé permanent incluant l’ensemble des paramètres physiques mesurés, l’identification complète de l’opérateur et de la charge traitée, ainsi que les résultats de tous les contrôles qualité réalisés. Cette documentation, légalement assimilable à un dossier médical, doit être conservée pendant des durées minimales définies par les réglementations nationales : cinq ans minimum selon la FDA américaine, dix ans selon la réglementation européenne, et jusqu’à vingt ans dans certains pays particulièrement exigeants comme le Japon.
CHAPITRE 7 : AVANTAGES ÉCONOMIQUES ET OPÉRATIONNELS

L’analyse économique des cycles de stérilisation courts révèle des bénéfices financiers substantiels et multidimensionnels qui justifient largement l’investissement technologique et organisationnel nécessaire à leur implémentation. Ces avantages économiques, quantifiables et mesurables, s’articulent autour de gains de temps opérationnels directs, d’économies énergétiques significatives, d’amélioration de la productivité chirurgicale et de réduction des coûts d’exploitation globaux des services hospitaliers. L’évaluation financière rigoureuse de ces bénéfices constitue un élément décisionnel majeur pour les gestionnaires d’établissements de santé confrontés à des contraintes budgétaires croissantes.
Les gains de temps représentent l’avantage le plus immédiatement perceptible et le plus facilement quantifiable des cycles de stérilisation courts. Un cycle complet, incluant les phases de conditionnement, de stérilisation et de séchage, nécessite seulement dix à quinze minutes contre trente-cinq à quarante-cinq minutes pour un cycle standard traditionnel. Cette réduction drastique de vingt-cinq à trente minutes par cycle génère une économie temporelle considérable qui se traduit directement par une augmentation de la capacité de traitement des services de stérilisation centrale.
Pour un hôpital de cinq cents lits réalisant quotidiennement cinquante à quatre-vingts cycles de stérilisation, l’adoption généralisée des cycles courts lorsque les conditions techniques le permettent peut libérer jusqu’à vingt à trente heures de capacité machine par jour. Cette capacité additionnelle permet soit de traiter un volume accru d’instruments sans investissement supplémentaire en équipement, soit de créer une marge de sécurité opérationnelle pour absorber les pics d’activité chirurgicale ou les dysfonctionnements techniques imprévus.
Le calcul du retour sur investissement pour un hôpital type révèle des perspectives financières particulièrement attractives. L’investissement initial pour l’acquisition d’autoclaves compatibles avec les cycles courts et la formation du personnel représente généralement entre deux cent mille et cinq cent mille euros selon la taille de l’établissement et le niveau technologique choisi. Cet investissement est typiquement amorti en trois à cinq années grâce aux économies opérationnelles générées, auxquelles s’ajoutent les revenus additionnels issus de l’augmentation du nombre d’interventions chirurgicales réalisables.
Les économies énergétiques constituent un second pilier des bénéfices économiques des cycles courts, particulièrement significatif dans le contexte actuel d’augmentation des coûts énergétiques et de préoccupations environnementales croissantes. La consommation de vapeur d’un cycle court est réduite de trente à quarante pourcent par rapport à un cycle standard, grâce à la diminution de la durée totale de traitement et à l’optimisation des phases de conditionnement et de séchage. Cette réduction se traduit par des économies substantielles sur la facture énergétique annuelle des établissements hospitaliers.
La consommation d’eau de refroidissement et de production de vapeur est similairement réduite de vingt-cinq à trente-cinq pourcent, contribuant à l’amélioration du bilan environnemental des hôpitaux et à la réduction des coûts d’approvisionnement en eau et de traitement des effluents. Pour un grand hôpital universitaire, ces économies énergétiques et hydriques peuvent représenter plusieurs dizaines de milliers d’euros d’économie annuelle, somme non négligeable dans des budgets hospitaliers de plus en plus contraints.
L’amélioration de la productivité chirurgicale constitue l’impact économique le plus significatif des cycles courts, bien que sa quantification précise nécessite une analyse complexe prenant en compte de multiples variables organisationnelles et cliniques. La réduction des temps d’attente pour la disponibilité d’instruments stérilisés permet une optimisation du planning opératoire et une augmentation potentielle de quinze à vingt pourcent de la capacité chirurgicale des blocs opératoires, sans nécessiter d’investissement supplémentaire en infrastructure ou en personnel.
Cette amélioration de productivité se traduit concrètement par une réduction des retards opératoires, une diminution des annulations de dernière minute liées à des problèmes d’instrumentation, et une amélioration générale de la fluidité des parcours chirurgicaux. L’impact sur la satisfaction des chirurgiens et des équipes soignantes constitue un bénéfice qualitatif additionnel qui, bien que difficilement quantifiable financièrement, contribue significativement à l’amélioration du climat de travail et à la réputation d’excellence de l’établissement.
Les coûts évités représentent une catégorie particulièrement importante de bénéfices économiques qui résultent de l’optimisation organisationnelle permise par les cycles courts. La réduction du stock d’instruments nécessaires constitue un premier élément d’économie substantielle. Grâce à la rotation accélérée permise par les cycles courts, les hôpitaux peuvent réduire de vingt à trente pourcent leur inventaire d’instruments chirurgicaux tout en maintenant le même niveau de service, libérant ainsi des capitaux importants pour d’autres investissements prioritaires.
La diminution des annulations chirurgicales liées à des problèmes d’instrumentation représente une économie particulièrement significative. Chaque annulation génère des coûts directs substantiels incluant les salaires du personnel mobilisé, l’occupation improductive des salles d’opération et les coûts de reprogrammation, ainsi que des coûts indirects liés à la perte de revenus et aux éventuelles pénalités contractuelles avec les organismes payeurs. L’évitement de ces annulations grâce aux cycles courts peut représenter plusieurs centaines de milliers d’euros d’économie annuelle pour un grand établissement hospitalier.
| Paramètre économique | Cycle standard | Cycle court | Gain relatif |
|---|---|---|---|
| Durée totale cycle | 35-45 minutes | 10-15 minutes | -70% |
| Consommation vapeur | 100% (référence) | 60-70% | -30 à -40% |
| Consommation eau | 100% (référence) | 65-75% | -25 à -35% |
| Capacité quotidienne | 40-50 cycles | 60-80 cycles | +15 à +20% |
| Stock instruments requis | 100% (référence) | 70-80% | -20 à -30% |
• Investissement initial : 300 000 € (équipement + formation)
• Économie annuelle énergie/eau : 45 000 €
• Gain productivité chirurgicale : 180 000 € (revenus additionnels)
• Réduction stock instruments : 150 000 € (libération capital)
• Retour sur investissement : 2,4 années
CHAPITRE 8 : LIMITATIONS, PRÉCAUTIONS ET PERSPECTIVES
Bien que les cycles de stérilisation courts offrent des avantages opérationnels et économiques indéniables, leur utilisation s’accompagne de limitations techniques importantes et de précautions d’emploi strictes qui doivent être impérativement comprises et respectées par tous les utilisateurs. Ces contraintes, loin d’être des inconvénients rédhibitoires, constituent des garde-fous essentiels pour garantir la sécurité microbiologique optimale et prévenir tout risque de contamination croisée ou d’infection nosocomiale. La maîtrise parfaite de ces limitations conditionne l’utilisation sécurisée et efficace de cette technologie avancée dans l’environnement hospitalier moderne.
Les limitations techniques fondamentales des cycles courts découlent directement de leur principe de fonctionnement basé sur l’intensification thermique pour compenser la réduction temporelle. Cette approche, bien que scientifiquement validée, réduit mécaniquement les marges de sécurité microbiologique par rapport aux cycles standards traditionnels. La marge de sécurité temporelle, qui constituait historiquement un filet de protection contre les variations de bioburden ou les légères anomalies de fonctionnement, est considérablement réduite dans les cycles courts, imposant une vigilance accrue et une rigueur absolue dans l’application des protocoles.
La sensibilité particulière à la qualité de vapeur représente une contrainte technique majeure qui nécessite une surveillance constante et des contrôles rigoureux. La vapeur utilisée pour les cycles courts doit impérativement présenter des caractéristiques physico-chimiques optimales : degré de surchauffe minimal, absence totale de condensats, pureté chimique parfaite et stabilité thermique absolue. Toute déviation de ces paramètres peut compromettre l’efficacité du traitement thermique, particulièrement critique compte tenu de la durée d’exposition réduite qui ne permet pas de compenser les défauts de qualité vapeur.
Le risque de condensation excessive constitue une problématique technique complexe directement liée à la cinétique rapide des cycles courts. L’injection massive de vapeur surchauffée dans une chambre relativement froide peut provoquer une condensation importante sur les surfaces instrumentales, créant des poches d’eau qui font écran à la pénétration thermique et constituent des zones de protection potentielle pour les microorganismes. Cette problématique nécessite un dimensionnement précis des systèmes de drainage et une optimisation des profils de température pour minimiser les phénomènes de condensation parasite.