LES AUTOCLAVES VERTICAUX : FONCTIONNEMENT, APPLICATIONS ET AVANTAGES
UN GUIDE TECHNIQUE COMPLET SUR LA STÉRILISATION INDUSTRIELLE ET MÉDICALE

Autoclave vertical de laboratoire haute performance avec système de contrôle numérique avancé
1. INTRODUCTION
1.1 Contexte Historique et Définition
Les autoclaves verticaux représentent aujourd’hui l’une des technologies de stérilisation les plus fiables et les plus utilisées dans les secteurs médical, pharmaceutique, alimentaire et de la recherche scientifique. L’histoire de l’autoclave remonte à 1679, lorsque le physicien français Denis Papin inventa le « digesteur à vapeur », précurseur de l’autoclave moderne. Ce n’est qu’en 1879 que Charles Chamberland, collaborateur de Louis Pasteur, développa le premier autoclave à vapeur spécifiquement conçu pour la stérilisation médicale.
Un autoclave vertical est un appareil de stérilisation utilisant de la vapeur d’eau sous pression pour éliminer tous les micro-organismes viables, y compris les bactéries, virus, champignons et spores. La caractéristique distinctive des autoclaves verticaux réside dans leur conception : la chambre de stérilisation est accessible par le haut, permettant un chargement vertical des matériaux à stériliser. Cette configuration offre des avantages significatifs en termes d’encombrement au sol et d’efficacité opérationnelle.
1.2 L’Importance Cruciale de la Stérilisation
Dans notre monde moderne, où les infections nosocomiales coûtent des milliards d’euros aux systèmes de santé et causent des centaines de milliers de décès chaque année, la stérilisation efficace des équipements médicaux n’a jamais été aussi critique. Selon l’Organisation Mondiale de la Santé (OMS), environ 7% des patients hospitalisés dans les pays développés et 10% dans les pays en développement contractent au moins une infection associée aux soins de santé.
Les autoclaves verticaux jouent un rôle essentiel dans la prévention de ces infections en garantissant que les instruments chirurgicaux, les dispositifs médicaux, la verrerie de laboratoire et de nombreux autres articles critiques sont parfaitement stérilisés. La vapeur sous pression reste la méthode de stérilisation la plus efficace, économique et écologique disponible aujourd’hui.
1.3 Position des Autoclaves Verticaux dans l’Industrie
Le marché mondial des autoclaves médicaux et de laboratoire était évalué à environ 3,2 milliards de dollars en 2023 et devrait atteindre 4,8 milliards de dollars d’ici 2030, avec un taux de croissance annuel composé (TCAC) de 5,8%. Les autoclaves verticaux représentent environ 35% de ce marché, particulièrement prisés dans les petits et moyens établissements de santé, les laboratoires de recherche et les installations pharmaceutiques où l’espace est limité.
Les principaux fabricants mondiaux incluent des entreprises européennes comme Tuttnauer (Pays-Bas/Israël), Systec (Allemagne), HMC Europe (Allemagne), RAYPA (Espagne), des fabricants américains comme Consolidated Sterilizer Systems (CSS) et TOMY (présence mondiale avec racines japonaises), et des producteurs japonais comme Hirayama Manufacturing Corporation. Ces entreprises ont établi des standards d’excellence reconnus mondialement.
2. PRINCIPE DE FONCTIONNEMENT TECHNIQUE
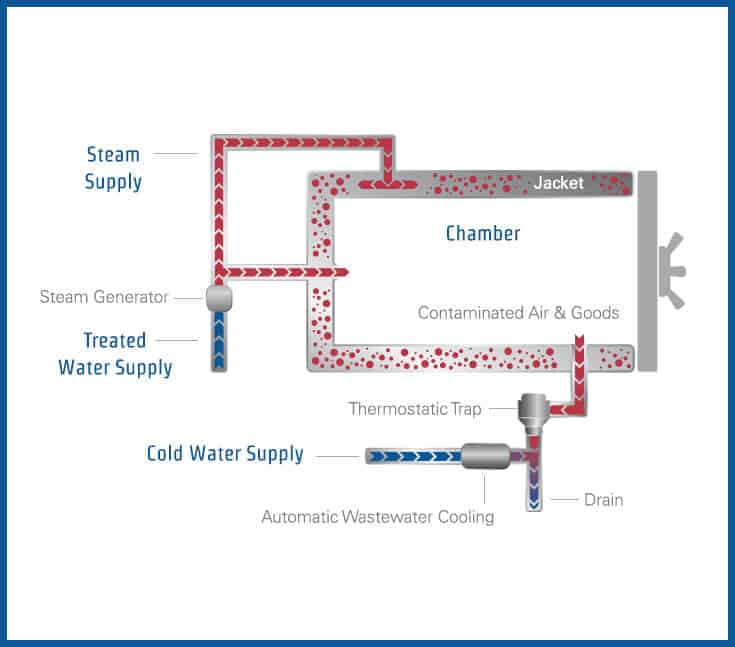
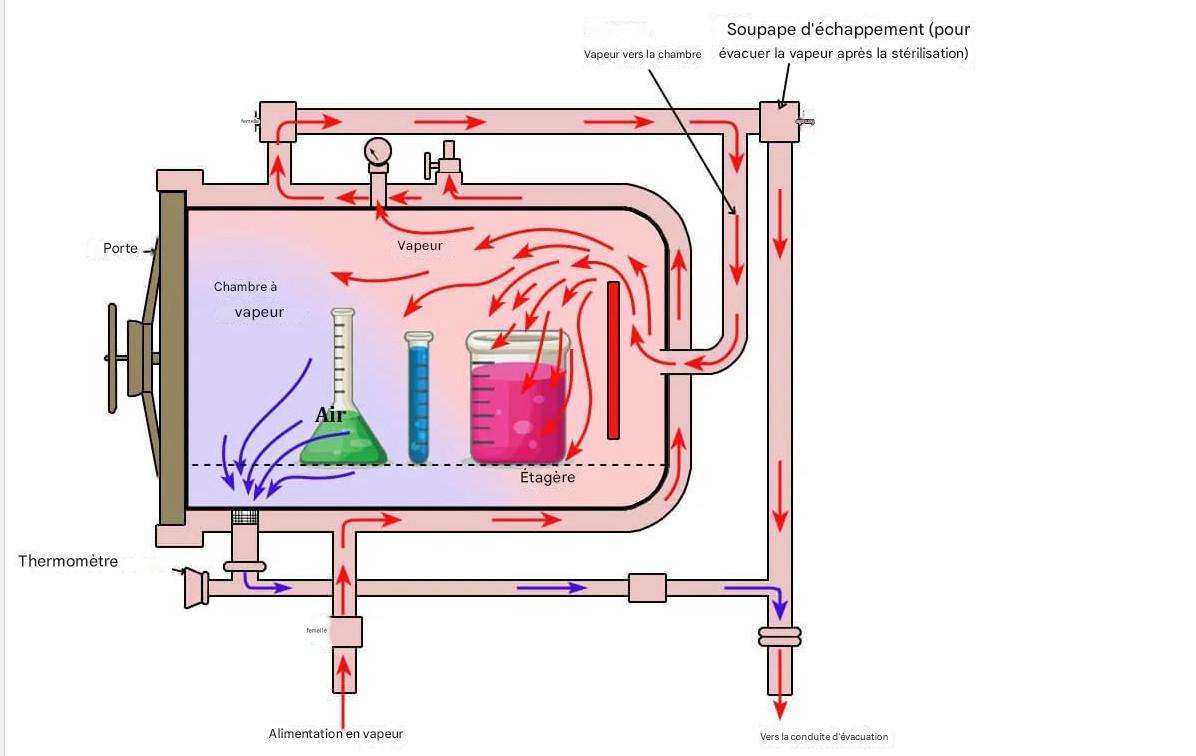
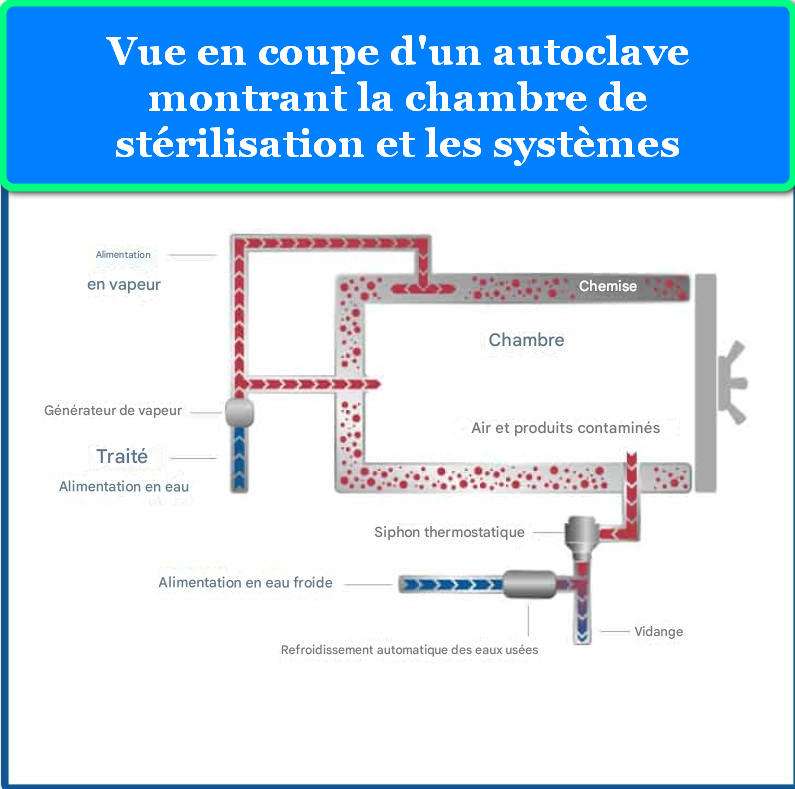
Coupe technique montrant les principaux composants d’un autoclave vertical
2.1 Le Mécanisme de Stérilisation par Vapeur
Le principe fondamental de la stérilisation en autoclave repose sur l’utilisation de vapeur saturée sous pression. La vapeur d’eau possède une capacité calorifique exceptionnellement élevée et peut transférer son énergie thermique très efficacement lorsqu’elle se condense au contact de surfaces plus froides. Ce processus de condensation libère la chaleur latente de vaporisation, environ 2260 kJ/kg à 100°C, permettant une transmission de chaleur bien supérieure à l’air chaud sec.
Lorsque la vapeur pénètre dans la chambre de l’autoclave et entre en contact avec les instruments froids, elle se condense instantanément, transférant son énergie thermique et élevant rapidement la température des objets. Cette combinaison de chaleur humide et de pression crée des conditions létales pour tous les micro-organismes, y compris les spores bactériennes résistantes comme Geobacillus stearothermophilus et Bacillus atrophaeus, utilisées comme indicateurs biologiques standard.
2.2 Paramètres Critiques de Stérilisation
La stérilisation efficace en autoclave dépend de trois paramètres interdépendants qui doivent être soigneusement contrôlés :
Température : Les autoclaves verticaux fonctionnent typiquement à deux températures standard :
- 121°C (250°F) à 1 bar (15 psi) : Cycle standard pour la plupart des matériaux, incluant instruments, textiles, milieux de culture, solutions aqueuses
- 134°C (273°F) à 2 bars (30 psi) : Cycle rapide pour instruments chirurgicaux, particulièrement efficace contre les prions
Des températures intermédiaires (126°C, 128°C) sont également utilisées pour des applications spécifiques. Le choix de la température dépend de la nature des matériaux à stériliser et de la charge microbienne initiale.
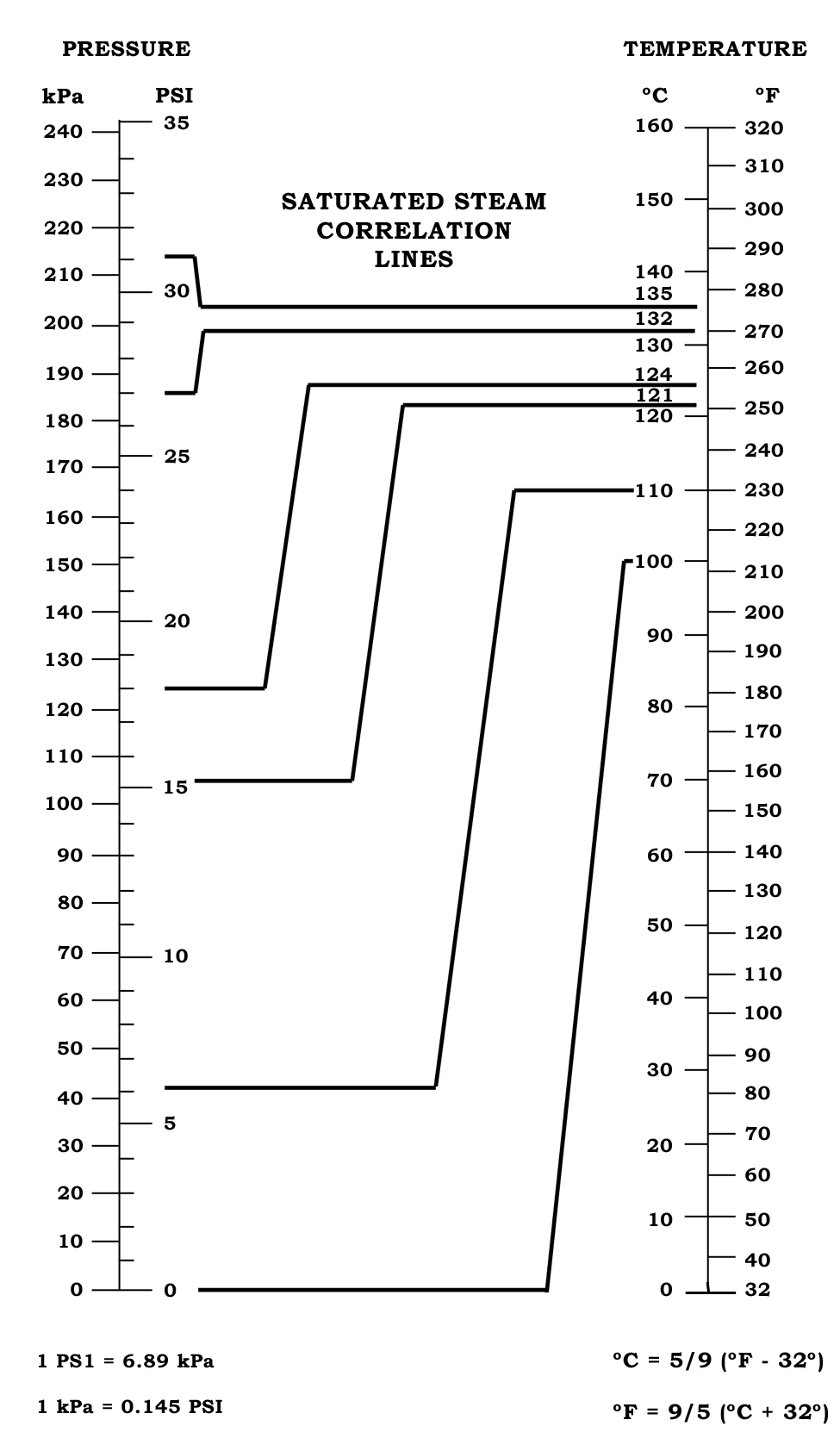
Pression : La pression dans un autoclave vertical varie généralement entre 1 et 3 bars (15-45 psi) au-dessus de la pression atmosphérique. La relation entre température et pression de la vapeur saturée est définie par les tables thermodynamiques. À pression atmosphérique (1 atm), l’eau bout à 100°C, mais sous pression, la température d’ébullition augmente, permettant d’atteindre les températures de stérilisation nécessaires sans évaporation.
Temps d’exposition : La durée du cycle de stérilisation varie selon plusieurs facteurs :
- Type et charge microbienne initiale
- Nature des matériaux (poreux, non-poreux, liquides)
- Configuration de chargement
- Température de stérilisation choisie
Pour un cycle à 121°C, le temps d’exposition typique est de 15-20 minutes pour instruments solides, 20-30 minutes pour matériaux poreux, et jusqu’à 60 minutes pour grandes quantités de liquides.
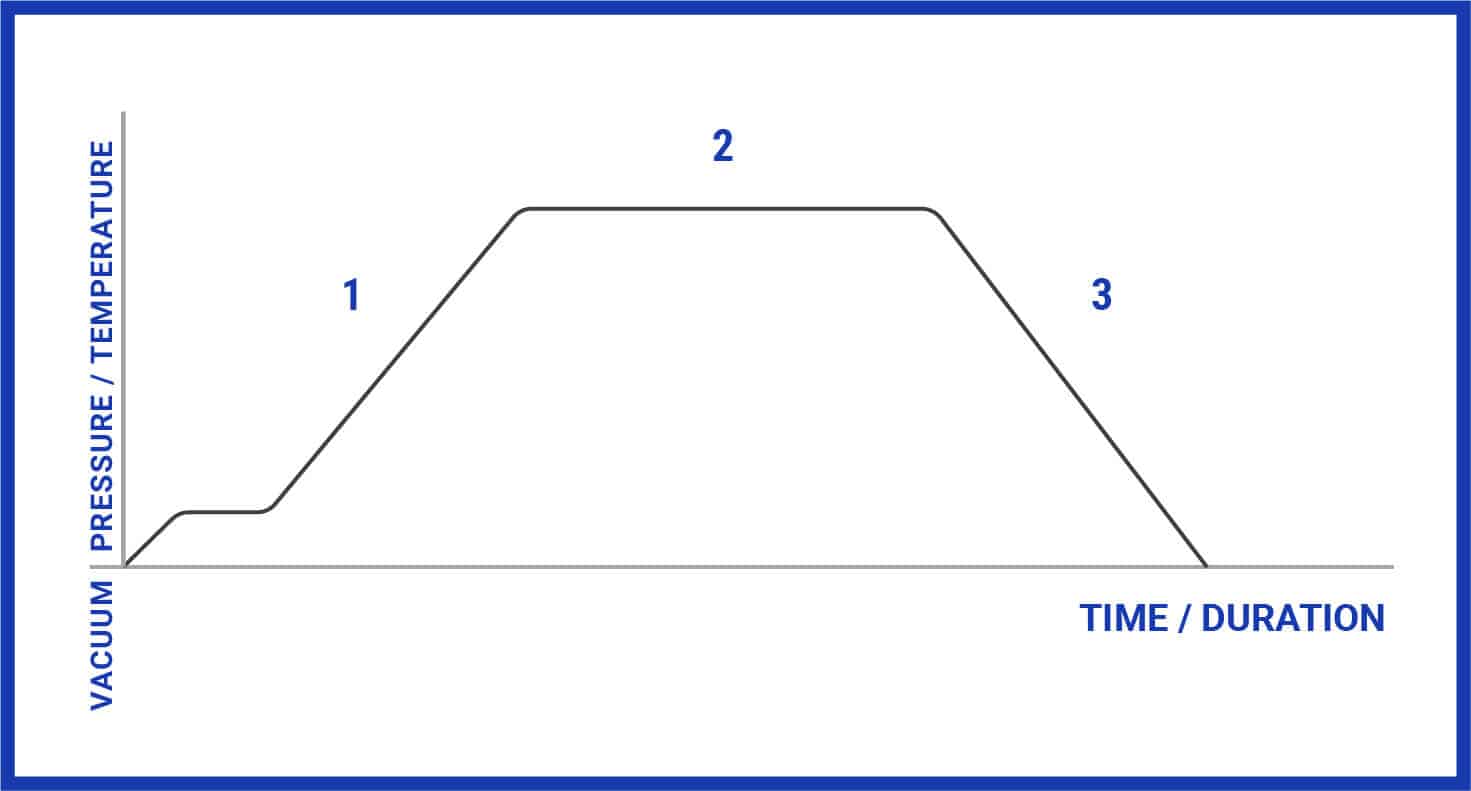
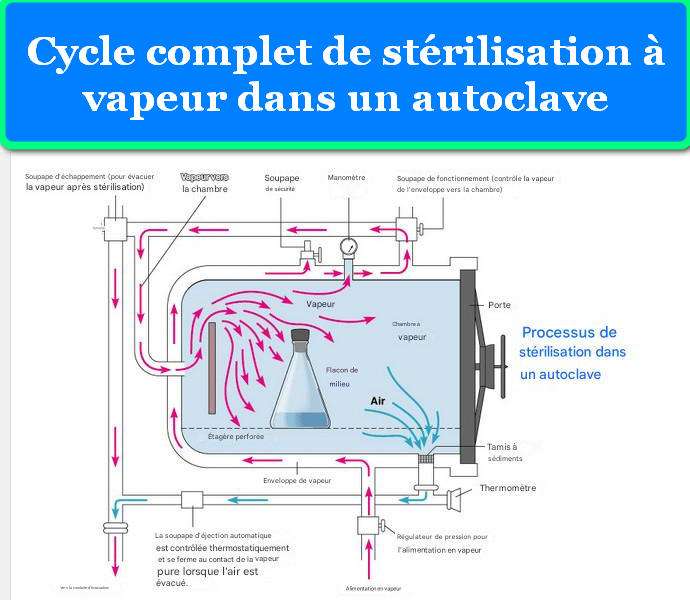
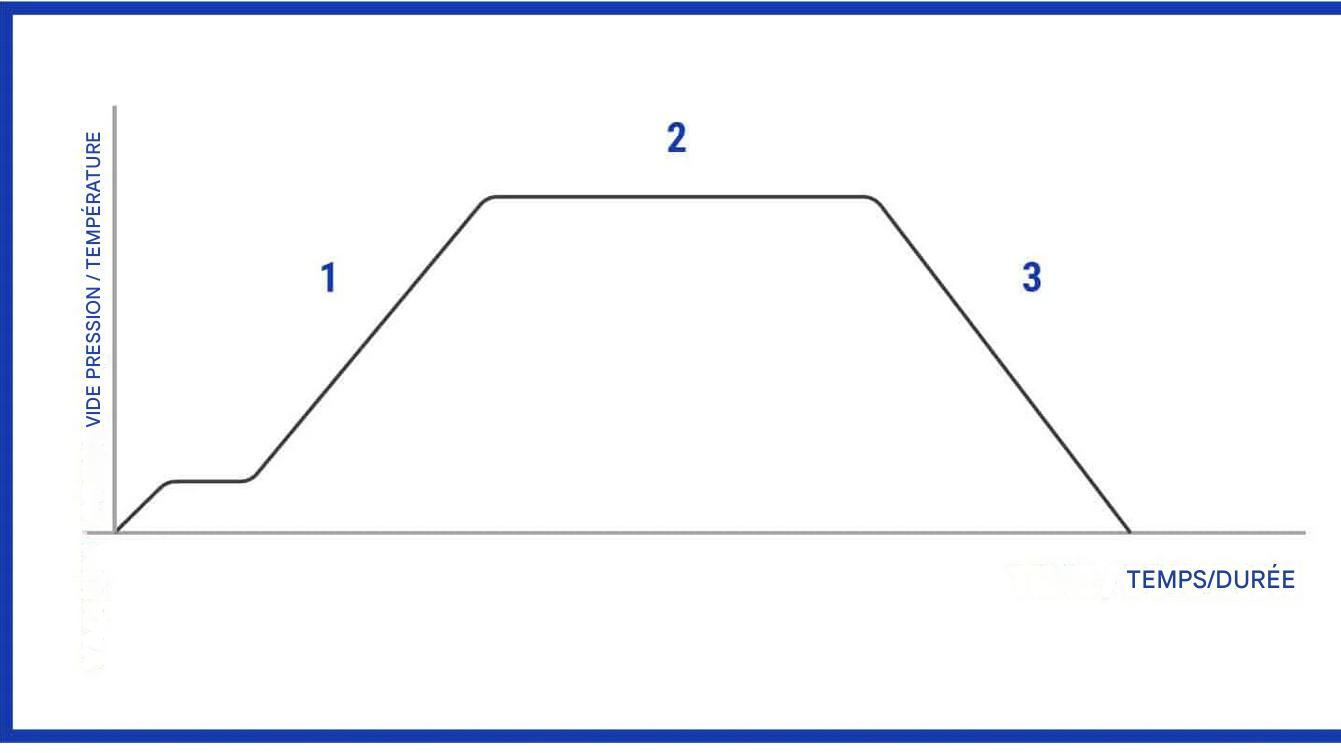
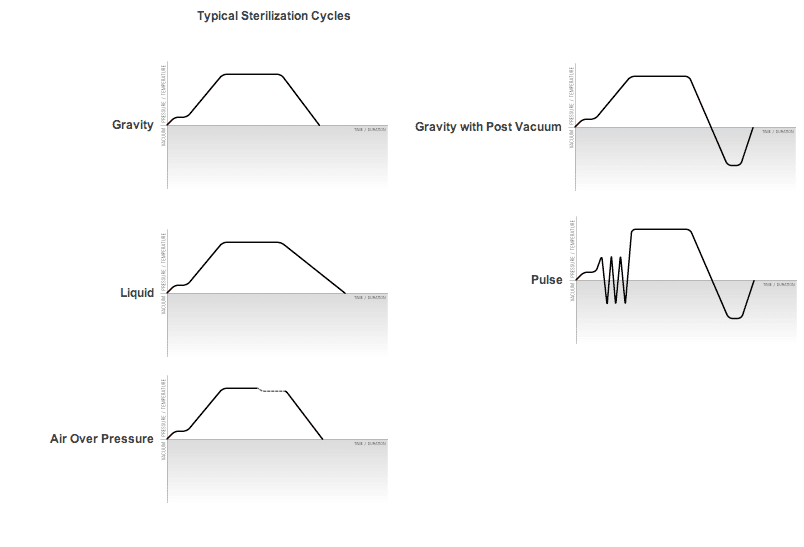
2.3 Les Six Phases du Cycle de Stérilisation
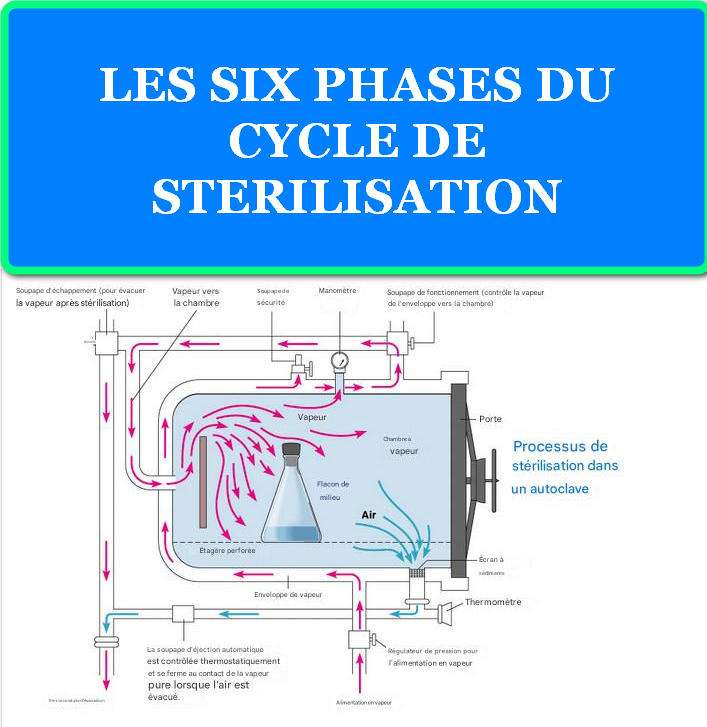
Courbe température-temps montrant les différentes phases d’un cycle de stérilisation
Phase 1 : Préparation et Chargement
Avant tout cycle, l’opérateur doit préparer soigneusement les matériaux à stériliser. Les instruments doivent être nettoyés pour éliminer toute matière organique résiduelle, qui pourrait protéger les micro-organismes. Les articles sont ensuite emballés dans des matériaux perméables à la vapeur mais imperméables aux microbes (papier crépon, non-tissés, conteneurs rigides perforés). Le chargement vertical se fait par le haut de la chambre, avec un espacement adéquat entre les articles pour permettre la circulation de la vapeur.
Phase 2 : Évacuation de l’Air (Déaération)
C’est l’une des phases les plus critiques. L’air présent dans la chambre et entre les articles constitue un excellent isolant thermique et empêche la vapeur d’atteindre toutes les surfaces. Les autoclaves verticaux modernes utilisent plusieurs méthodes de déaération :
-
Déplacement gravitaire : La vapeur, plus légère que l’air, entre par le haut et pousse l’air vers le bas, où il est évacué par une valve inférieure. Cette méthode est simple mais relativement lente (5-10 minutes).
-
Vide prélim inaire : Une pompe à vide extrait l’air de la chambre avant l’admission de vapeur, créant un vide partiel (20-80 mbar). Cette méthode est beaucoup plus rapide et efficace, particulièrement pour les charges poreuses et creuses.
-
Cycles pulsés : Alternance de phases de vide et d’admission de vapeur (3-5 cycles), permettant une élimination quasi-totale de l’air même dans les zones difficiles d’accès.
Phase 3 : Montée en Température et Pression
Une fois l’air évacué, la vapeur continue d’être admise dans la chambre jusqu’à atteindre la température et la pression de consigne. Dans un autoclave vertical typique de 50-100 litres, cette phase dure généralement 5-15 minutes. Les autoclaves modernes utilisent des générateurs de vapeur intégrés à haute efficacité qui produisent de la vapeur propre et sèche à partir d’eau déminéralisée ou distillée.
Le taux de montée en température doit être contrôlé pour éviter les chocs thermiques sur certains matériaux sensibles et pour garantir que toute la charge atteint uniformément la température cible. Les sondes de température multiples (PT100, thermocouples type K) surveillent en permanence la température en différents points de la chambre.
Phase 4 : Phase de Stérilisation (Temps de Contact)
C’est la phase active de destruction microbienne. Une fois la température cible atteinte dans toute la chambre, le temps de stérilisation commence. La vapeur saturée maintient une température constante grâce à un contrôle précis de la pression. Les micro-organismes sont détruits par dénaturation irréversible de leurs protéines et acides nucléiques.
L’efficacité de cette phase est mesurée par le concept de valeur F₀ (unité équivalente à 121°C pendant 1 minute). Pour une stérilisation pharmaceutique, une valeur F₀ minimale de 8 à 15 est généralement requise. Les autoclaves modernes calculent automatiquement la valeur F₀ en intégrant le profil température-temps de tout le cycle.
Phase 5 : Refroidissement et Dépressurisation
À la fin du temps de stérilisation, l’admission de vapeur cesse. Le refroidissement peut être :
-
Passif : La chambre refroidit naturellement par dissipation thermique. Lent mais sûr pour les liquides (évite l’ébullition retardée dangereuse).
-
Actif : Injection d’air filtré stérile ou circulation d’eau de refroidissement dans la double paroi de la chambre. Réduit le temps de cycle de 30-60 minutes.
La dépressurisation doit être progressive, particulièrement pour les liquides, pour éviter une ébullition explosive qui pourrait faire déborder ou exploser les contenants. Un taux de dépressurisation contrôlé de 0,1-0,2 bar/minute est typique.
Phase 6 : Séchage
Pour les charges poreuses et emballées, le séchage est essentiel pour éviter la recontamination par l’humidité. Les autoclaves équipés de pompe à vide appliquent un vide post-stérilisation (2-30 minutes) qui extrait l’humidité par évaporation. L’air filtré stérile est ensuite admis pour ramener la chambre à pression atmosphérique.
Les autoclaves sans vide utilisent un séchage par circulation d’air chaud filtré (30-60 minutes à 80-90°C). Le séchage complet est crucial pour maintenir l’intégrité des emballages et prolonger la durée de conservation stérile des articles.
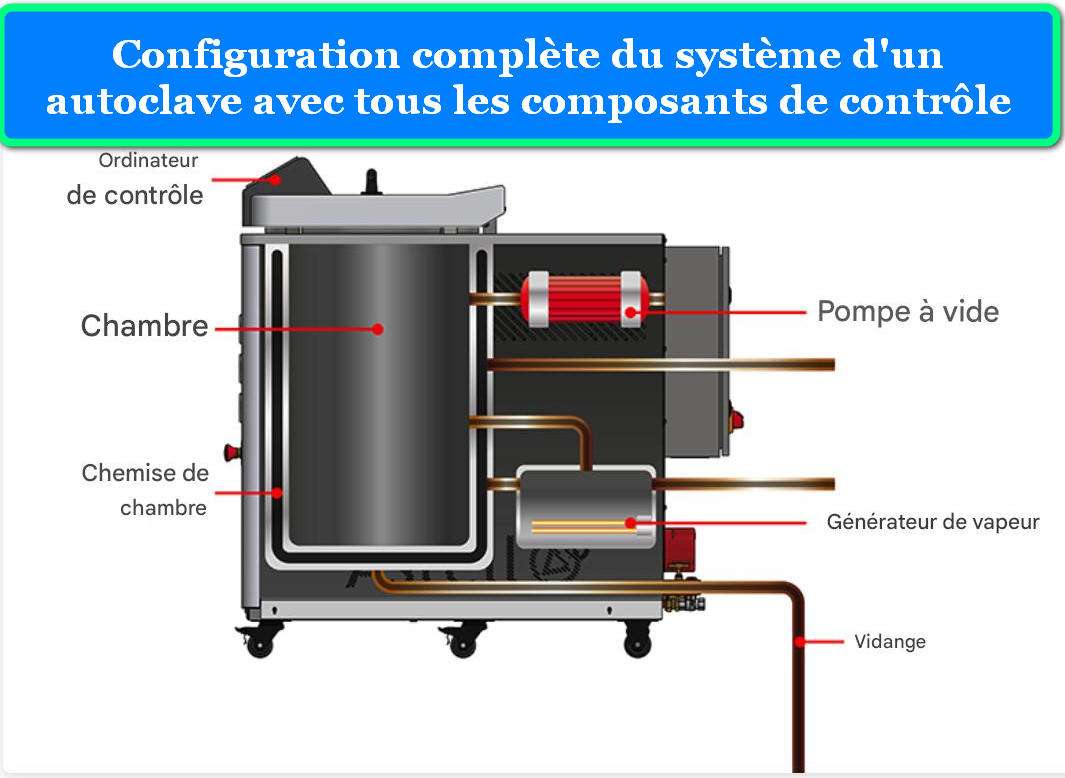
2.4 Composants Techniques Principaux
Chambre de Stérilisation : Typiquement fabriquée en acier inoxydable 316L (EN 1.4404) de 3-6 mm d’épaisseur, résistant à la corrosion et capable de supporter des pressions jusqu’à 4 bars. Les dimensions varient de 18L à plus de 250L pour les modèles verticaux. La chambre cylindrique est conçue selon les codes de pression ASME Section VIII Division 1 (USA) ou EN 13445 (Europe), avec tests de pression hydrostatique à 1,5 fois la pression maximale de travail.
Générateur de Vapeur : Intégré dans la base de l’autoclave vertical, il utilise des éléments chauffants en Incoloy 800 (alliage nickel-fer-chrome résistant à la corrosion et aux hautes températures) de 3-12 kW selon le volume. L’eau est chauffée dans un réservoir séparé ou directement dans la chambre, produisant de la vapeur à 100% de saturation.
Système de Contrôle : Les autoclaves modernes utilisent des automates programmables (PLC) ou des microcontrôleurs avec écrans tactiles couleur. Ils gèrent :
- Séquençage automatique des cycles
- Surveillance multipoints de température et pression
- Calcul de valeur F₀ en temps réel
- Enregistrement et traçabilité des cycles (conformité FDA 21 CFR Part 11)
- Diagnostic et alarmes
- Connexion réseau et impression de rapports
Soupapes et Capteurs de Sécurité :
- Soupape de sécurité tarée : S’ouvre automatiquement si la pression dépasse 1,1-1,15 fois la pression maximale de travail
- Pressostats de sécurité : Double redondance coupant l’alimentation électrique en cas de surpression
- Capteurs de température : PT100 classe A (précision ±0,15°C à 0°C) ou thermocouples type K
- Capteurs de pression : Transmetteurs piézorésistifs (précision ±0,5% pleine échelle)
- Détecteurs de niveau : Électrodes ou sondes capacitives pour surveillance du niveau d’eau
Système de Porte/Couvercle : Les autoclaves verticaux utilisent des couvercles à charnière ou amovibles avec :
- Joint torique en silicone résistant aux hautes températures (FDA, USP Class VI)
- Mécanisme de verrouillage mécanique ou électromécanique empêchant l’ouverture sous pression
- Indicateur visuel de pression résiduelle
3. SPÉCIFICATIONS TECHNIQUES ET NORMES INTERNATIONALES

Autoclave vertical de grande capacité pour applications pharmaceutiques certifié CE et FDA
3.1 Gamme de Capacités et Configurations
Les autoclaves verticaux sont disponibles dans une large gamme de capacités pour répondre aux besoins variés :
Petites capacités (18-50L) :
- Idéaux pour cabinets dentaires, petites cliniques, laboratoires de recherche
- Dimensions typiques : Ø 300-350 mm × H 400-600 mm
- Puissance : 2-4 kW
- Prix : 3 000-8 000 €
- Exemples : Tuttnauer 2340M (23L), HMC HV-25 (25L), TOMY SX-300 (30L)
Capacités moyennes (50-100L) :
- Usage intensif en hôpitaux, laboratoires pharmaceutiques, industries
- Dimensions typiques : Ø 400-450 mm × H 700-900 mm
- Puissance : 6-9 kW
- Prix : 8 000-15 000 €
- Exemples : Systec VX-95 (95L), Hirayama HV-85 (85L), Tuttnauer 3870 ELV (75L)
Grandes capacités (100-250L+) :
- Centrales de stérilisation hospitalières, industries pharmaceutiques
- Dimensions typiques : Ø 500-600 mm × H 1000-1500 mm
- Puissance : 12-18 kW
- Prix : 15 000-35 000 €
- Exemples : HMC HG-160 (160L), Tuttnauer 3870 EAP (140L), Systec VB-160 (160L)
3.2 Matériaux de Construction et Qualité
Chambre : Acier inoxydable 316L (DIN 1.4404 / AISI 316L) avec très faible teneur en carbone (< 0,03%), excellente résistance à la corrosion par piqûres et inter granulaire. Finition électropolie (Ra < 0,8 μm) pour faciliter le nettoyage et éviter les points de corrosion.
Habillage et Isolation : Acier inoxydable 304 (DIN 1.4301) ou acier peint époxy. Isolation thermique en laine minérale (50-100 mm) réduisant les pertes thermiques et protégeant les opérateurs.
Joints et Étanchéité :
- Joints toriques en silicone platine (USP Class VI, FDA 21 CFR 177.2600)
- Résistance thermique : -60°C à +220°C
- Dureté : 60-80 Shore A
- Durée de vie : 1 000-2 000 cycles selon conditions d’utilisation
Tuyauterie et Vannes :
- Tubes en acier inoxydable 316L soudés TIG (qualité alimentaire/pharmaceutique)
- Vannes pneumatiques ou électromagnétiques à membrane PTFE ou EPDM
- Raccords Tri-Clamp pour montage/démontage sanitaire
3.3 Normes Européennes

Autoclave vertical certifié selon les normes EN 285 et EN 13060 pour usage médical
L’Europe possède les normes les plus strictes au monde pour les autoclaves médicaux :
EN 285:2015 – Stérilisation – Stérilisateurs à la vapeur – Grands stérilisateurs
Cette norme s’applique aux autoclaves de chambre ≥ 60 litres et définit :
- Exigences de performance (distribution thermique, pénétration de vapeur)
- Tests de qualification (IQ/OQ/PQ)
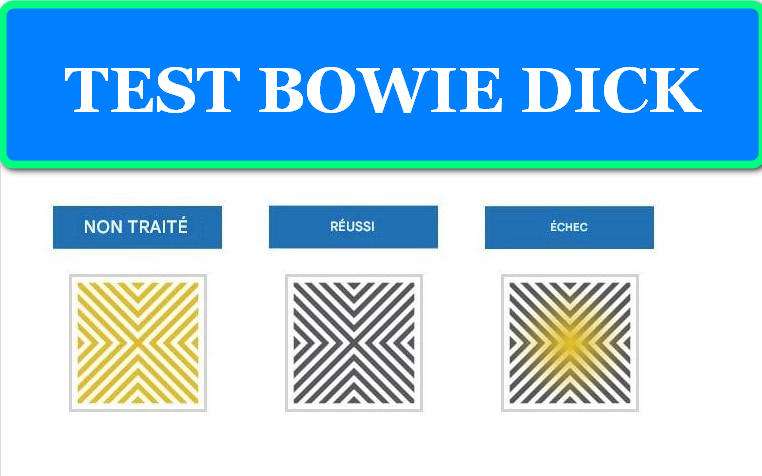
- Contrôles de routine (test Bowie-Dick, test de fuite, indicateurs biologiques)
- Documentation et traçabilité
- Qualité de la vapeur (non-condensables < 3,5%, surchauffe < 15°C, sécheresse > 0,9)
EN 13060:2014 – Petits stérilisateurs à la vapeur
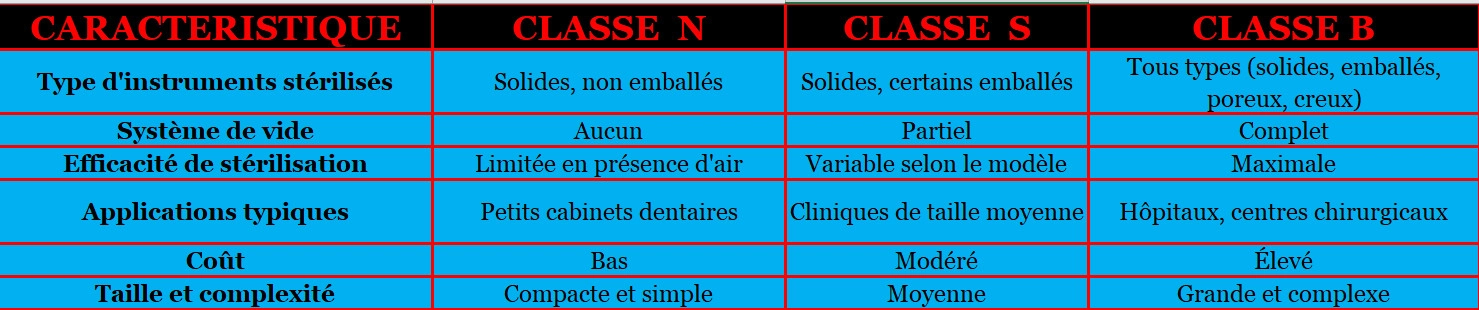
Pour autoclaves < 60 litres, elle définit trois classes de performance :
Classe N (Naked – nu) : Cycles de base par déplacement gravitaire pour instruments solides non emballés. Pas de phase de vide. Utilisation immédiate après stérilisation. Prix : 3 000-6 000 €.
Classe S (Specific – spécifique) : Performances intermédiaires définies par le fabricant. Peut inclure certains cycles avec vide partiel. Stérilisation possible d’instruments emballés et de charges poreuses limitées. Prix : 6 000-12 000 €.
Classe B (Big – grande) : Performances maximales avec vide fractionné (3+ cycles à -80 kPa). Stérilise tous types de charges : instruments emballés/non emballés, solides, poreux, corps creux type A et B. Séchage actif obligatoire. Équivalent aux grands stérilisateurs EN 285. Prix : 12 000-25 000 €.
Directive Machines 2006/42/CE : Sécurité mécanique, électrique, prévention des risques.
Directive Équipements sous Pression (PED) 2014/68/UE : Catégorie I à IV selon pression × volume. Autoclaves > 100L à 3 bars = Catégorie III nécessitant inspection par organisme notifié.
Règlement Dispositifs Médicaux (MDR) 2017/745 : Si l’autoclave est vendu pour usage médical, il doit porter le marquage CE médical avec dossier technique complet et système de gestion de la qualité ISO 13485.
3.4 Normes Américaines
Code ASME Section VIII Division 1 : Standard de référence pour la conception et fabrication des récipients sous pression. Tous les autoclaves vendus aux USA doivent être construits selon ASME et porter le « U-stamp » appliqué après inspection par un inspecteur ASME autorisé (National Board). Cela garantit :
- Calculs de résistance mécanique selon règles ASME
- Matériaux approuvés ASME
- Procédures de soudage qualifiées
- Tests de pression hydrostatique (1,5× MAWP)
- Inspection par tiers indépendant
FDA (Food and Drug Administration) :
- 21 CFR Part 820 (Quality System Regulation) : Bonnes Pratiques de Fabrication pour dispositifs médicaux
- 21 CFR Part 11 : Signatures électroniques et enregistrements électroniques – impose des exigences strictes sur la traçabilité, l’authentification des utilisateurs, les audit trails inaltérables
- FDA 510(k) Premarket Notification : Dossier de pré-commercialisation démontrant l’équivalence substantielle avec dispositifs existants
AAMI (Association for the Advancement of Medical Instrumentation) :
- ANSI/AAMI ST8 : Vapeur d’eau de qualité hospitalière pour stérilisation
- ANSI/AAMI ST55 : Stérilisation à la table, paramètres de cycle et contrôles
- ANSI/AAMI ST79 : Guide complet de stérilisation en établissement de santé
NSF/ANSI 49 : Stérilisateurs de classe II pour cabinets médicaux et dentaires – définit tests de performance et certification par tiers.
3.5 Normes Japonaises
Le Japon possède également des standards très rigoureux :
Labor Standards Bureau Certification : Inspection et certification obligatoire pour tous les récipients sous pression par le Bureau des Normes du Travail du Ministère de la Santé, du Travail et du Bien-être social. Tests périodiques obligatoires (annuels ou bi-annuels selon pression).
JIS (Japanese Industrial Standards) :
- JIS T 7322 : Stérilisateurs à la vapeur petits et moyens – similaire à EN 13060
- JIS T 7324 : Tests de performance des stérilisateurs
- JIS T 1322 : Indicateurs biologiques pour stérilisation vapeur
Pharmaceutical and Medical Device Agency (PMDA) : Équivalent japonais de la FDA, régule les dispositifs médicaux vendus au Japon. Certification PMDA obligatoire pour usage médical.
Les fabricants japonais comme TOMY et Hirayama sont réputés pour la qualité exceptionnelle de leurs autoclaves, souvent dépassant les exigences réglementaires. TOMY, fondé en 1958 à Tokyo, est le leader des autoclaves au Japon et exporte dans plus de 100 pays.
3.6 Norme Internationale ISO
ISO 17665-1:2006 (révisée 2024) : « Stérilisation des produits de santé – Chaleur humide – Partie 1: Exigences pour le développement, la validation et le contrôle de routine d’un procédé de stérilisation pour dispositifs médicaux »
Cette norme harmonisée internationalement définit :
- Approche systématique de développement et validation des procédés
- Concept de SAL (Sterility Assurance Level) – généralement 10⁻⁶ (moins d’une chance sur un million qu’un article soit non stérile)
- Qualification de l’équipement : IQ (Installation Qualification), OQ (Operational Qualification), PQ (Performance Qualification)
- Revalidation périodique
- Gestion des changements
- Documentation et libération des lots
L’ISO 17665 est adoptée en Europe comme EN ISO 17665 et largement reconnue aux USA et au Japon, facilitant le commerce international d’autoclaves et de produits stérilisés.
3.7 Contrôles de Qualité et Validation
Tests de Routine Quotidiens :
- Test de fuite de vide (Bowie-Dick modifié) – détecte les fuites d’air parasites
- Vérification des températures et pressions de consigne
- Inspection visuelle (joints, condensateur, drains)
Tests Hebdomadaires :
- Indicateurs biologiques (spores Geobacillus stearothermophilus) – test ultime de stérilité
- Intégrateurs chimiques classe 5 ou 6 – vérifient température, temps, vapeur
Tests Mensuels/Trimestriels :
- Test de pénétration de vapeur (charge poreuse)
- Cartographie thermique (9+ points de mesure)
- Test de surchauffe de vapeur
- Test de non-condensables
Requalification Annuelle :
- OQ/PQ complets avec 3 cycles consécutifs réussis
- Étalonnage des sondes de température (laboratoire accrédité ISO/IEC 17025)
- Vérification des soupapes de sécurité
- Test de pression hydrostatique (tous les 3-5 ans selon réglementation locale)
4. APPLICATIONS PAR SECTEUR
4.1 Secteur Médical et Hospitalier
 Système de stérilisation vertical automatique pour établissements hospitaliers
Système de stérilisation vertical automatique pour établissements hospitaliers
Les établissements de santé constituent le plus grand marché pour les autoclaves verticaux, représentant environ 45% des ventes mondiales.
Hôpitaux Universitaires Européens
Le CHU Charité de Berlin, l’un des plus grands centres médicaux d’Europe avec 3 000 lits, utilise plus de 150 autoclaves dont 40% sont des modèles verticaux. Leur centrale de stérilisation principale, gérée par un système informatisé de gestion (SGIS), traite quotidiennement :
- 8 000 instruments chirurgicaux
- 1 500 plateaux d’opération
- 2 000 textiles stérilisés (champs, blouses)
- 500 dispositifs médicaux complexes (endoscopes, instruments robotiques)
Le CHU a investi en 2022 dans une flotte d’autoclaves verticaux Tuttnauer ELV série D (85-160L) avec enregistrement électronique conforme FDA 21 CFR Part 11 et connectivité réseau. Chaque cycle est tracé avec un code-barres liant la charge stérilisée au patient, assurant une traçabilité complète en cas de rappel.
L’Hôpital Universitaire de Genève (HUG) en Suisse, centre d’excellence avec 2 000 lits, a modernisé en 2021 sa centrale de stérilisation avec 25 autoclaves verticaux Systec VB série (100-160L). Les avantages rapportés incluent :
- Réduction de 35% de la consommation d’eau grâce au système WaterEco
- Diminution de 28% de la consommation électrique avec récupération de chaleur
- Temps de cycle réduit de 20% (moyenne 45 minutes vs 56 minutes)
- Coûts de maintenance annuels diminués de 15 000 € grâce à la fiabilité accrue
Cliniques et Hôpitaux Américains
La Mayo Clinic (Rochester, Minnesota), classée #1 des hôpitaux américains, opère un réseau de 30 blocs opératoires avec une demande quotidienne massive de stérilisation. Leur département de Processing des Dispositifs Médicaux (MDR) utilise 85 autoclaves dont 35 modèles verticaux TOMY SX-700 (70L) et Consolidated Sterilizer Systems vertical door units (100-150L).
Un projet pilote de 2023 a démontré que les autoclaves verticaux CSS, avec leur technologie exclusive de séchage HeatBoost, réduisaient le temps total de cycle de 38 minutes à 29 minutes pour charges instrumentales standard, permettant un débit 31% supérieur et économisant environ 120 000 $ annuellement en coûts opérationnels.
La Cleveland Clinic (Ohio), avec 6 500 lits sur 11 campus, a standardisé en 2020 sur des autoclaves verticaux Tuttnauer série 3870 (75-150L) pour tous ses services décentralisés (unités de soins, cliniques satellites). Cette standardisation a permis :
- Formation simplifiée du personnel
- Stock de pièces détachées réduit de 60%
- Contrats de maintenance consolidés avec économies de 18%
- Interchangeabilité des cycles entre sites
Centres Médicaux Japonais
Le Tokyo Medical University Hospital, établissement de 1 015 lits au cœur de Tokyo, représente l’excellence de la stérilisation japonaise. Confronté à des contraintes d’espace extrêmes typiques des centres urbains japonais, l’hôpital a investi dans 50 autoclaves verticaux compacts :
- 30 unités TOMY SX-500 (50L) pour services décentralisés
- 15 unités Hirayama HV-110 (110L) pour centrale principale
- 5 unités TOMY SX-700E (70L) avec séchage amélioré pour endoscopie
La culture japonaise de Kaizen (amélioration continue) se reflète dans leur gestion :
- Maintenance préventive stricte toutes les 500 heures
- Enregistrements papier et électroniques redondants
- Tests biologiques bi-hebdomadaires (vs hebdomadaires en Europe/USA)
- Formation annuelle obligatoire de tout le personnel
Les taux d’échec de stérilisation sont remarquablement bas : 0,02% (2 sur 10 000 cycles), soit 5× meilleurs que la moyenne internationale (0,1%).
Applications Spécifiques en Milieu Hospitalier
-
Blocs Opératoires : Stérilisation d’instruments chirurgicaux (pinces, ciseaux, rétracteurs, boîtes d’implants), plateaux spécialisés (orthopédie, neurochirurgie, cardiologie), textiles (champs, blouses, compresses).
-
Services de Soins : Bassins, urinaux, instruments de petite chirurgie, matériel de pansements.
-
Laboratoires Hospitaliers : Milieux de culture, verrerie, pipettes, déchets biologiques contaminés (Catégorie B selon ADR).
-
Pharmacie Hospitalière : Stérilisation de préparations magistrales en petites séries, contenants pour médicaments cytostatiques.
-
Endoscopie : Pré-désinfection d’endoscopes semi-critiques (bien que la désinfection de haut niveau soit plus courante).
4.2 Laboratoires de Recherche
Les laboratoires de recherche représentent 30% du marché mondial des autoclaves verticaux, en raison de leur polyvalence.
Instituts de Recherche Européens
L’Institut Pasteur à Paris, fondé en 1887, demeure un pilier de la recherche biomédicale mondiale. Ses 130 laboratoires répartis sur 3 campus utilisent environ 180 autoclaves verticaux pour des applications diversifiées :
- Microbiologie : Stérilisation de milieux de culture (gélose, bouillons), verrerie (tubes, pipettes, fioles), déchets de culture (catégorie 3 selon classification des agents biologiques)
- Biologie moléculaire : Stérilisation de solutions tampons, tubes PCR vides, déchets génétiquement modifiés (OGM)
- Recherche animale (animalerie A3) : Stérilisation de cages, litières, eau, nourriture pour animaux en conditions axéniques (sans germes)
Les Instituts Max Planck en Allemagne (86 instituts employant 24 000 personnes) ont standardisé en 2019 sur des autoclaves verticaux Systec série VX et VE (50-150L) pour leurs installations P2 et P3 (niveaux de biosécurité 2 et 3). La raison : fiabilité exceptionnelle, conformité stricte aux normes allemandes (BetrSichV, TRBS), et service après-vente rapide avec pièces détachées disponibles sous 24h en Europe.
Un chercheur du Max Planck Institute for Infection Biology à Berlin rapporte : « Nos autoclaves Systec VX-150 fonctionnent 8-12 heures par jour depuis 7 ans avec seulement 3 interventions mineures (remplacement de joints et d’une électrovanne). Le coût total de possession est imbattable. »
Laboratoires de Recherche Américains
Les National Institutes of Health (NIH) à Bethesda, Maryland, constituent le plus grand centre de recherche biomédicale au monde avec un budget de 47 milliards de dollars (2023). Leur campus principal de 120 hectares héberge 1 200 laboratoires utilisant environ 450 autoclaves verticaux, principalement :
- TOMY SX-500 et SX-700 (50-70L) – 60%
- Tuttnauer 3870 ELV (75-110L) – 25%
- Consolidated Sterilizer vertical models – 15%
Les Centers for Disease Control and Prevention (CDC) à Atlanta gèrent des laboratoires BSL-3 et BSL-4 manipulant les pathogènes les plus dangereux (Ebola, Marburg, SARS-CoV-2). Leurs autoclaves verticaux incluent des modèles spécialisés pour décontamination de déchets hautement infectieux avec :
- Doubles portes (pass-through) entre zones contaminées/propres
- Cycles de pré-vide très poussés (> 95% d’extraction d’air)
- Temps de stérilisation étendus (60 minutes à 134°C minimum)
- Validation biologique systématique à chaque cycle
- Système de verrouillage biométrique et traçabilité électronique
Centres de Recherche Japonais
Le RIKEN (Institute of Physical and Chemical Research), le plus grand institut de recherche scientifique du Japon avec 3 000 chercheurs, utilise intensivement des autoclaves verticaux japonais. Leur Centre de Science du Cerveau à Wako utilise 45 autoclaves TOMY et Hirayama pour :
- Préparation de milieux de culture cellulaire neuronale
- Stérilisation d’outils de microchirurgie pour modèles animaux
- Décontamination de déchets transgéniques
Le Centre RIKEN BioResource à Tsukuba, qui maintient la plus grande collection de souris de laboratoire au monde (>10 000 lignées), utilise 120 autoclaves verticaux exclusivement pour :
- Stérilisation de 20 000 cages par semaine
- Stérilisation de 50 tonnes de litière par mois
- Stérilisation de nourriture et eau pour colonies axéniques
Leur protocole rigoureux impose des tests biologiques quotidiens (vs hebdomadaires standard), reflétant les standards qualité japonais exceptionnels.
4.3 Industrie Pharmaceutique
L’industrie pharmaceutique représente environ 20% du marché des autoclaves, avec des exigences réglementaires extrêmement strictes.
Entreprises Pharmaceutiques Européennes
Novartis à Bâle, Suisse, l’une des plus grandes compagnies pharmaceutiques au monde (revenus : 50,6 milliards $ en 2023), utilise des centaines d’autoclaves verticaux dans ses installations de production. Leur site de production de biosimilaires à Kundl, Autriche, utilise 85 autoclaves verticaux Fedegari et Systec (100-250L) certifiés GMP (Good Manufacturing Practice) pour :
- Stérilisation de composants de systèmes fermés (sacs, tubes, connecteurs)
- Stérilisation de petits équipements de remplissage
- Stérilisation de containers pour substances actives pharmaceutiques (API)
- Stérilisation terminale de certains produits injectables thermostables
Tous ces autoclaves sont qualifiés selon l’approche 4Q (DQ/IQ/OQ/PQ) avec revalidation annuelle complète. Les cycles de stérilisation suivent des procédures master validées avec calcul de valeur F₀ et documentation exhaustive exigée par l’Agence Européenne des Médicaments (EMA) et la FDA pour les produits exportés aux USA.
Sanofi en France (siège à Paris, revenus : 43,7 milliards € en 2023) opère des sites de production à Vitry-sur-Seine, Lyon et Sisteron utilisant au total plus de 200 autoclaves verticaux de classe pharmaceutique. Leur site de production de vaccins à Val-de-Reuil utilise des autoclaves verticaux RAYPA et Systec pour stérilisation de :
- Flacons et bouchons avant remplissage aseptique
- Milieux de culture pour tests de stérilité
- Équipements de laboratoire de contrôle qualité
Compagnies Pharmaceutiques Américaines
Pfizer (New York, revenus : 58,5 milliards $ en 2023), fabricant du vaccin COVID-19 Comirnaty, a massivement investi dans des installations de production stérile entre 2020-2023. Leur site de Kalamazoo, Michigan, utilise 150+ autoclaves dont 60 modèles verticaux CSS et Consolidated Sterilizer Systems pour production de petites molécules et produits biologiques.
Un ingénieur de validation Pfizer explique : « Nos autoclaves verticaux CSS avec contrôleur X1 et enregistrement électronique 21 CFR Part 11 ont été qualifiés en 6 semaines, vs 12 semaines pour nos anciens modèles européens. La documentation de validation fournie par CSS était exemplaire, facilitant grandement l’acceptation FDA. »
Johnson & Johnson (New Brunswick, New Jersey) opère 138 sites de production pharmaceutique dans le monde. Leur usine de production de Listerine à Lititz, Pennsylvanie, utilise 25 autoclaves verticaux pour stérilisation de composants de conditionnement et équipements de laboratoire.
Groupes Pharmaceutiques Japonais
Takeda Pharmaceutical (Osaka, revenus : 3 300 milliards ¥ / 30 milliards $ en 2023), la plus grande compagnie pharmaceutique asiatique, maintient des standards de stérilisation parmi les plus stricts au monde. Leur site de production d’Osaka utilise 180 autoclaves dont 70 modèles verticaux TOMY et Hirayama certifiés selon standards PMDA et FDA.
Astellas Pharma (Tokyo) a investi 500 millions ¥ (4,5 millions $) en 2022 pour moderniser la centrale de stérilisation de son site de Tsukuba avec 40 nouveaux autoclaves verticaux TOMY série SX-E équipés de :
- Système de traçabilité RFID des charges
- Intégration ERP pour documentation électronique
- Surveillance IoT en temps réel avec maintenance prédictive
- Validation automatisée des cycles selon GAMP 5
Ces investissements reflètent la priorité absolue accordée à la qualité dans l’industrie pharmaceutique japonaise, où un seul rappel de produit peut causer des milliards de yens de pertes et détruire la réputation d’une entreprise.
4.4 Industrie Alimentaire et Autres Secteurs
Industrie Alimentaire
Les autoclaves verticaux trouvent des applications importantes dans l’industrie alimentaire, représentant environ 5% du marché :
Conserveries : Stérilisation de bocaux de conserves, bien que les autoclaves horizontaux rotatifs soient plus courants pour grande production. Les petites conserveries artisanales (confitures, sauces, produits biologiques) utilisent fréquemment des autoclaves verticaux de 50-100L pour lots de 50-200 pots.
Laboratoires de Contrôle Qualité : L’industrie alimentaire utilise des autoclaves verticaux pour stérilisation de :
- Milieux de culture microbiologique (tests de pathogènes : Salmonella, Listeria, E. coli)
- Verrerie et équipements de laboratoire
- Dilutions et suspensions d’échantillons
Production Biologique : Les entreprises de fermentation (production de probiotiques, enzymes industrielles, levures) utilisent des autoclaves verticaux pour stérilisation de fermenteurs de petite taille (5-50L) et équipements associés.
Autres Secteurs
Cosmétiques : Stérilisation de packaging et équipements de production pour produits stériles (crèmes ophtalmiques, produits de soin pour peaux sensibles).
Tatouage et Perçage Corporel : Petits autoclaves verticaux 18-23L pour stérilisation d’instruments, avec exigences réglementaires variables selon pays (obligatoire dans UE, recommandé aux USA).
Vétérinaire : Cliniques et hôpitaux vétérinaires utilisent autoclaves verticaux 23-75L pour instruments chirurgicaux, textiles, équipements dentaires.
Recherche Agronomique : Stérilisation de terres, substrats de culture, semences, équipements pour cultures in vitro de plantes.
5. AVANTAGES DES AUTOCLAVES VERTICAUX

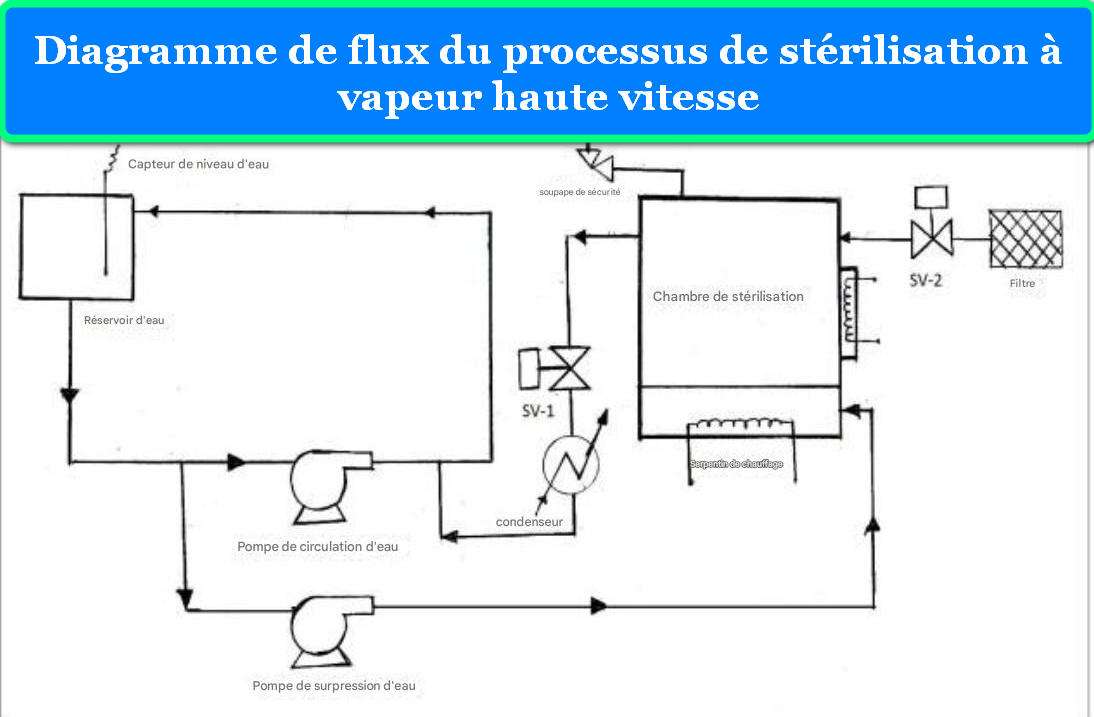
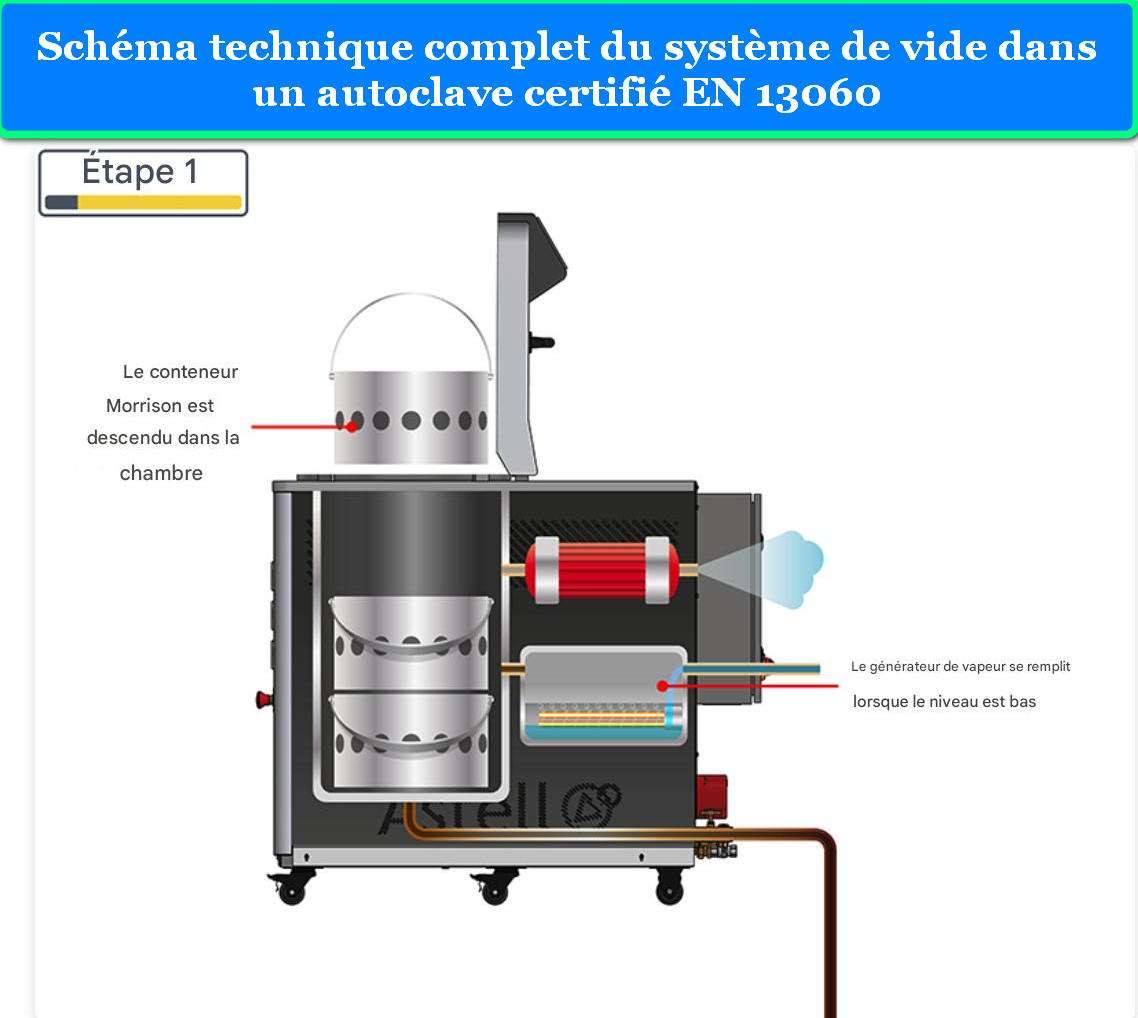
Diagramme technique montrant le système de vide pour élimination efficace de l’air
Les autoclaves verticaux offrent de multiples avantages qui expliquent leur popularité persistante malgré la disponibilité d’alternatives horizontales.
5.1 Gain d’Espace et Empreinte Réduite
Chargement par le Haut – Avantage Majeur
Le principal atout des autoclaves verticaux est leur configuration à chargement vertical qui élimine le besoin d’espace latéral. Un autoclave vertical de 100L occupe typiquement :
- Empreinte au sol : 60 cm × 70 cm = 0,42 m²
- Hauteur : 120-140 cm (accessible pour opérateur standard)
- Espace de dégagement latéral : minimal (15-20 cm pour ventilation)
Comparativement, un autoclave horizontal de capacité équivalente nécessite :
- Empreinte au sol : 80 cm × 150 cm = 1,2 m² (3× plus)
- Profondeur avec porte ouverte : 220 cm
- Espace frontal : 100 cm minimum pour chargement/déchargement
Pour installations avec contraintes d’espace (laboratoires urbains, cliniques dentaires, services hospitaliers décentralisés), l’autoclave vertical est souvent la seule solution viable. Une étude de 2022 menée par Laboratory Equipment International a révélé que 68% des laboratoires citaient « gain d’espace » comme raison principale d’achat d’autoclave vertical.
Installation Flexible
Les autoclaves verticaux peuvent être :
- Posés sur établi ou meuble (modèles < 50L)
- Installés sur pieds réglables (modèles 50-100L)
- Montés sur roulettes pour déplacement (modèles portables)
- Placés en angle ou contre murs sans problème d’accès
5.2 Coût Initial Abordable
Analyse Comparative des Prix (2024)
| Capacité | Autoclave Vertical | Autoclave Horizontal | Différence |
|---|---|---|---|
| 18-30L | 3 000-6 000 € | 8 000-15 000 € | -60% |
| 50-75L | 8 000-12 000 € | 15 000-25 000 € | -50% |
| 100-150L | 15 000-25 000 € | 35 000-60 000 € | -55% |
Les autoclaves verticaux coûtent 50-60% moins cher que les horizontaux de capacité similaire. Cette différence s’explique par :
- Construction plus simple (pas de double porte, mécanisme de verrouillage moins complexe)
- Chambre cylindrique standard (vs chambre rectangulaire plus coûteuse à fabriquer)
- Systèmes de manutention absents (pas de chariots motorisés)
- Génération de vapeur intégrée simplifiée
Pour établissements avec budgets limités (cliniques privées, laboratoires universitaires, PME pharmaceutiques), cet avantage de coût est déterminant. Un audit financier mené en 2023 par le groupe hospitalier AP-HP (Paris) a calculé qu’en remplaçant 50 autoclaves horizontaux de faible utilisation par des verticaux, ils économiseraient 1,2 million € sur l’investissement initial.
5.3 Facilité d’Utilisation et Formation
Interface Utilisateur Intuitive
Les autoclaves verticaux modernes utilisent des interfaces simplifiées :
- Écrans tactiles couleur 7-10 pouces avec icônes graphiques
- Menus en 10-20 langues
- Programmes pré-définis (3-10 cycles standards)
- Assistant de chargement guidant l’utilisateur
- Messages d’erreur explicites avec actions correctives
Chargement Ergonomique
Contrairement aux autoclaves horizontaux nécessitant manipulation de lourds plateaux et chariots, le chargement vertical est direct :
- Ouvrir couvercle (effort < 5 kg avec assistance pneumatique/gaz)
- Placer articles dans paniers empilables
- Fermer et verrouiller couvercle
- Sélectionner cycle et démarrer
Cette simplicité réduit le temps de formation : 2-4 heures vs 8-16 heures pour autoclaves horizontaux complexes. Le personnel administratif ou technique peut être formé rapidement, réduisant la dépendance à personnel spécialisé.
Maintenance de Premier Niveau Simple
Les opérateurs peuvent effectuer eux-mêmes :
- Nettoyage quotidien de la chambre (15 min)
- Remplissage du réservoir d’eau
- Remplacement des filtres à air
- Vidange et détartrage mensuel (30 min)
Cela réduit les coûts de maintenance externe et améliore la disponibilité.
5.4 Efficacité Énergétique
Consommation Électrique Optimisée
Les autoclaves verticaux modernes intègrent des technologies d’économie d’énergie :
Isolation Thermique Renforcée : 80-100 mm de laine minérale ou fibre céramique réduisant pertes thermiques de 40% vs modèles anciens.
Générateurs de Vapeur Haute Efficacité : Éléments chauffants Incoloy à faible inertie thermique chauffant l’eau rapidement (5-8 min vs 12-15 min pour anciens modèles résistifs), réduisant consommation de 25%.
Système de Refroidissement Actif Efficace : Ventilateurs à variation de vitesse (EC motors) consommant 60% moins qu’anciens moteurs AC. Récupération de chaleur optionnelle préchauffant l’eau d’alimentation (économie 15%).
Mode Veille Intelligent : Consommation en veille réduite à 5-15W vs 50-100W pour anciens modèles.
Analyse de Consommation (Autoclave 85L)
Ancien modèle (2010) :
- Consommation par cycle : 6,5 kWh
- Cycles/jour : 4
- Consommation annuelle : 6,5 × 4 × 250 = 6 500 kWh
- Coût (0,15 €/kWh) : 975 €/an
Modèle moderne (2024) :
- Consommation par cycle : 4,2 kWh (-35%)
- Consommation annuelle : 4,2 × 4 × 250 = 4 200 kWh
- Coût : 630 €/an
- Économie : 345 €/an
Sur durée de vie de 12 ans : 4 140 € d’économies, compensant partiellement le coût d’investissement.
Consommation d’Eau Réduite
Les technologies WaterEco et systèmes de récupération de condensats réduisent consommation d’eau de 50-70% :
- Ancien modèle : 15-20 L/cycle
- Modèle moderne avec récupération : 5-8 L/cycle
- Économie annuelle (4 cycles/jour, 250 jours) : 10 000-12 000 L (10-12 m³)
- Économie financière (eau+assainissement à 4 €/m³) : 40-48 €/an
Bien que modeste financièrement, l’impact environnemental est significatif, particulièrement important pour certifications ISO 14001 et labels écologiques.
5.5 Polyvalence des Applications
Les autoclaves verticaux peuvent stériliser une gamme exceptionnellement large de matériaux :
Liquides : Solutions aqueuses, milieux de culture, tampons, eau pour injections (à condition de respecter dépressurisation lente).
Solides : Instruments métalliques, verrerie, céramiques, certains plastiques résistants à la chaleur (PP, PC).
Poreux : Textiles (champs, blouses, compresses), filtres, papiers, caoutchoucs.
Emballés : Articles dans sachets papier/plastique, conteneurs rigides perforés, wraps non-tissés.
Déchets : Déchets biologiques contaminés, cultures microbiennes, tissus animaux.
Cette polyvalence élimine le besoin de multiples types d’équipements de stérilisation, simplifiant opérations et réduisant investissements.
5.6 Fiabilité et Durabilité
Conception Robuste
Construction en acier inoxydable 316L massif (3-6 mm) assurant :
- Résistance à la corrosion exceptionnelle
- Durée de vie opérationnelle : 12-20 ans
- Résistance aux chocs thermiques et mécaniques
Peu de Pièces Mobiles
Comparés aux autoclaves horizontaux avec :
- Systèmes de chariots motorisés
- Doubles portes avec interlocks complexes
- Systèmes hydrauliques de verrouillage
Les autoclaves verticaux ont une mécanique beaucoup plus simple, réduisant pannes et maintenance.
Taux de Disponibilité Élevés
Études de terrain montrent :
- Taux de disponibilité moyen : 98,5% (358 jours/an)
- Temps moyen entre pannes (MTBF) : 2 500-4 000 heures
- Temps moyen de réparation (MTTR) : 2-4 heures
Comparativement, autoclaves horizontaux complexes : disponibilité 95-97%, MTBF 1 500-2 500 h.
5.7 Comparaison avec Autoclaves Horizontaux
| Critère | Autoclave Vertical | Autoclave Horizontal |
|---|---|---|
| Empreinte au sol | 0,3-0,5 m² | 1,0-2,5 m² |
| Coût initial | 3 000-25 000 € | 15 000-100 000 € |
| Capacité typique | 18-250 L | 100-1 500 L |
| Chargement | Manuel, simple | Manuel/automatisé, complexe |
| Formation | 2-4 h | 8-24 h |
| Maintenance | Simple, faible coût | Complexe, coût élevé |
| Idéal pour | Petits volumes, espace limité | Grands volumes, production intensive |
6. MAINTENANCE ET COÛTS D’EXPLOITATION

Système combiné autoclave-laveur pour applications industrielles pharmaceutiques
6.1 Programme de Maintenance Préventive
Maintenance Quotidienne (5-10 minutes)
- Nettoyage de la chambre avec détergent neutre
- Vérification visuelle du joint de porte (fissures, déformations)
- Nettoyage du filtre à peluches du drain
- Vérification niveau d’eau du réservoir
- Essuyage des surfaces externes
Maintenance Hebdomadaire (15-20 minutes)
- Test biologique avec indicateurs de spores
- Vérification des températures et pressions de consigne
- Nettoyage du bac de condensation
- Test de fuite de porte (si autoclave avec vide)
- Examen des messages d’erreur dans le journal d’événements
Maintenance Mensuelle (1 heure)
- Détartrage de la chambre et du générateur de vapeur (si eau dure)
- Nettoyage/remplacement du filtre à air d’admission
- Vérification de la soupape de sécurité (actionnement manuel)
- Lubrification des charnières et mécanismes de verrouillage
- Test de fonctionnement de toutes les alarmes
Maintenance Trimestrielle (2-3 heures, technicien)
- Test de pénétration de vapeur (charge poreuse standard)
- Cartographie thermique avec 9+ thermocouples
- Vérification électrique (connexions, isolement, terre)
- Inspection des joints et rempl acement si nécessaire
- Vérification des vannes et électrovannes
- Test de fonctionnement de la pompe à vide (si équipé)
Maintenance Annuelle (1 journée, technicien agréé)
- Qualification opérationnelle (OQ) complète
- Étalonnage des sondes de température (traçable)
- Étalonnage du transmetteur de pression
- Test de sécurité électrique selon EN 62353
- Inspection mécanique complète (soudures, supports)
- Test de la soupape de sécurité (banc d’étalonnage)
- Mise à jour du logiciel si disponible
- Test de performance complète avec 3 cycles consécutifs
Maintenance Pluriannuelle (3-5 ans)
- Test de pression hydrostatique (selon réglementation locale)
- Remplacement préventif des électrovannes
- Remplacement des éléments chauffants (si signes d’usure)
- Inspection par organisme notifié (équipements PED catégorie III/IV)
6.2 Coûts d’Exploitation Détaillés
Coût d’Investissement Initial
Exemple : Autoclave vertical 85L classe B avec enregistreur électronique
| Composante | Coût |
|---|---|
| Autoclave de base | 12 000 € |
| Options (séchage amélioré, enregistreur) | 2 500 € |
| Installation et qualification IQ/OQ | 1 500 € |
| Formation du personnel (4 personnes) | 800 € |
| Pièces détachées initiales | 500 € |
| TOTAL INVESTISSEMENT | 17 300 € |
Coûts Opérationnels Annuels
Hypothèses : 4 cycles/jour, 250 jours/an (1 000 cycles/an)
Consommables :
- Eau déminéralisée : 8 L/cycle × 1 000 = 8 m³ × 4 €/m³ = 32 €
- Détergent de nettoyage : 50 €
- Indicateurs biologiques (52 tests/an) : 52 × 4 € = 208 €
- Intégrateurs chimiques classe 5 (1 000/an) : 1 000 × 0,30 € = 300 €
- Papier enregistreur (si thermographe) : 60 €
Énergie :
- Électricité : 4,2 kWh/cycle × 1 000 × 0,15 €/kWh = 630 €
- Eau de refroidissement (si circuit ouvert) : 50 m³ × 4 €/m³ = 200 €
Maintenance :
- Contrat maintenance préventive (2 visites/an) : 1 500 €
- Étalonnages annuels : 400 €
- Pièces de rechange (joints, filtres) : 350 €
Main-d’œuvre :
- Temps opérateur (10 min/cycle × 1 000 × 25 €/h / 60) : 4 167 €
- Temps nettoyage/maintenance interne (2 h/semaine × 50 × 25 €/h) : 2 500 €
TOTAL COÛT OPÉRATIONNEL ANNUEL : 10 397 €
Coût par Cycle : 10 397 € / 1 000 = 10,40 €/cycle
6.3 Coût Total de Possession (TCO) sur 12 ans
| Année | Investissement | Maintenance | Opération | Total Annuel | Cumulé |
|---|---|---|---|---|---|
| 0 | 17 300 € | – | – | 17 300 € | 17 300 € |
| 1-5 | – | 2 250 €/an | 8 147 €/an | 10 397 €/an | 69 285 € |
| 6 | – | 3 500 € | 8 147 € | 11 647 € | 80 932 € |
| 7-10 | – | 2 500 €/an | 8 647 €/an | 11 147 €/an | 125 520 € |
| 11 | – | 5 000 € | 8 647 € | 13 647 € | 139 167 € |
| 12 | – | 2 500 € | 8 647 € | 11 147 € | 150 314 € |
TCO 12 ans : 150 314 € soit 12 526 €/an ou 12,53 €/cycle
Note : Années 6 et 11 incluent révisions majeures (remplacement pompe à vide, électrovannes, test hydrostatique).
Comparaison avec Autoclave Horizontal
Autoclave horizontal 100L équivalent :
- Investissement initial : 35 000 € (+102%)
- Coût opérationnel/cycle : 14,50 € (+39%)
- TCO 12 ans : 210 000 € (+40%)
L’autoclave vertical offre un TCO significativement inférieur pour utilisateurs à faible/moyen volume.
6.4 Gestion des Pièces de Rechange
Pièces d’Usure Courantes (stock recommandé)
- Joints de porte en silicone (2-3 pièces)
- Filtres à air d’admission (5 pièces)
- Fusibles et disjoncteurs de rechange
- Électrovannes (1 de chaque type)
- Sondes de température PT100 (1-2 pièces)
Durée de Vie Typique des Composants
- Joint de porte : 1 500-3 000 cycles (1,5-3 ans)
- Élément chauffant : 10 000-15 000 cycles (10-15 ans)
- Pompe à vide : 5 000-8 000 heures (5-8 ans)
- Électrovannes : 500 000-1 000 000 cycles (10-15 ans)
- Sonde PT100 : dérive après 5-7 ans (réétalonnage ou remplacement)
Disponibilité des Pièces
Fabricants réputés (Tuttnauer, Systec, HMC, TOMY) garantissent disponibilité des pièces détachées pendant 10-15 ans après arrêt de production du modèle. Délais typiques :
- Pièces courantes : 24-72 h (Europe), 3-7 jours (international)
- Pièces spécifiques : 5-15 jours
- Pièces obsolètes : possibilité de fabrication sur mesure (3-8 semaines, coûts élevés)
6.5 Durée de Vie et Amortissement
Durée de Vie Opérationnelle
- Usage léger (< 500 cycles/an) : 15-20 ans
- Usage moyen (500-1 500 cycles/an) : 12-15 ans
- Usage intensif (> 1 500 cycles/an) : 10-12 ans
Amortissement Comptable
- France : 5-10 ans selon régime fiscal
- Allemagne : 8 ans selon AfA-Tabelle
- USA : 7 ans selon MACRS (Modified Accelerated Cost Recovery System)
- Japon : 6-8 ans selon méthode de l’amortissement dégressif
La longévité exceptionnelle des autoclaves verticaux de qualité fait que beaucoup d’unités fonctionnent bien au-delà de leur période d’amortissement, générant des années supplémentaires de valeur.
7. ÉTUDES DE CAS INTERNATIONALES
7.1 Cas Européen : CHU de Toulouse, France
Contexte
Le Centre Hospitalier Universitaire de Toulouse, l’un des plus grands hôpitaux universitaires de France avec 3 000 lits et 11 000 employés, faisait face en 2020 à des défis de stérilisation :
- Centrale de stérilisation surchargée avec temps d’attente de 4-8 heures
- Coûts de transport interne élevés (40 000 €/an)
- Insatisfaction des services chirurgicaux
- Autoclaves horizontaux anciens (15-20 ans) avec pannes fréquentes
Solution Implémentée
En 2021, le CHU a lancé un projet de décentralisation partielle avec installation de 18 autoclaves verticaux Systec VE-150 (150L classe B) dans :
- 8 blocs opératoires (2 unités chacun)
- Service d’endoscopie (1 unité)
- Laboratoire central (1 unité)
Investissement : 18 × 22 000 € = 396 000 € incluant formation et qualification
Résultats Mesurés (après 2 ans)
Efficacité Opérationnelle :
- Temps disponibilité instruments : réduit de 6,5 h à 1,5 h (-77%)
- Augmentation capacité stérilisation : +35% (de 12 000 à 16 200 cycles/an)
- Réduction annulations d’interventions pour indisponibilité instruments : -62%
Économies Financières :
- Réduction transports internes : -30 000 €/an
- Réduction achats instruments supplémentaires : -45 000 €/an
- Réduction main-d’œuvre centrale : -2 ETP = -80 000 €/an
- Économie totale annuelle : 155 000 €/an
- Retour sur investissement : 2,6 ans
Qualité et Satisfaction :
- Taux échec stérilisation : réduit de 0,8% à 0,3%
- Satisfaction chirurgiens (enquête) : augmentée de 6,2/10 à 8,7/10
- Aucune infection post-opératoire attribuée à défaut de stérilisation
Environnement :
- Consommation eau : -45% (systèmes WaterEco)
- Consommation électricité : -32% (technologie récente)
- Émissions CO₂ : -15 tonnes/an
Citation du Responsable Stérilisation : « La décentralisation avec autoclaves verticaux Systec a transformé notre organisation. Les blocs sont autonomes pour stérilisation d’urgence, et la centrale peut se concentrer sur instruments complexes. La fiabilité des VE-150 est exceptionnelle : en 2 ans, seulement 3 interventions mineures sur 18 unités. »
7.2 Cas Américain : Genentech, Californie
Contexte
Genentech (membre de Roche Group), pionnier de la biotechnologie basé à South San Francisco, produisant des médicaments biologiques révolutionnaires (Avastin, Herceptin, Rituxan), faisait face à un audit FDA en 2019 identifiant des déficiences dans leur programme de stérilisation :
- Documentation de cycles insuffisante
- Absence de traçabilité électronique
- Qualification IQ/OQ/PQ incomplète pour certains autoclaves
- Non-conformité avec 21 CFR Part 11
Solution Implémentée
Genentech a lancé en 2020 un projet de modernisation de $2,8M incluant :
- Remplacement de 45 autoclaves obsolètes par 45 autoclaves verticaux Consolidated Sterilizer Systems série X1 (75-150L)
- Implémentation système LIMS (Laboratory Information Management System) intégrant données d’autoclaves
- Formation intensive de 120 opérateurs
- Revalidation complète selon GAMP 5
Caractéristiques Clés des CSS X1 :
- Contrôleur X1 avec enregistrement électronique conforme 21 CFR Part 11
- Calcul temps réel F₀ et impression automatique rapports
- Connexion Ethernet pour intégration LIMS
- Interface utilisateur intuitive avec gestion droits utilisateurs
- Audit trail complet inaltérable
- Signature électronique pour libération des cycles
Résultats (après 3 ans)
Conformité Réglementaire :
- Audit FDA 2022 : zéro observation sur stérilisation (vs 7 en 2019)
- 100% cycles tracés électroniquement avec signature
- Temps génération rapport batch record : réduit de 4 h à 15 min
- Conformité 21 CFR Part 11 complète
Efficacité :
- Temps qualification nouvel autoclave : réduit de 12 semaines à 6 semaines
- Documentation validation : 60% réduite (modèles master CSS)
- Productivité opérateurs : +25% (interface simplifiée)
Qualité :
- Taux échec cycle : 0,05% (5 sur 10 000) vs 0,3% précédemment
- Variabilité F₀ entre autoclaves : réduite de 18% à 4%
- Temps investigation déviation : réduit de 8 h à 2 h (données détaillées)
Coûts :
- TCO réduit de 22% vs anciens autoclaves
- Coûts validation/revalidation : -45%
- Coûts investigation/CAPA : -60%
Citation du VP Quality Assurance : « Le projet autoclaves CSS X1 a été un game-changer pour notre conformité FDA. L’intégration LIMS sans couture et la robustesse du système 21 CFR Part 11 nous donnent une confiance totale. C’est un investissement qui s’est payé en moins de 3 ans. »
7.3 Cas Japonais : RIKEN Center for Biosystems Dynamics Research (BDR), Kobe
Contexte
Le RIKEN BDR à Kobe, centre de recherche de pointe en biologie des systèmes avec 500 chercheurs et 100 laboratoires, manipule des organismes génétiquement modifiés (OGM) de biosécurité niveau 2 (P2) nécessitant stérilisation rigoureuse de tous les déchets avant élimination.
En 2018, inspection du Ministry of Education, Culture, Sports, Science and Technology (MEXT) a identifié :
- Système décentralisé inefficace (70 petits autoclaves dispersés)
- Maintenance inadéquate (25% des unités avec calibration expirée)
- Documentation papier volumineuse et sujette à erreurs
- Non-conformité partielle avec Cartagena Act (loi OGM japonaise)
Solution Implémentée
Projet de centralisation-modernisation (2019-2020) avec investissement de 180 millions ¥ ($1,6M) :
- Construction salle de stérilisation dédiée (200 m²) avec zones propres/sales séparées
- Installation de 25 autoclaves verticaux TOMY SX-700 (70L) avec séchage amélioré
- 5 autoclaves de grande capacité TOMY LSX-700 (700L) pour déchets volumineux
- Système de gestion informatisé avec traçabilité RFID des sacs de déchets
Caractéristiques Système TOMY :
- Contrôle numérique avec mémoire 100 programmes
- Capteurs multicouches (3 sondes température par chambre)
- Système dual-fan cooling réduisant temps cycle de 35%
- Enregistreur SD card + impression papier (redondance typiquement japonaise)
- Interface japonaise/anglaise
Résultats (après 4 ans)
Conformité et Sécurité :
- Conformité Cartagena Act : 100% (vs 78% en 2018)
- Inspections MEXT : zéro non-conformité (vs 12 remarques en 2018)
- Incidents de libération accidentelle OGM : 0 (vs 2 incidents mineurs 2016-2018)
- Certification ISO 14001 obtenue en 2021
Efficacité Opérationnelle :
- Capacité traitement déchets : +180% (de 3,5 à 9,8 tonnes/an)
- Temps moyen traitement déchets : réduit de 18 h à 4 h
- Personnel dédié stérilisation : optimisé de 12 ETP à 6 ETP
- Disponibilité systèmes : 99,2% (temps d’arrêt < 7 jours/an)
Qualité :
- Tests biologiques positifs (échec stérilisation) : 0,008% (1 sur 12 000) – record mondial
- Maintenance préventive stricte toutes les 500 h
- Étalonnage semestriel (vs annuel standard) de toutes les sondes
- Formation continue obligatoire annuelle du personnel
Environnement :
- Consommation eau par kg de déchets : -55%
- Consommation électricité : -40% (technologie efficace + récupération chaleur)
- Certification LEED Gold du bâtiment en 2020
Culture Kaizen : Le centre a implémenté un programme d’amélioration continue (Kaizen) avec :
- Réunions mensuelles d’optimisation des processus
- Suggestions personnel récompensées (12 implémentées en 3 ans)
- Benchmarking avec autres centres RIKEN
- Publication interne trimestrielle des performances
Citation du Directeur des Opérations : « Ce projet illustre la philosophie japonaise de monozukuri (fabrication excellente). Les autoclaves TOMY, conçus au Japon avec précision et fiabilité inégalées, combinés à notre culture de discipline et amélioration continue, créent un système de classe mondiale. Notre taux d’échec de 0,008% démontre que la perfection est atteignable. »
8. TENDANCES ET INNOVATIONS
8.1 Automatisation et Contrôle Numérique Avancé
Intelligence Artificielle et Machine Learning
Les autoclaves de nouvelle génération intègrent des algorithmes d’IA pour :
- Optimisation automatique des cycles : L’IA analyse la nature de la charge (via capteurs de poids, composition déclarée) et ajuste automatiquement température, temps, pression pour efficacité maximale tout en garantissant stérilité.
- Détection précoce d’anomalies : Algorithmes de détection d’anomalies identifient déviations subtiles (variations de température, pressions, consommations) indiquant problèmes émergents avant panne complète.
- Optimisation énergétique : L’IA programme cycles selon tarifs électriques variables (heures creuses/pleines), météo (température ambiante affectant refroidissement), prévisions de charge.
Exemple : Tuttnauer T-AI série (lancée 2024) prétend réduire consommation énergétique de 18% supplémentaires via optimisation IA sur 6 mois d’apprentissage.
Contrôle par Tablette et Smartphone
Applications mobiles permettent :
- Surveillance à distance de l’état des autoclaves
- Notifications push pour fins de cycles, alarmes, maintenance due
- Démarrage de cycles à distance (après chargement par personnel)
- Accès historique des cycles et rapports
- Assistance technique en réalité augmentée (technicien voit caméra opérateur et guide réparations)
8.2 Systèmes de Traçabilité Électronique Avancés
Technologie RFID
Étiquettes RFID sur :
- Instruments individuels (implants coûteux, instruments complexes)
- Plateaux et conteneurs
- Emballages de stérilisation
Avantages :
- Traçabilité automatique instrument → cycle → patient
- Prévention d’utilisation d’instruments non stérilisés (portiques RFID bloquant sortie)
- Gestion inventaire en temps réel
- Identification rapide en cas de rappel
Blockchain pour Traçabilité Inaltérable
Certains fabricants (Getinge, Fedegari) explorent blockchain pour enregistrement des cycles de stérilisation, créant registre distribué immuable prouvant conformité et facilitant audits réglementaires.
8.3 Efficacité Énergétique de Nouvelle Génération
Récupération de Chaleur Avancée
Systèmes de récupération de chaleur de prochaine génération :
- Préchauffage eau d’alimentation avec chaleur d’échappement
- Production eau chaude sanitaire pour établissement
- Préchauffage air ventilation de la salle
- Efficacité globale augmentée jusqu’à 40%
Pompes à Chaleur Intégrées
Concept révolutionnaire : utiliser pompe à chaleur pour :
- Refroidissement accéléré post-cycle (évaporateur)
- Récupération chaleur pour cycle suivant (condenseur)
- Réduction consommation de 30-50% selon conditions
Prototypes testés par Systec et HMC Europe, commercialisation prévue 2025-2026.
Autoclaves Solaires
Pour régions ensoleillées et applications mobiles, autoclaves alimentés partiellement par panneaux solaires :
- Panneaux 2-4 kW sur toit ou structure dédiée
- Batteries Li-ion pour stabilisation
- Réduction coûts opérationnels de 40-60%
- Autonomie partielle ou totale (selon ensoleillement)
Projets pilotes en Afrique (Médecins Sans Frontières) et Australie rurale.
8.4 Connectivité IoT et Maintenance Prédictive
Internet des Objets (IoT)
Autoclaves connectés transmettent en temps réel :
- Températures, pressions, états
- Consommations (eau, électricité, vapeur)
- Alarmes et diagnostics
- Performances (valeurs F₀, temps de cycles)
Vers serveurs cloud pour :
- Surveillance centralisée de flotte multi-sites
- Analyse big data de performances
- Benchmarking inter-établissements
- Reporting automatisé
Maintenance Prédictive
Algorithmes analysent données IoT pour prédire pannes :
- Usure de joints (évolution de tests de fuite)
- Dégradation éléments chauffants (temps de montée en température croissant)
- Encrassement (pression vapeur anormale)
- Dérive sondes (écarts entre capteurs redondants)
Système génère automatiquement ordres de maintenance préventive avant panne, réduisant temps d’arrêt imprévus de 70-80%.
Exemple : HMC Europe AutoclaveCare IoT (lancé 2023) prétend réduire pannes imprévues de 75% sur 200 autoclaves surveillés.
8.5 Normes Environnementales Futures
Réglementation Européenne Écoconception
Directive Écoconception 2009/125/CE étendue progressivement aux équipements médicaux. Exigences probables d’ici 2026-2028 :
- Efficacité énergétique minimale (kWh/cycle/litre)
- Consommation eau maximale (L/cycle)
- Taux recyclabilité ≥ 85% en masse
- Élimination substances dangereuses (plomb, cadmium, mercure)
- Affichage obligatoire performance environnementale
Certifications Carbone
Labels émergents :
- Carbon Trust Standard : Mesure et réduction empreinte carbone
- Cradle-to-Cradle : Conception circulaire, matériaux recyclables
- EU Ecolabel : Label écologique européen officiel
Hôpitaux et laboratoires sous pression de leurs parties prenantes privilégieront équipements certifiés.
Autoclaves « Zéro Déchet »
Concept : autoclaves avec taux de recyclabilité 95-100% :
- Acier inoxydable 100% recyclable
- Électronique modulaire démontable
- Plastiques mono-matériau recyclables
- Programme reprise fabricant en fin de vie
Pilotes lancés par Systec (GreenCycle Program) et Tuttnauer (Circular Economy Initiative).
9. CONCLUSION
9.1 Synthèse des Avantages
Les autoclaves verticaux se sont imposés comme une solution de stérilisation incontournable dans de nombreux secteurs grâce à une combinaison unique d’avantages :
Économiques : Coût d’investissement 50-60% inférieur aux autoclaves horizontaux, coûts d’exploitation réduits, maintenance simplifiée, TCO optimisé pour utilisateurs à volume faible/moyen.
Pratiques : Empreinte au sol réduite de 60-70%, installation flexible, chargement simple et ergonomique, formation rapide du personnel.
Techniques : Polyvalence exceptionnelle (liquides, solides, poreux, emballés), fiabilité élevée (disponibilité > 98%), conformité aux normes internationales les plus strictes.
Environnementaux : Efficacité énergétique croissante, consommation d’eau réduite, technologies de récupération de chaleur, empreinte carbone diminuée.
Ces qualités expliquent pourquoi les autoclaves verticaux représentent 35% du marché mondial des autoclaves et pourquoi leur adoption continue de croître, particulièrement dans établissements de petite et moyenne taille.
9.2 Perspectives d’Avenir
L’avenir des autoclaves verticaux s’annonce prometteur avec plusieurs tendances clés :
Digitalisation Totale : D’ici 2030, la quasi-totalité des autoclaves seront connectés IoT avec IA intégrée, maintenance prédictive, et traçabilité blockchain. La gestion de flottes multi-sites sera centralisée avec tableaux de bord temps réel.
Durabilité Renforcée : Pression croissante pour efficacité énergétique, récupération chaleur, consommation eau minimale. Autoclaves neutres carbone ou à énergie positive (avec solaire) deviendront standards dans certaines applications.
Modularité et Évolutivité : Conception modulaire permettant upgrades électroniques sans remplacement mécanique, prolongeant durée de vie à 20-25 ans et réduisant obsolescence.
Miniaturisation et Portabilité : Développement d’autoclaves ultra-compacts pour applications mobiles (médecine d’urgence, missions humanitaires, cliniques mobiles) avec batteries haute capacité et énergies renouvelables.
Personnalisation par IA : Autoclaves apprendront les habitudes d’utilisation spécifiques de chaque établissement et optimiseront automatiquement leurs performances.
Standardisation Internationale : Harmonisation croissante des normes (ISO, EN, ASME, JIS) facilitant commerce international et réduisant coûts de certification.
9.3 Recommandations pour le Choix
Pour choisir l’autoclave vertical optimal, considérer :
1. Volume et Fréquence
- < 500 cycles/an : 18-50L suffisants
- 500-1 500 cycles/an : 50-100L recommandés
-
1 500 cycles/an : 100-150L ou considérer horizontal
2. Type de Charge
- Instruments non emballés simples : Classe N acceptable
- Instruments emballés, poreux légers : Classe S adéquate
- Charges complexes, corps creux, production pharmaceutique : Classe B obligatoire
3. Exigences Réglementaires
- Usage médical EU : EN 13060 ou EN 285 + marquage CE médical
- Production pharmaceutique : cGMP, 21 CFR Part 11, qualification IQ/OQ/PQ
- Recherche : flexibilité cycles, capacité validation
4. Budget
- Budget serré : modèles Classe N/S basiques (3 000-8 000 €)
- Budget moyen : Classe B avec enregistrement (12 000-18 000 €)
- Budget important : Classe B premium avec IoT, IA (20 000-30 000 €)
5. Fabricant
- Privilégier fabricants établis : Tuttnauer, Systec, HMC, TOMY, Hirayama, CSS, RAYPA
- Vérifier disponibilité service après-vente local
- Confirmer disponibilité pièces détachées (10-15 ans minimum)
6. Fonctionnalités
- Essentielles : contrôle température/pression précis, enregistrement cycles, alarmes sécurité
- Importantes : séchage actif, programmes multiples, port USB
- Avancées : IoT, 21 CFR Part 11, intégration LIMS, maintenance prédictive
7. Durabilité
- Évaluer efficacité énergétique (kWh/cycle)
- Vérifier consommation eau et options de récupération
- Considérer coût total possession (TCO) sur 10-12 ans, pas seulement prix initial
En conclusion, les autoclaves verticaux continueront de jouer un rôle central dans la stérilisation pour de nombreuses années. Leur évolution technologique constante, combinée à leurs avantages économiques et pratiques intrinsèques, en fait un investissement judicieux pour tout établissement nécessitant une stérilisation fiable, efficace et conforme aux normes les plus exigeantes.







.webp)


























 Un autoclave de classe B représente le niveau technologique le plus avancé en matière de stérilisation à la vapeur. Cette classification, définie par la norme européenne EN 13060, établit trois catégories d’autoclaves selon leur capacité à traiter différents types de charges et leurs performances de pénétration de vapeur.
Un autoclave de classe B représente le niveau technologique le plus avancé en matière de stérilisation à la vapeur. Cette classification, définie par la norme européenne EN 13060, établit trois catégories d’autoclaves selon leur capacité à traiter différents types de charges et leurs performances de pénétration de vapeur.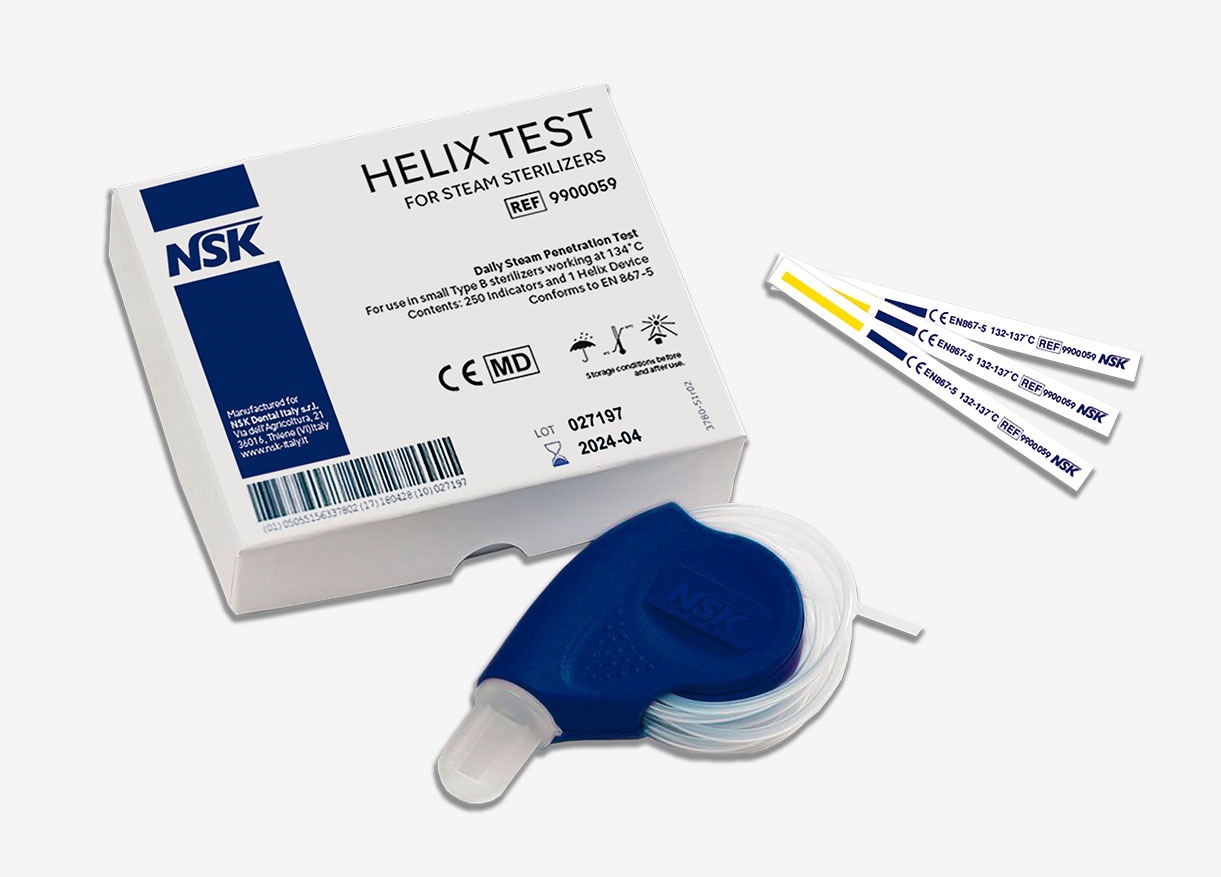 Le test Helix constitue une évolution majeure dans l’évaluation des performances des autoclaves de classe B. Développé pour répondre aux limitations du test Bowie-Dick traditionnel, il offre une approche plus spécifique et représentative des défis rencontrés avec les instruments médicaux modernes.
Le test Helix constitue une évolution majeure dans l’évaluation des performances des autoclaves de classe B. Développé pour répondre aux limitations du test Bowie-Dick traditionnel, il offre une approche plus spécifique et représentative des défis rencontrés avec les instruments médicaux modernes.
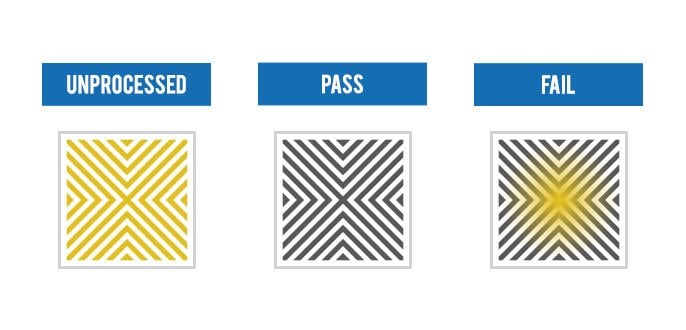
.jpg) L’interprétation correcte des résultats du test Helix constitue un élément critique pour garantir la validité du processus de stérilisation. Cette phase requiert une expertise technique approfondie et une compréhension claire des critères d’acceptation définis par les normes internationales.
L’interprétation correcte des résultats du test Helix constitue un élément critique pour garantir la validité du processus de stérilisation. Cette phase requiert une expertise technique approfondie et une compréhension claire des critères d’acceptation définis par les normes internationales.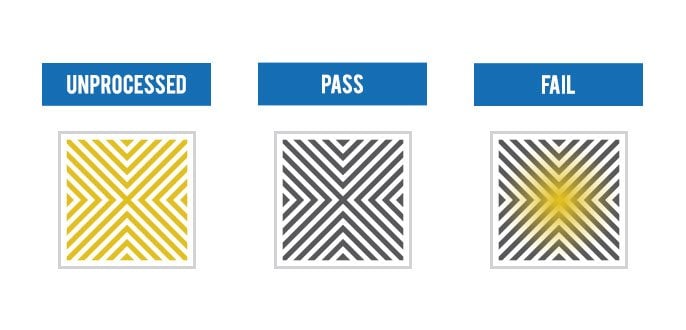 La distinction entre les tests Helix et Bowie-Dick constitue un point crucial pour la compréhension des stratégies de validation des autoclaves. Bien que ces deux tests évaluent la capacité de pénétration de la vapeur, leurs méthodologies et applications diffèrent fondamentalement.
La distinction entre les tests Helix et Bowie-Dick constitue un point crucial pour la compréhension des stratégies de validation des autoclaves. Bien que ces deux tests évaluent la capacité de pénétration de la vapeur, leurs méthodologies et applications diffèrent fondamentalement.
















































































:max_bytes(150000):strip_icc()/102163642_canning-5c901230f5614658b3a569fdf67d1684.jpg)
:max_bytes(150000):strip_icc()/Canning-jar-equipment-GettyImages-89795243-588b753e5f9b5874ee52643d.jpg)



:max_bytes(150000):strip_icc()/GettyImages-1334064660-6ca34a90987f4724819dc32a07680d70.jpg)




:max_bytes(150000):strip_icc()/sea-pressure-canners-winners-afton-cyrus-02-d5b3c920014d45db8b59c5642b22c0a6.jpeg)
:strip_icc()/How-topreserving-canningcanning-basics_sourcefile_updated-aa5acb6e20d24e9e8140d59810c78db8.jpg)