L’AUTOCLAVE DANS L’INDUSTRIE PHARMACEUTIQUE : UN PILIER DE LA STÉRILISATION ET DE LA SÉCURITÉ

INTRODUCTION
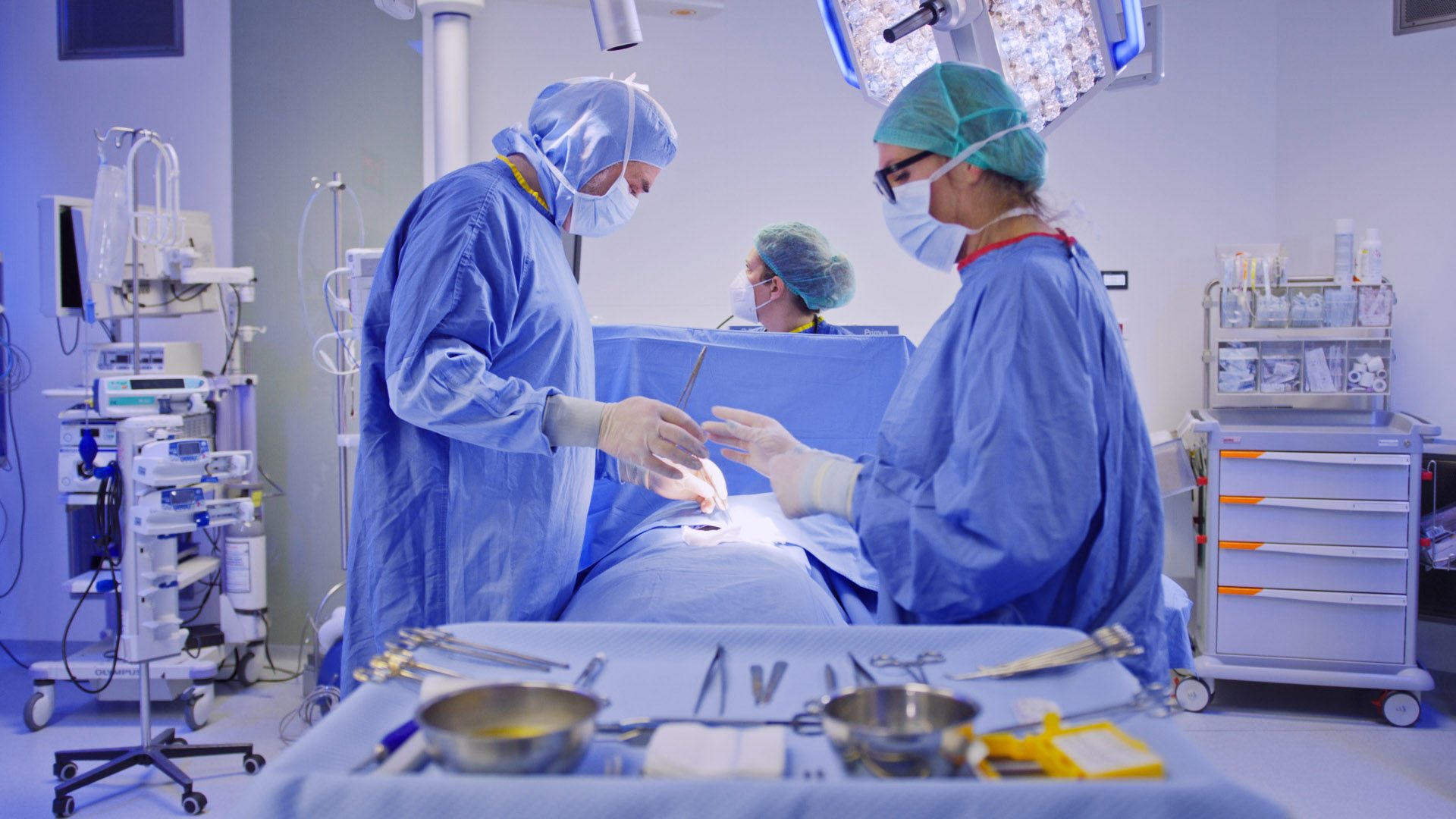
Dans le secteur pharmaceutique mondial, où la moindre contamination microbienne peut avoir des conséquences catastrophiques pour la santé publique, l’autoclave s’impose comme l’équipement le plus critique et le plus réglementé de la chaîne de production stérile. Cette technologie centenaire, constamment perfectionnée, représente aujourd’hui un marché global estimé à 2,32 milliards USD en 2024 et projeté à 3,49 milliards USD d’ici 2032, reflétant son rôle indispensable dans une industrie en expansion continue.
L’autoclave pharmaceutique incarne la convergence entre physique thermodynamique, microbiologie, ingénierie de précision et conformité réglementaire absolue. Contrairement aux autoclaves de laboratoire ou hospitaliers, les autoclaves pharmaceutiques industriels doivent répondre à des exigences extraordinairement strictes définies par un ensemble complexe de normes internationales harmonisées : FDA 21 CFR Part 211 aux États-Unis, EU GMP Annex 1 en Europe, réglementations de la PMDA au Japon, directives WHO pour les marchés émergents, et standards techniques ISO 17665 et EN 285 mondialement reconnus.
Cet article propose une exploration exhaustive de l’autoclave dans l’industrie pharmaceutique, examinant ses fondements techniques, ses applications critiques, les cadres réglementaires internationaux, les protocoles de validation, les défis opérationnels, et les innovations qui façonnent l’avenir de la stérilisation pharmaceutique.
CHAPITRE 1 : FONDEMENTS SCIENTIFIQUES ET TECHNIQUES DE LA STÉRILISATION PAR AUTOCLAVE
1.1 Principes thermodynamiques de la stérilisation par vapeur saturée
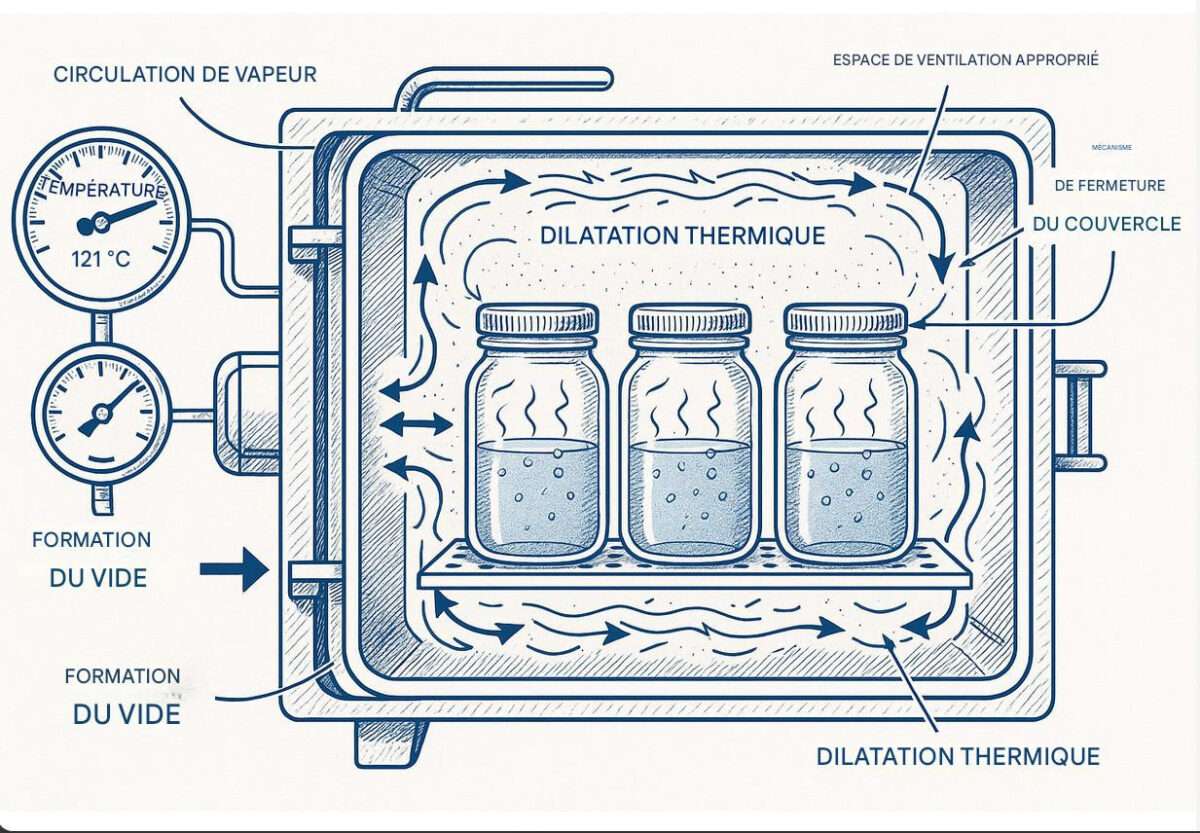
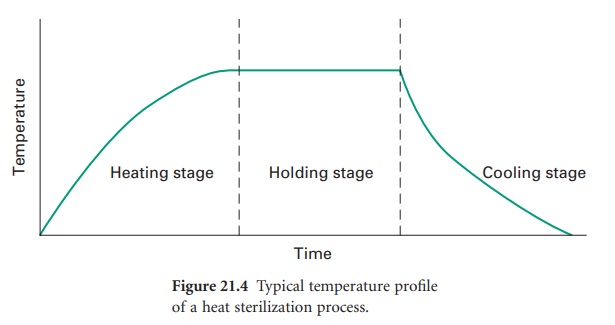
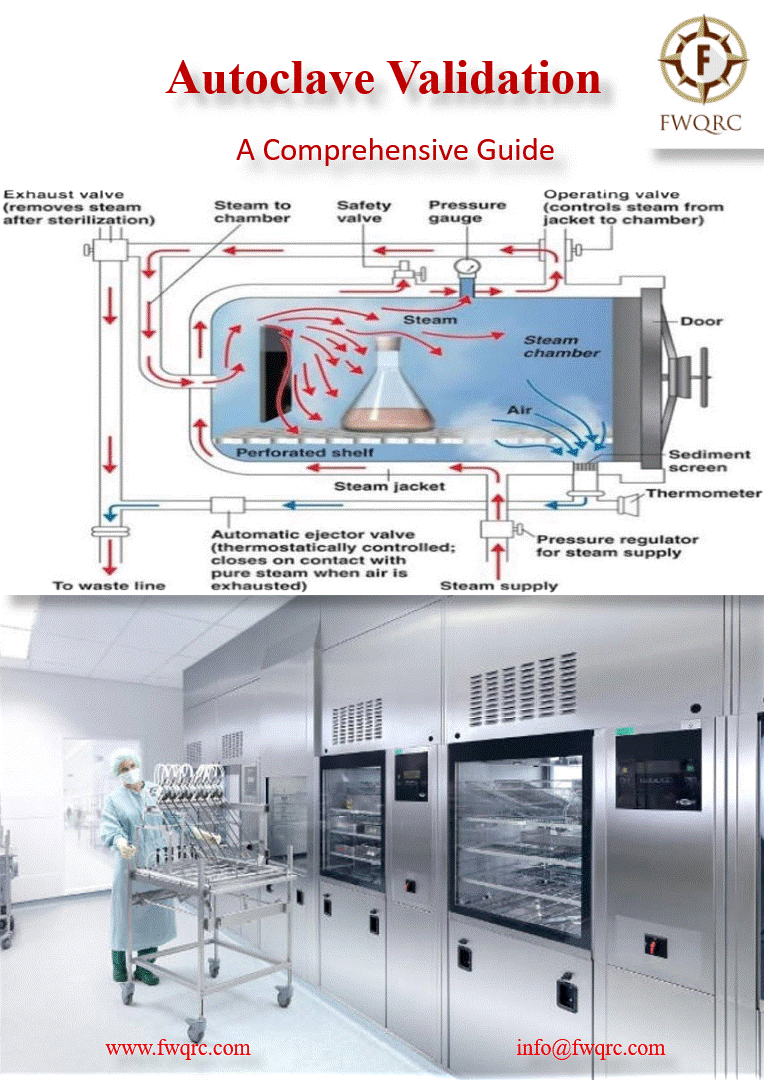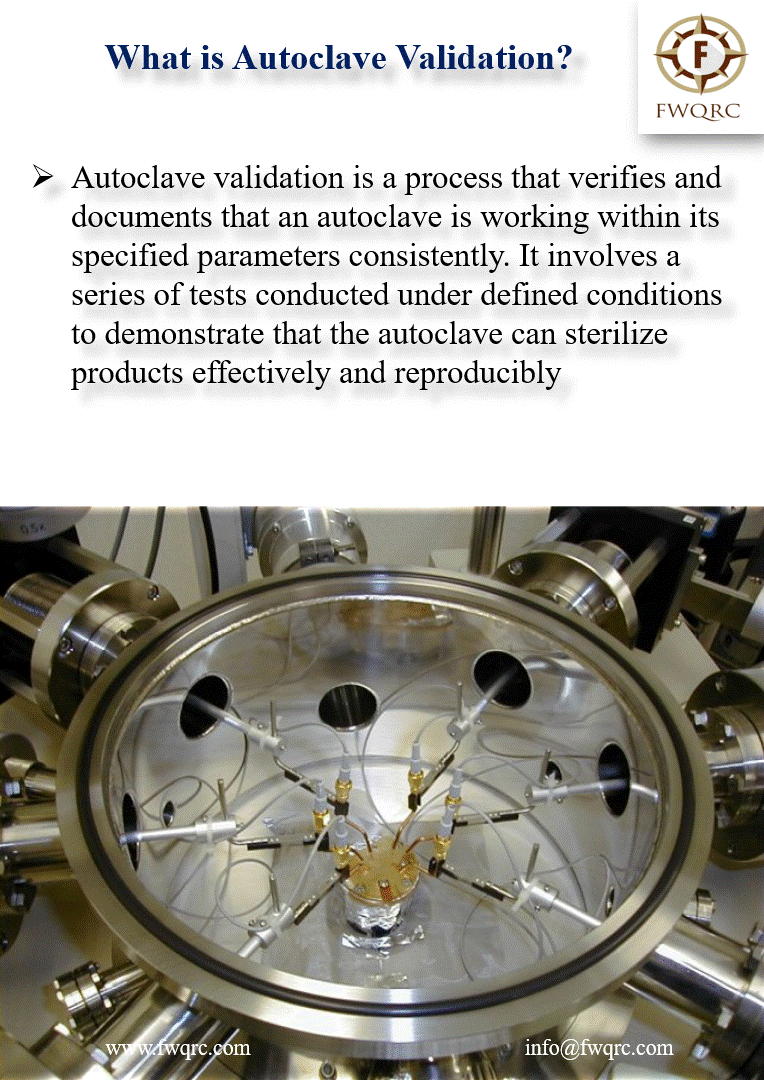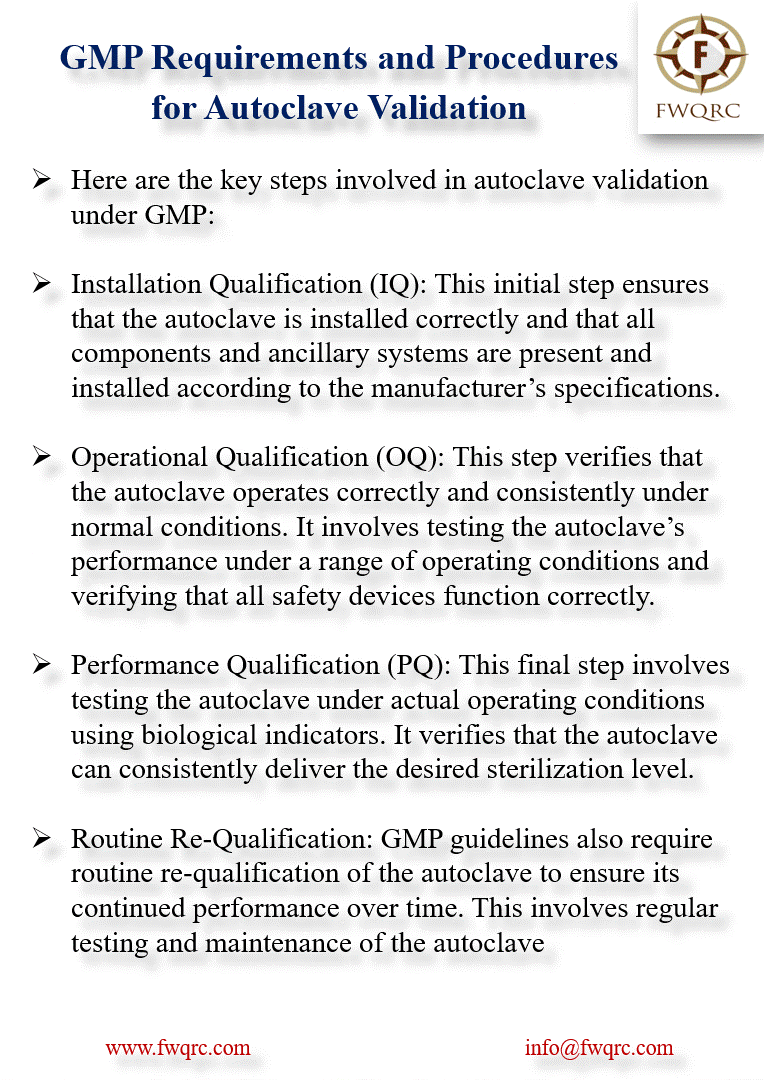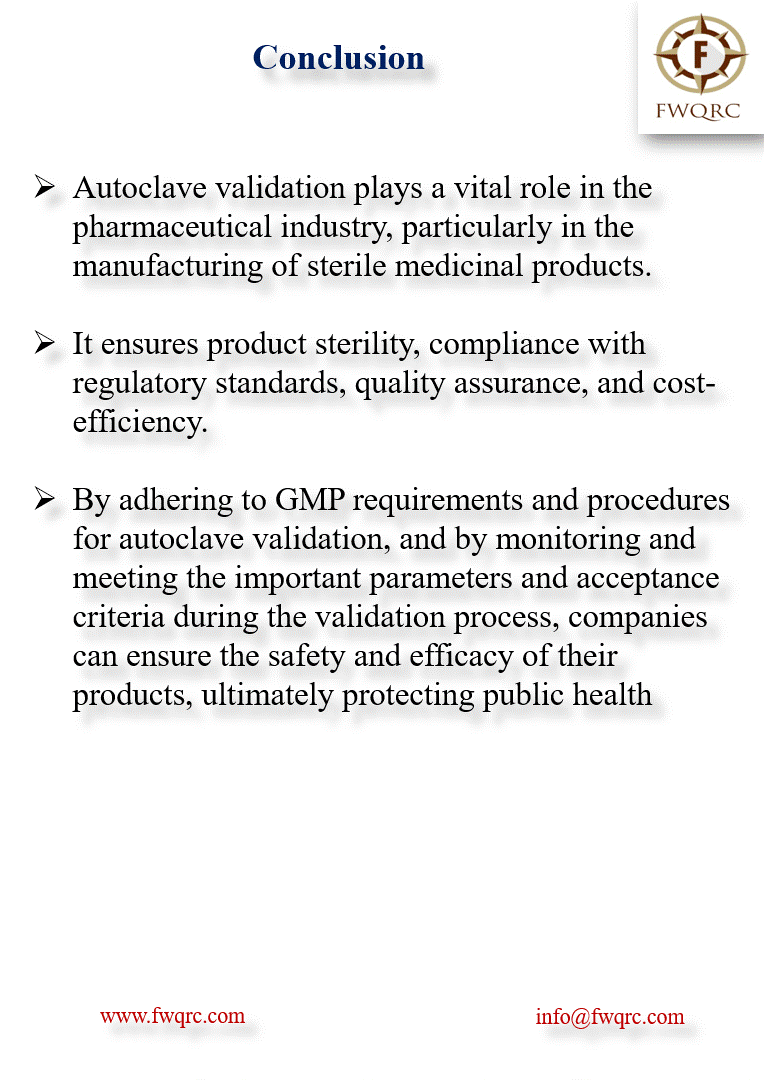
La stérilisation par autoclave repose sur l’action létale de la vapeur d’eau saturée sous pression sur les micro-organismes. Cette méthode exploite trois paramètres physiques interdépendants : température, pression et temps d’exposition. La vapeur saturée possède une capacité thermique supérieure à l’air sec, permettant un transfert d’énergie plus efficace vers les objets à stériliser.
À pression atmosphérique (1013 mbar), l’eau bout à 100°C, température insuffisante pour détruire les spores bactériennes les plus résistantes. En augmentant la pression dans une enceinte fermée, la température d’ébullition s’élève selon la loi de Clausius-Clapeyron. À 2 bars (pression relative de 1 bar au-dessus de la pression atmosphérique), la vapeur atteint 121°C. À 3 bars relatifs, elle atteint 134°C. Ces températures, maintenues pendant des durées définies, assurent la destruction de tous les micro-organismes pathogènes, incluant les spores de Geobacillus stearothermophilus, organisme indicateur biologique le plus résistant à la chaleur humide.
Le mécanisme de destruction microbienne résulte de la dénaturation irréversible des protéines cellulaires et de l’hydrolyse des acides nucléiques. La vapeur saturée pénètre les structures cellulaires, provoque la coagulation du cytoplasme et désorganise les membranes cellulaires. La présence d’eau sous forme vapeur catalyse ces réactions de dégradation, expliquant la supériorité de la chaleur humide sur la chaleur sèche.
1.2 Paramètres critiques et leur interdépendance
Le concept de Sterility Assurance Level (SAL), pierre angulaire de la stérilisation pharmaceutique, quantifie la probabilité qu’une unité stérilisée contienne encore un micro-organisme viable. La FDA et l’EMA exigent un SAL de 10⁻⁶, signifiant une probabilité inférieure à une sur un million qu’un produit reste contaminé après stérilisation.
L’atteinte de ce SAL nécessite une combinaison précise temps-température. Les cycles standards incluent : 121°C pendant 15 minutes (cycle minimal pour instruments), 121°C pendant 20-30 minutes (solutions aqueuses), 134°C pendant 3-4 minutes (instruments poreux), et 134°C pendant 18 minutes (charge textile complexe). Ces paramètres sont calculés en utilisant la valeur F₀, temps équivalent à 121°C nécessaire pour réduire la population microbienne d’un facteur 10¹² (12 log de réduction).
La pression, bien que paramètre contrôlé, n’exerce pas d’effet stérilisant direct. Son rôle consiste exclusivement à élever la température de la vapeur au-dessus de 100°C. Toutefois, la corrélation température-pression constitue un contrôle critique : toute déviation entre la température mesurée et la pression observée signale une contamination de la vapeur par de l’air résiduel ou des gaz non-condensables, compromettant l’efficacité de la stérilisation.
1.3 Qualité de la vapeur : le facteur souvent négligé
La norme EN 285 définit trois critères essentiels pour la vapeur de stérilisation : dryness (fraction sèche), superheat (surchauffe), et non-condensable gases (gaz non-condensables). Ces propriétés déterminent l’efficacité du transfert thermique et la pénétration de la vapeur dans les charges poreuses.
La fraction sèche doit être supérieure à 95%, signifiant que la vapeur ne contient pas plus de 5% de gouttelettes d’eau liquide en suspension. Une vapeur trop humide (wet steam) ralentit le réchauffement des charges, crée des poches d’air emprisonnées, et provoque une condensation excessive pouvant endommager les produits. À l’inverse, une vapeur surchauffée (superheat >25°C) se comporte comme un gaz sec, perdant sa capacité de condensation immédiate et donc son efficacité thermique.
Les gaz non-condensables (principalement air, dioxyde de carbone) constituent le contaminant le plus problématique. Même en faible concentration (>3,5% en volume selon EN 285), ils créent des barrières thermiques isolantes, empêchant la vapeur d’atteindre toutes les surfaces. Les autoclaves pharmaceutiques intègrent donc des systèmes sophistiqués d’évacuation de l’air : pompes à vide pulsée dans les autoclaves à pré-vide, ou gravité assistée dans les autoclaves gravitaires.
La qualité de l’eau alimentant le générateur de vapeur influence directement ces paramètres. L’industrie pharmaceutique utilise exclusivement de l’eau purifiée (PW) ou, pour les applications les plus critiques, de l’eau pour préparations injectables (WFI), conformément aux monographies USP <1231> et Ph. Eur. 0008. Ces eaux, déminéralisées et exemptes d’endotoxines, préviennent l’accumulation de dépôts minéraux dans les chambres de stérilisation et éliminent le risque de contamination pyrогénique des produits stériles.
1.4 Cinétique de la mort microbienne
La destruction thermique des micro-organismes suit une cinétique de premier ordre, modélisée par l’équation logarithmique de réduction décimale. La valeur D (Decimal Reduction Time) représente le temps nécessaire à une température donnée pour réduire une population microbienne de 90% (1 log). Pour Geobacillus stearothermophilus, organisme indicateur biologique standard, la valeur D₁₂₁°C est d’environ 1,5 minutes.
La valeur z (Temperature Coefficient) quantifie la sensibilité d’un organisme aux variations de température. Pour G. stearothermophilus, z = 10°C, signifiant qu’une augmentation de 10°C réduit le temps D d’un facteur 10. Cette relation permet de calculer l’équivalence entre différents profils temps-température, concept fondamental pour la validation des cycles de stérilisation.
Le concept F₀ (F-zero) standardise la létalité des cycles de stérilisation à une température de référence de 121°C avec z = 10°C. Un F₀ de 8 minutes représente le minimum absolu pour la pharmacopée américaine (USP), tandis que la pharmacopée européenne (Ph. Eur.) recommande F₀ ≥ 8 pour les solutions aqueuses et F₀ ≥ 15 pour les dispositifs médicaux implantables. Les autoclaves pharmaceutiques modernes calculent F₀ en temps réel en intégrant les contributions létales de toutes les phases du cycle, incluant les montées et descentes en température.
CHAPITRE 2 : TYPOLOGIE DES AUTOCLAVES PHARMACEUTIQUES ET LEURS APPLICATIONS SPÉCIFIQUES

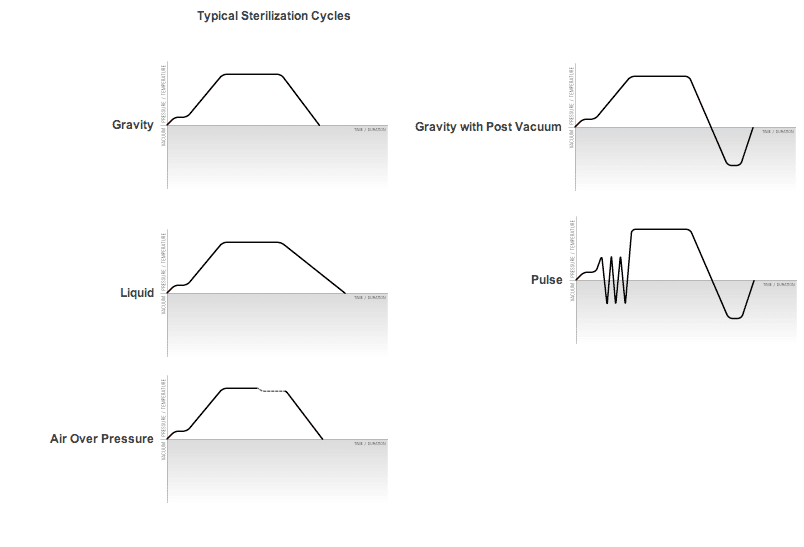
2.1 Autoclaves gravitaires pour charges liquides
Les autoclaves gravitaires, ou autoclaves à déplacement par gravité, exploitent la densité différentielle entre l’air froid (lourd) et la vapeur (légère) pour évacuer progressivement l’air de la chambre. La vapeur entre par le haut de l’enceinte, pousse l’air vers le bas, et l’expulse par un drain inférieur. Ce processus, relativement lent (10-15 minutes de purge), assure néanmoins une évacuation complète pour les charges non poreuses.
Ces autoclaves dominent la stérilisation des solutions aqueuses pharmaceutiques : médicaments injectables en flacons, ampoules, poches de perfusion, milieux de culture liquides, et solutions d’irrigation. Leur conception privilégie l’homogénéité thermique dans les fluides, évitant la surchauffe localisée qui pourrait dégrader les principes actifs thermosensibles.
L’industrie pharmaceutique utilise principalement des autoclaves gravitaires de grande capacité (500-5000 litres) pour le traitement terminal post-remplissage. Dans ce process, les récipients hermétiquement scellés subissent une stérilisation en sur-pression, maintenant l’intégrité des fermetures tout en éliminant tout contaminant résiduel. Les cycles typiques à 121°C pendant 15-20 minutes (F₀ = 8-12) préservent la stabilité chimique des formulations tout en garantissant la stérilité.
Les fabricants comme Getinge, Fedegari, Steris et Belimed proposent des autoclaves gravitaires conformes EN 285 avec des systèmes de refroidissement contrôlé prévenant le choc thermique sur les contenants en verre. L’intégration de systèmes de surpression d’air comprimé pendant le refroidissement compense la contraction de volume des liquides, évitant l’implosion des bouchons et l’intrusion microbienne.
2.2 Autoclaves à pré-vide pour charges poreuses et complexes
Les autoclaves à pré-vide (ou à vide pulsé) utilisent une pompe à vide pour extraire activement l’air de la chambre avant l’admission de vapeur. Ce processus, répété en plusieurs cycles de vide-vapeur (typiquement 3-4 pulses), élimine l’air de manière extrêmement efficace, permettant à la vapeur de pénétrer les charges poreuses, les emballages multicouches, et les dispositifs à lumières étroites.
Ces autoclaves constituent l’équipement de référence pour la stérilisation des dispositifs médicaux textiles (blouses, draps chirurgicaux), des instruments chirurgicaux complexes, des filtres HEPA, et des matériaux d’emballage poreux. Leur capacité à atteindre rapidement 134°C avec des cycles courts (3-4 minutes de plateau) optimise le débit de production tout en préservant les matériaux thermosensibles.
La phase de séchage final différencie radicalement les autoclaves à pré-vide. Après la phase de stérilisation, un vide poussé (typiquement 50-100 mbar) évapore instantanément l’humidité résiduelle, produisant des charges parfaitement sèches. Cette fonctionnalité s’avère critique pour les textiles et les dispositifs ne tolérant aucune humidité résiduelle.
En Europe, la norme EN 285 impose pour les autoclaves à pré-vide un test d’étanchéité quotidien (vacuum leak test) et un test de Bowie-Dick vérifiant la pénétration uniforme de la vapeur. Ces contrôles, absents pour les autoclaves gravitaires, reflètent la complexité supérieure et les risques associés aux systèmes à vide.
2.3 Autoclaves à vapeur pure (clean steam) pour applications aseptiques
Les autoclaves à vapeur pure (clean steam autoclaves) génèrent leur vapeur à partir d’eau WFI (Water For Injection), garantissant l’absence totale d’endotoxines, de particules, et de contaminants chimiques. Ces systèmes, extrêmement coûteux, sont réservés aux applications les plus critiques : stérilisation de composants entrant en contact direct avec des produits stériles (filtres, tubulures, composants de systèmes aseptiques), et traitement de dispositifs implantables exigeant une bio-compatibilité absolue.
La pharmacopée américaine USP <1229> et la directive EU GMP Annex 1 exigent l’utilisation de vapeur pure lorsque la vapeur entre en contact avec des surfaces critiques des produits stériles. Cette exigence s’applique notamment aux autoclaves de stérilisation-in-place (SIP) des équipements de production aseptique : bioréacteurs, cuves de fermentation, systèmes de filtration stérile, et lignes de remplissage aseptique.
La génération de vapeur pure nécessite des systèmes spécialisés : générateurs de vapeur pure (clean steam generators) utilisant de l’échange thermique entre vapeur d’utilité et WFI dans des échangeurs en acier inoxydable 316L électropoli, excluant tout contact entre WFI et vapeur d’usine potentiellement contaminée. La validation de ces systèmes inclut des tests exhaustifs d’endotoxines (LAL test, limite <0,25 EU/mL), de particules (limite selon USP <788>), et de non-condensables.
2.4 Autoclaves de stérilisation-in-place (SIP) intégrés aux lignes de production
Les systèmes SIP (Sterilization-In-Place) représentent une évolution majeure dans l’industrie pharmaceutique moderne. Ces autoclaves, intégrés directement aux équipements de production, stérilisent les systèmes sans démontage, maintenant l’intégrité aseptique de bout en bout. Les bioréacteurs de production de biopharmaceutiques, les lignes de remplissage aseptique, et les systèmes de chromatographie de purification intègrent désormais des capacités SIP.
Un cycle SIP typique commence par un rinçage à l’eau WFI chaude (80-90°C) éliminant les résidus de production, suivi d’une montée en température progressive à 121-134°C par injection de vapeur pure, puis d’un plateau de stérilisation (F₀ = 12-15 minimum), et finalement d’un refroidissement contrôlé sous air stérile filtré. L’ensemble du cycle, entièrement automatisé et documenté électroniquement, peut durer 2-4 heures selon la complexité du système.
La validation SIP présente des défis uniques : cartographie thermique exhaustive de tous les points critiques (dead legs, valves, capteurs), vérification de l’absence de zones froides (<121°C), qualification des systèmes de drainage (prévention de la re-contamination), et démonstration de la répétabilité sur minimum 3 cycles consécutifs. Les simulations par éléments finis (CFD – Computational Fluid Dynamics) sont désormais courantes pour optimiser la conception et prédire les profils thermiques.
CHAPITRE 3 : CADRES RÉGLEMENTAIRES INTERNATIONAUX ET EXIGENCES DE CONFORMITÉ
3.1 Réglementation FDA (États-Unis) : 21 CFR Part 211 et Guidances
La Food and Drug Administration (FDA) régit la stérilisation pharmaceutique aux États-Unis principalement à travers 21 CFR Part 211 (Current Good Manufacturing Practice for Finished Pharmaceuticals). Les sections §211.67 (Equipment Cleaning and Maintenance) et §211.113 (Control of Microbiological Contamination) établissent les exigences fondamentales pour les autoclaves pharmaceutiques.
La FDA n’impose pas de cycle de stérilisation spécifique, adoptant une approche performance-based. Les fabricants doivent démontrer que leurs cycles de stérilisation atteignent le SAL requis (10⁻⁶) pour leur produit spécifique, tenant compte de la bioburden initial, de la résistance thermique des contaminants identifiés, et des caractéristiques du produit (pH, activité de l’eau, composition). Cette flexibilité exige néanmoins une validation robuste documentée dans un Sterilization Validation Master Plan.
Le Guidance for Industry « Sterile Drug Products Produced by Aseptic Processing » (septembre 2004) constitue le document de référence. Il détaille les attentes concernant la qualification des autoclaves (Installation Qualification IQ, Operational Qualification OQ, Performance Qualification PQ), la validation des cycles de stérilisation (biological indicator studies, temperature distribution studies, heat penetration studies), et la maintenance préventive.
Les inspections FDA (Pre-Approval Inspections pour nouveaux produits, Routine Inspections périodiques) vérifient scrupuleusement la documentation de validation, les enregistrements de cycles (batch records), les résultats de requalification annuelle, et la gestion des déviations. Les Form 483 (observations d’inspection) et Warning Letters liés aux défaillances de stérilisation représentent une cause majeure de sanctions réglementaires, incluant la suspension de production et le rappel de lots.
3.2 Réglementation européenne : EU GMP et Annex 1 révisé
En Europe, l’Agence Européenne des Médicaments (EMA) et les autorités nationales (ANSM en France, MHRA au Royaume-Uni, PEI en Allemagne) appliquent les EU Guidelines to Good Manufacturing Practice (EU GMP). L’Annex 1 « Manufacture of Sterile Medicinal Products », révisé en août 2022 après une décennie de consultation, représente le texte le plus détaillé et le plus prescriptif au monde concernant la fabrication de produits stériles.
L’Annex 1 révisé introduit des exigences significativement renforcées : approche basée sur les risques (Quality Risk Management selon ICH Q9) pour toutes les décisions de stérilisation, système de management de la contamination (Contamination Control Strategy formalisé), et exigences de validation lifecycle incluant continued process verification. L’accent sur la culture qualité et la surveillance continue transforme fondamentalement l’approche européenne.
Concernant spécifiquement les autoclaves, l’Annex 1 exige : qualification formelle selon la cascade IQ-OQ-PQ, revalidation périodique (annuelle minimum ou après modification significative), utilisation d’indicateurs biologiques pour chaque validation, monitoring continu des paramètres critiques avec alarmes, et investigation formelle de toute déviation aux paramètres validés.
La directive 2001/83/EC et le Regulation (EU) 2017/745 (Medical Device Regulation) imposent des exigences complémentaires pour les dispositifs médicaux stériles. La conformité EN ISO 17665-1:2024 devient obligatoire, harmonisant les pratiques européennes avec les standards ISO internationaux.
3.3 Réglementations japonaises : PMDA et J-GMP
Au Japon, la Pharmaceuticals and Medical Devices Agency (PMDA) supervise la réglementation pharmaceutique selon les Japanese Good Manufacturing Practice (J-GMP), alignés progressivement sur les standards ICH et PIC/S (Pharmaceutical Inspection Co-operation Scheme). Les Ministerial Ordinances on Standards for Manufacturing Control and Quality Control (MHLW Ordinance No. 179) définissent les exigences spécifiques pour la stérilisation.
La culture japonaise de précision et de perfectionnement continu (Kaizen) imprègne profondément l’approche réglementaire. Les autorités japonaises attendent une documentation exhaustive, une traçabilité absolue, et une démonstration de continuous improvement. Les cycle de stérilisation doivent être validés selon des protocoles extrêmement détaillés, incluant des études de worst-case challenge avec bioburden artificiellement élevé.
Les fabricants exportant vers le Japon doivent obtenir une GMP certification délivrée après inspection par la PMDA ou une autorité reconnue (Mutual Recognition Agreement avec EU, WHO certification). Le processus, réputé rigoureux et chronophage, requiert fréquemment des clarifications techniques approfondies et des études complémentaires.
Le Japon a développé des standards techniques nationaux harmonisés avec ISO, notamment JIS T 0841-1 (équivalent ISO 17665-1) pour la stérilisation à la vapeur. L’adoption progressive de ces standards internationaux facilite la reconnaissance mutuelle et l’harmonisation globale.
3.4 Standards techniques internationaux : ISO 17665, EN 285, USP
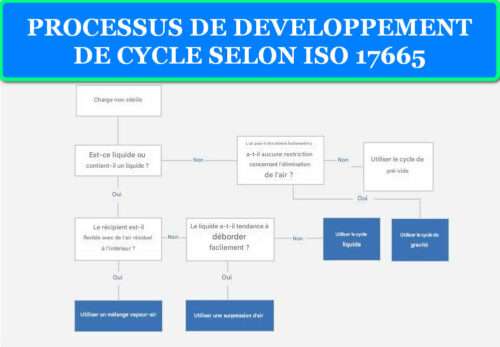
L’International Organization for Standardization (ISO) a publié ISO 17665-1:2024 « Sterilization of health care products — Moist heat — Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices ». Ce standard, référence mondiale, définit méthodologies et critères d’acceptation pour tous les aspects de la stérilisation par vapeur.
ISO 17665-1 structure le processus de validation en trois phases : Process Definition (définition des paramètres critiques basée sur la résistance microbienne et les caractéristiques du produit), Process Qualification (IQ, OQ, PQ formels démontrant la capacité du processus), et Process Control (monitoring de routine et maintenance du statut validé). Le standard impose minimum 3 cycles consécutifs réussis pour chaque phase de qualification.
La norme européenne EN 285:2015 « Sterilization – Steam sterilizers – Large sterilizers » spécifie les exigences de construction, performance, et testing pour les autoclaves de grande capacité (volume ≥60L ou chambre accommodant ≥1 unité de stérilisation). EN 285 définit des tests d’acceptation exhaustifs : vacuum leak test (taux de fuite <1.3 mbar/minute), Bowie-Dick test (détection d’air résiduel), steam quality tests (dryness, superheat, non-condensables), et temperature distribution tests.
La United States Pharmacopeia (USP) Chapitre <1229> « Sterilization of Compendial Articles » fournit des guidelines spécifiques pour la stérilisation des articles pharmaceutiques. Bien que non-binding légalement (contrairement aux chapitres <1000), USP <1229> représente le standard de pratique reconnu universellement. Il détaille les paramètres minimaux pour différents types de charges et les méthodologies de validation.
Ces standards convergent progressivement grâce aux efforts d’harmonisation ICH (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use) et PIC/S. L’objectif : une reconnaissance mutuelle des validations entre juridictions, réduisant la duplication des efforts tout en maintenant les standards de sécurité.
CHAPITRE 4 : PROTOCOLES DE VALIDATION ET QUALIFICATION DES AUTOCLAVES

4.1 Qualification d’Installation (IQ) : Documentation et vérification physique
La Qualification d’Installation (Installation Qualification – IQ) constitue la première étape formelle de validation, documentant que l’autoclave a été installé conformément aux spécifications du fabricant et aux exigences réglementaires. L’IQ ne teste pas les performances mais vérifie l’intégrité de l’installation.
Un protocole IQ typique inclut : vérification des documents techniques (manuels d’utilisation, de maintenance, certificats de conformité CE/FDA), inspection visuelle complète (absence de dommages, propreté, identification correcte), vérification des utilities (vapeur, électricité, eau, air comprimé, drainage conforme aux spécifications), calibration des instruments critiques (sondes de température, capteurs de pression, transmetteurs), et vérification des systèmes de sécurité (soupapes de surpression, interlocks, alarmes).
La documentation IQ doit inclure : plans d’implantation (layout drawings), schémas P&ID (Piping and Instrumentation Diagrams), liste des composants critiques avec numéros de série, certificats de calibration initiaux des instruments, et procédures d’exploitation standard (SOPs) pour l’opération et la maintenance. Chaque vérification est documentée dans un rapport IQ signé par le responsable qualification, le responsable production, et le responsable assurance qualité.
Les instruments de mesure utilisés pour la qualification doivent eux-mêmes être calibrés avec traçabilité aux standards nationaux (NIST aux États-Unis, PTB en Allemagne, LNE en France). Les certificats de calibration ISO 17025 accrédités sont exigés, démontrant une incertitude de mesure compatible avec les tolérances de processus (typiquement ±0,5°C pour les sondes de température, ±50 mbar pour les capteurs de pression).
La Qualification Opérationnelle (Operational Qualification – OQ) démontre que l’autoclave fonctionne selon ses spécifications dans toute sa plage opérationnelle, sans charge de produit. L’OQ teste systématiquement tous les sous-systèmes et fonctions de sécurité.
Les tests OQ obligatoires incluent :
Tests d’étanchéité et de vide : Vacuum leak test (autoclaves à pré-vide) mesurant le taux de remontée en pression après création d’un vide à 60 mbar absolu. Le critère d’acceptation EN 285 impose une remontée <1,3 mbar/minute sur 10 minutes, garantissant l’intégrité des joints et l’absence de fuites d’air.
Test de Bowie-Dick : Test diagnostic détectant l’air résiduel entravant la pénétration de vapeur. Un pack standardisé de textiles contenant une feuille indicatrice chimique thermochromique est placé au centre de la chambre vide. Après un cycle à 134°C pendant 3,5 minutes, l’indicateur doit présenter un virage de couleur uniforme. Tout pattern irrégulier signale une poche d’air résiduel, nécessitant investigation et correction.
Tests de qualité de vapeur : Mesures de dryness fraction (méthode gravimétrique : condensation de vapeur dans un piège calibré, pesée pour déterminer le ratio vapeur/condensat), superheat (mesure simultanée température/pression avec comparaison aux tables vapeur saturée), et non-condensable gases (méthode vacuum pum down : évacuation de l’atmosphère de la chambre sous vide et analyse du résidu non-condensé).
Tests de distribution et homogénéité thermique : Installation de thermocouples de référence (minimum 12-16 points) dans toute la chambre vide (coins, centre, niveau drains) et réalisation de 3 cycles consécutifs au paramètre nominal. Tous les points doivent atteindre la température de stérilisation avec une tolérance de ±2°C maximum et maintenir cette température pendant toute la phase de plateau.
Tests de corrélation pression-température : Vérification que la température mesurée correspond à la température théorique de vapeur saturée pour la pression observée (selon tables thermodynamiques). Un écart >2°C indique une contamination par gaz non-condensables.
Tests des systèmes de sécurité et alarmes : Vérification de tous les interlocks (impossibilité d’ouvrir la porte sous pression), déclenchement des alarmes (température, pression, durée), et fonctionnement des dispositifs de sécurité (soupapes de surpression, systèmes d’arrêt d’urgence).
La Qualification de Performance (Performance Qualification – PQ) démontre que l’autoclave stérilise efficacement la charge de produit réelle dans les conditions opérationnelles de routine. La PQ constitue l’étape la plus critique, validant l’intégralité du processus de stérilisation.
La PQ nécessite une caractérisation préalable de la charge : identification du worst-case loading pattern (configuration de chargement présentant le défi thermique maximal), détermination de la cold spot (point le plus lent à atteindre la température de stérilisation), et évaluation du bioburden typique des produits.
Les études de pénétration thermique (heat penetration studies) constituent le cœur de la PQ. Des thermocouples de référence calibrés sont placés aux points critiques identifiés dans la charge de produit (centres de flacons, zones profondes de packs textiles, intérieurs de dispositifs tubulaires). Un data logger haute résolution (acquisition ≥1 mesure/seconde) enregistre les profils température-temps pendant au moins 3 cycles consécutifs.
Les critères d’acceptation exigent que tous les points de mesure atteignent la température de stérilisation validée et l’y maintiennent pendant la durée complète du plateau. Le calcul F₀ cumulatif pour chaque point doit dépasser la valeur minimale validée (typiquement F₀ ≥8 selon USP, F₀ ≥15 pour dispositifs critiques selon Ph. Eur.).
La validation microbiologique utilise des indicateurs biologiques (biological indicators – BI) contenant des spores de Geobacillus stearothermophilus à population définie (10⁶ spores minimum). Les BI sont placés aux mêmes emplacements que les thermocouples lors d’un cycle de PQ. Après le cycle, les BI sont incubés (55-60°C pendant 7 jours) et observés pour croissance microbienne. L’absence totale de croissance sur tous les BI confirme l’efficacité létale du cycle.
Les autoclaves pharmaceutiques modernes automatisent partiellement cette démarche via des systèmes de validation intégrés (Integrated Validation Systems) utilisant des sondes de température sans fil autonomes placées dans la charge, communiquant par radiofréquence avec une station réceptrice externe.
4.4 Revalidation périodique et gestion du changement
La validation n’est pas un événement ponctuel mais un processus continu. Les régulations FDA 21 CFR §211.110(a) et EU GMP Annex 15 exigent la revalidation des processus critiques à intervalles réguliers et suite à tout changement significatif.
La revalidation périodique (minimum annuelle, fréquence accrue selon évaluation de risque) répète les études PQ avec charge de produit actuelle. Cette revalidation confirme que les performances de l’autoclave n’ont pas dérivé avec l’usure et que le processus reste dans son état validé.
La gestion du changement (change control) formalise l’évaluation de tout changement potentiellement impactant : modification d’un composant critique (pompe à vide, générateur vapeur), changement de configuration de charge, nouvelle présentation de produit, modification de paramètres opératoires. Chaque changement nécessite une évaluation de risque (Risk Assessment selon ICH Q9) déterminant l’étendue de la revalidation requise.
Les programmes de continued process verification, concept renforcé dans l’Annex 1 révisé 2022, imposent un monitoring statistique continu des paramètres critiques pour détecter précocement toute tendance de dérive (trending). Les techniques de Statistical Process Control (SPC) avec cartes de contrôle Shewhart et analyses de capabilité processus (Cp, Cpk) quantifient la robustesse et permettent une maintenance prédictive.
CHAPITRE 5 : CONTRÔLES DE ROUTINE ET MONITORING CONTINU

5.1 Tests quotidiens obligatoires et leur signification
Chaque jour d’utilisation, avant tout cycle de production, les autoclaves pharmaceutiques doivent subir des tests de contrôle confirmant leur état opérationnel. Ces tests, définis dans les SOPs validées et les Work Instructions, documentent la readiness de l’équipement.
Le vacuum leak test quotidien (autoclaves à pré-vide) détecte toute dégradation des joints, fissure de porte, ou dysfonctionnement de la pompe à vide. Sa réalisation systématique prévient le risque de cycles inefficaces par contamination d’air. Les résultats, enregistrés dans le logbook de l’équipement, font l’objet d’un trending mensuel.
Le Bowie-Dick test quotidien (obligatoire EN 285 pour autoclaves à pré-vide utilisés pour charges poreuses) assure la pénétration correcte de vapeur. Des packs Bowie-Dick commerciaux (pack chimique standardisé) ou des systèmes électroniques équivalents (Bowie-Dick electronic test devices) fournissent un résultat pass/fail immédiat. Un échec déclenche une investigation formelle et impose l’arrêt de production jusqu’à résolution et retest réussi.
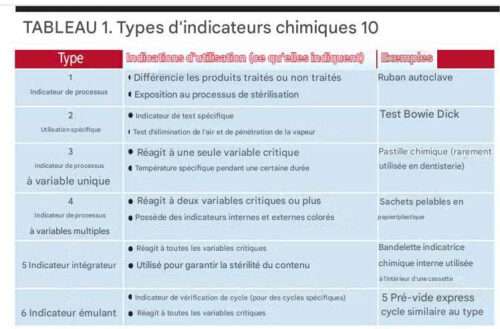
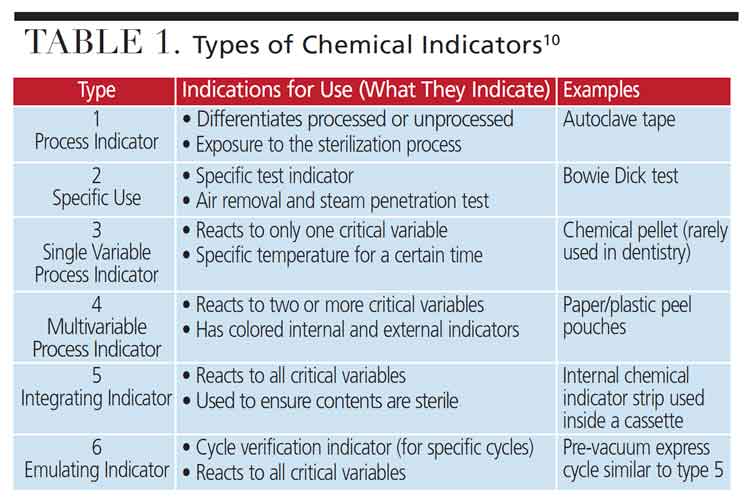
Les indicateurs chimiques process (chemical indicators Class 1 selon ISO 11140-1) placés dans chaque charge distinguent visuellement les articles traités des non-traités. Ces indicateurs, bien que ne garantissant pas la stérilité, constituent un contrôle process critique prévenant les mélanges articles stériles/non-stériles.
5.2 Enregistrement électronique et Data Integrity
Les autoclaves pharmaceutiques modernes intègrent des systèmes d’enregistrement électronique (Electronic Batch Records – EBR) conformes à 21 CFR Part 11 (USA) et Annex 11 EU GMP (Europe). Ces systèmes capturent automatiquement tous les paramètres critiques (température multipoints, pression, durée phases) avec horodatage infalsifiable.
Les principes ALCOA+ (Attributable, Legible, Contemporaneous, Original, Accurate + Complete, Consistent, Enduring, Available) régissent l’intégrité des données. Chaque enregistrement doit être attribuable à un opérateur identifié (login unique), contemporain (horodatage automatique), original (stockage en format natif non-altérable), et disponible pour inspection réglementaire durant toute la durée de rétention (minimum 3 ans post-expiration du produit selon FDA, 5 ans selon EU).
Les systèmes SCADA (Supervisory Control and Data Acquisition) interfacés avec les autoclaves permettent le monitoring temps-réel, la génération automatique d’alarmes en cas de dérive paramétrique, et l’archivage centralisé. L’intégration avec les systèmes LIMS (Laboratory Information Management Systems) et MES (Manufacturing Execution Systems) assure la traçabilité complète batch-to-equipment-to-results.
Les audits data integrity constituent désormais une priorité des inspections réglementaires. Les Warning Letters FDA et les Critical findings EU liés aux manipulations de données (data falsification, deletion, unauthorized modifications) ont augmenté drastiquement. Les fabricants investissent massivement dans des systèmes audit trail robustes, backup redondants, et contrôles d’accès stricts.
5.3 Indicateurs biologiques et challenge tests périodiques
Bien que non requis pour chaque cycle de routine (sauf protocoles spécifiques), les indicateurs biologiques (BI) sont utilisés périodiquement pour confirmer l’efficacité létale des cycles. Les programmes de surveillance recommandent des tests BI hebdomadaires ou mensuels selon le niveau de criticité.
Les BI commerciaux (ATCC, Mesa Labs, 3M, Merck) contiennent des spores de Geobacillus stearothermophilus ATCC 7953 ou ATCC 12980 à population calibrée (10⁶ UFC typiquement). Les strips BI sont placés aux points cold spot identifiés lors de la validation PQ, subissent le cycle de production standard, puis sont incubés dans un milieu de culture spécifique (Tryptic Soy Broth) à 55-60°C pendant 7 jours. L’observation quotidienne détecte toute croissance (turbidité, virage colorimétrique) indiquant une survie microbienne.
Les tests positifs contrôles (BI non-exposés incubés parallèlement) confirment la viabilité des spores. Les tests négatifs contrôles (milieu de culture stérile incubé) confirment l’absence de contamination du système d’incubation. La documentation photographique et les résultats spectrophotométriques (mesure densité optique) fournissent des preuves objectives.
Les fractional cycle studies, études avancées réservées à la validation, exposent des BI à des fractions du cycle complet (50%, 75% de la durée de plateau) pour déterminer le safety margin du processus. Ces études démontrent la robustesse en prouvant que même des cycles partiels atteignent une inactivation significative.
CHAPITRE 6 : MAINTENANCE PRÉVENTIVE ET GESTION DU CYCLE DE VIE

6.1 Programme de maintenance préventive basé sur les risques
La maintenance préventive (Preventive Maintenance – PM) des autoclaves pharmaceutiques transcende le simple entretien technique pour constituer une exigence réglementaire critique. La FDA 21 CFR §211.67 et EU GMP Chapter 3 imposent des programmes PM documentés, basés sur les recommandations fabricant et l’historique opérationnel.
Un programme PM robuste structure les interventions selon plusieurs niveaux : maintenance quotidienne (nettoyage chambre, vérification joints porte, inspection visuelle), maintenance hebdomadaire (vérification filtres, test systèmes drainage), maintenance mensuelle (lubrification pièces mécaniques, vérification sondes température), maintenance trimestrielle (nettoyage complet circuits vapeur, inspection valves sécurité), maintenance semestrielle (démontage/inspection pompe vide, vérification échangeurs thermiques), et maintenance annuelle (révision complète avec remplacement pièces d’usure, recalibration tous instruments).
L’approche Risk-Based Maintenance, alignée sur ICH Q9, priorise les ressources sur les composants critiques impactant directement la stérilité. Les pompes à vide, générateurs vapeur, sondes température, et systèmes de sécurité reçoivent une attention prioritaire avec des fréquences de maintenance réduites et des stocks de pièces de rechange dédiés.
Les systèmes CMMS (Computerized Maintenance Management Systems) automatisent la planification, déclenchent des work orders automatiques selon les compteurs d’utilisation (nombre de cycles, heures de fonctionnement), et assurent la traçabilité complète des interventions. Chaque activité PM est documentée avec : date, technicien responsable, actions réalisées, pièces remplacées, observations, et conclusion (équipement released/not released for use).
6.2 Calibration et vérification métrologique
Les instruments de mesure et de contrôle de l’autoclave (sondes température, capteurs pression, transmetteurs, indicateurs, enregistreurs) requièrent une calibration périodique garantissant l’exactitude des mesures. Les fréquences de calibration, définies selon les recommandations fabricant et l’analyse de risque, s’établissent typiquement entre 6 et 12 mois.
La calibration, réalisée par des laboratoires accrédités ISO 17025 ou des techniciens qualifiés utilisant des standards traçables NIST/PTB, vérifie chaque instrument à minimum 3 points dans sa plage d’utilisation. Pour une sonde de température 0-150°C utilisée pour cycles à 121-134°C, la calibration couvre typiquement 100°C, 121°C, et 135°C. Le certificat de calibration documente les valeurs trouvées (as-found), les ajustements effectués, les valeurs finales (as-left), et l’incertitude de mesure.
Les critères d’acceptation définissent les tolérances acceptables. Pour les sondes de température critiques, une exactitude ±0,5°C est standard. Les instruments hors tolérance déclenchent une investigation OOS (Out-Of-Specification) : évaluation d’impact (cycles réalisés depuis dernière calibration réussie), décision sur le statut des lots traités (possibilité de rappel), actions correctives (remplacement instrument, ajustement fréquence calibration).
Les vérifications fonctionnelles (functional checks) entre calibrations formelles confirment la stabilité métrologique. Ces checks, réalisés avec des standards portables (thermomètres étalons, manomètres de référence), fournissent une assurance continue sans nécessiter démontage des instruments.
6.3 Gestion des pannes et investigations de déviations
Malgré une maintenance rigoureuse, les pannes surviennent inévitablement. La gestion structurée des pannes selon les principes CAPA (Corrective and Preventive Actions) minimise leur impact et prévient les récurrences.
Toute panne, défaillance, ou déviation paramétrique déclenche un Deviation Report formel. Ce document capture : description détaillée de l’événement, circonstances (date, heure, cycle concerné, produit traité), investigation root cause (analyse 5 Whys, Ishikawa diagram, Failure Mode Analysis), évaluation d’impact qualité sur les produits traités, actions correctives immédiates (quarantaine lots, retraitement, destruction), et actions préventives (modifications SOP, formation personnel, upgrade équipement).
Les pannes critiques impactant directement la stérilité (échec du cycle, température insuffisante, durée plateau incomplète) nécessitent une investigation approfondie avec possibilité d’implication des autorités réglementaires en cas d’impact produits commercialisés. Les procédures de recall (rappel de lots) s’activent si l’investigation révèle un risque patient.
Le trending des pannes (fréquence, types, composants impliqués) identifie les patterns systémiques. Une augmentation de pannes pompe à vide signale potentiellement un problème de qualité vapeur (humidité excessive usant prématurément les palettes). Une recrudescence d’alarmes température peut indiquer une dérive des sondes ou un problème générateur vapeur.
6.4 Modernisation et remplacement des équipements obsolètes
Les autoclaves pharmaceutiques, investissements majeurs (100k$ à 1M$ selon capacité), ont une espérance de vie typique de 15-20 ans avec maintenance adéquate. Toutefois, l’obsolescence technologique et réglementaire justifie souvent un remplacement anticipé.
L’obsolescence électronique constitue un défi majeur. Les automates programmables (PLC) et systèmes de contrôle des années 1990-2000 deviennent difficiles à maintenir (composants discontinués, expertise technique raréfiée, incompatibilité avec systèmes informatiques modernes). Les upgrades électroniques (retrofit) remplacent les contrôleurs obsolètes par des systèmes modernes tout en conservant la structure mécanique éprouvée.
L’évolution réglementaire force également la modernisation. Les exigences data integrity 21 CFR Part 11 et Annex 11 impossibles à implémenter sur d’anciens systèmes papier justifient l’upgrade vers des systèmes électroniques conformes. La révision Annex 1 2022 avec ses exigences Contamination Control Strategy et Real-Time Monitoring favorise les technologies modernes (monitoring sans fil, analytics prédictifs).
Les projets de remplacement suivent une méthodologie rigoureuse : User Requirements Specification (URS) définissant besoins fonctionnels et réglementaires, évaluation fournisseurs (audit qualité, revue Track Record), Factory Acceptance Test (FAT) avant expédition, Site Acceptance Test (SAT) après installation, et validation complète (IQ/OQ/PQ). Le délai total projet-to-operational peut atteindre 12-18 mois pour des autoclaves de production critique.
CHAPITRE 7 : APPLICATIONS PHARMACEUTIQUES SPÉCIFIQUES ET CAS D’USAGE

7.1 Stérilisation terminale des médicaments injectables
La stérilisation terminale par autoclave représente la méthode de référence pour les préparations injectables aqueuses thermostables : solutions salines, glucose, électrolytes, certains antibiotiques, vitamines, et vaccins. Ce procédé, appliqué après remplissage et scellement hermétique, garantit le SAL maximal (10⁻⁶) exigé pour les produits injectables.
Les cycles de stérilisation terminale typiques opèrent à 121°C pendant 15-20 minutes (F₀ = 8-12), température préservant la stabilité chimique de la majorité des principes actifs tout en assurant l’inactivation microbienne totale. Les autoclaves dédiés intègrent des systèmes de refroidissement contrôlé prévenant la surchauffe (overshoot) dommageable et le choc thermique sur les contenants en verre.
Le phénomène de container closure integrity (intégrité fermeture-contenant) constitue un défi critique. Les bouchons en caoutchouc/élastomère et les caps aluminium doivent maintenir l’étanchéité malgré les cycles thermiques répétés et les variations pression. Les autoclaves pharmaceutiques utilisent des systèmes de contre-pression (overpressure) : injection d’air comprimé dans la chambre pendant le refroidissement pour maintenir une pression externe supérieure ou égale à la pression interne des flacons, prévenant l’expulsion des bouchons et l’intrusion microbienne.
La stérilisation terminale, lorsque possible, est préférée réglementairement au remplissage aseptique (aseptic processing). L’Annex 1 EU GMP stipule explicitement : « Terminal sterilization is recognized as the method of choice wherever possible ». Cette préférence reflète la robustesse supérieure et le risque contamination minimisé comparativement aux processus aseptiques dépendants de l’environnement contrôlé.
7.2 Préparation des dispositifs médicaux et composants aseptiques
Les dispositifs médicaux implantables (prothèses articulaires, implants cardiovasculaires, lentilles intraoculaires) et les composants critiques des systèmes aseptiques (filtres stérilisants, tubulures de transfert, connectors) subissent une stérilisation autoclave préalable à leur utilisation.
Les matériaux constituant ces dispositifs imposent des contraintes spécifiques. Les polymères thermoplastiques (polycarbonate, polysulfone, PEEK) tolèrent des cycles à 121°C mais se dégradent à 134°C. Les élastomères (silicone, polyuréthane) résistent bien mais peuvent absorber humidité, nécessitant des phases de séchage prolongées. Les métaux (titane, acier inoxydable) supportent sans problème les températures maximales mais leur masse thermique élevée prolonge les temps de pénétration thermique.
Les emballages de stérilisation (sterilization wraps, pouches) jouent un rôle critique. Les matériaux non-tissés (Spunbond-Meltblown-Spunbond SMS, Tyvek®) doivent simultanément permettre la pénétration vapeur, résister mécaniquement au cycle, et maintenir une barrière microbienne post-stérilisation. La validation des emballages inclut des tests de peel strength (résistance pelage scellures), air permeability (perméabilité air), et microbial barrier (efficacité barrière microbienne selon ASTM F1608).
Les cycles de stérilisation pour dispositifs suivent typiquement des profils 134°C pendant 3-4 minutes (pré-vide pulsé) pour charges poreuses/emballées, ou 121°C pendant 30 minutes (gravitaire) pour dispositifs immergés en solution. La validation PQ place des BI et thermocouples dans les zones critiques (lumières internes cathéters, cavités prothèses) démontrant la pénétration adéquate vapeur/chaleur.
7.3 Décontamination des déchets pharmaceutiques et biologiques
Les autoclaves de décontamination (waste autoclaves) traitent les déchets biologiques et pharmaceutiques avant élimination, inactivant tous agents infectieux potentiels. Cette application, régie par des réglementations environnementales et biohazard, nécessite des cycles particulièrement robustes.
Les déchets incluent : cultures microbiennes, milieux contaminés, dispositifs souillés par fluides corporels, animaux d’expérimentation euthanasiés, tissus biologiques, et résidus de production de médicaments biologiques. La charge hétérogène, souvent emballée en sacs autoclavables renforcés, présente des défis de pénétration thermique significatifs.
Les cycles de décontamination opèrent typiquement à 134°C pendant 60-90 minutes minimum, assurant un F₀ ≥ 100 (inactivation 10-log supérieure aux exigences produits stériles). Les autoclaves déchets intègrent fréquemment des broyeurs intégrés (shredders) fragmentant les déchets post-stérilisation, réduisant le volume et rendant irrécupérables les matériaux potentiellement valorisables illégalement.
La validation microbiologique utilise des bio-indicateurs hautement résistants (Geobacillus stearothermophilus à population 10⁷-10⁸) placés au cœur des charges de déchets simulées. Des tests avec organismes surrogates (virus bactériophages MS2, prions PrP selon applications) démontrent l’efficacité contre les agents les plus résistants.
Les effluents liquides des autoclaves déchets (condensats potentiellement contaminés) nécessitent traitement avant rejet. Les systèmes de drainage intègrent des filtres HEPA, traitements chimiques (hypochlorite), ou réchauffage terminal garantissant l’élimination totale de contaminants avant évacuation égouts.
7.4 Stérilisation-in-place (SIP) des équipements de production
Les lignes de production pharmaceutique modernes, particulièrement pour les biopharmaceutiques (protéines recombinantes, anticorps monoclonaux, vaccins), intègrent des capacités SIP sophistiquées. Ces systèmes stérilisent les bioréacteurs, chromatographes, systèmes de filtration, et lignes de transfert sans démontage, préservant l’intégrité aseptique.
Un cycle SIP complet d’un bioréacteur de 2000L comprend : phase de rinçage WFI chaude 80°C (élimination résidus production et agents nettoyants), montée en température progressive à 121-134°C par injection vapeur pure (taux 5-10°C/min prévenant le choc thermique sur les sondes et joints), plateau de stérilisation 30-60 minutes (F₀ ≥ 15), refroidissement contrôlé 50-60°C (injection WFI froide dans échangeurs thermiques jacket), et pressurisation air stérile filtré (maintien surpression positive prévenant intrusion contaminants).
La validation SIP présente des défis uniques. La cartographie thermique doit identifier tous les cold spots potentiels : zones de stagnation (dead legs), valves complexes, piquages de capteurs, points hauts accumulant air. Les études CFD (Computational Fluid Dynamics) modélisent les écoulements vapeur et prédisent les profils thermiques, optimisant la conception avant construction.
Les bioréacteurs single-use (usage unique), tendance croissante en biopharmacie, éliminent partiellement le besoin de SIP. Ces systèmes pré-stérilisés par irradiation gamma arrivent prêts à l’emploi, réduisant drastiquement les temps de préparation et les risques de contamination croisée. Cependant, les équipements multi-use (réutilisables) restent majoritaires pour les productions large-échelle, maintenant la pertinence de la technologie autoclave SIP.
CHAPITRE 8 : DÉFIS CONTEMPORAINS ET INNOVATIONS TECHNOLOGIQUES
8.1 Sustainability et réduction d’empreinte environnementale
L’industrie pharmaceutique, sous pression croissante pour réduire son empreinte carbone, réexamine les processus énergivores. Les autoclaves, consommateurs majeurs de vapeur (énergie), d’eau (génération vapeur, refroidissement), et d’électricité (pompes vide, contrôles), font l’objet d’innovations sustainability.
Les autoclaves nouvelle génération intègrent des systèmes de récupération d’énergie : échangeurs thermiques récupérant la chaleur des condensats et l’utilisant pour préchauffer l’eau d’alimentation, réduction de 20-30% de la consommation vapeur. Les systèmes de pompes à vide à vitesse variable (VFD – Variable Frequency Drives) ajustent dynamiquement la puissance selon les besoins, économisant 40-50% d’électricité comparativement aux pompes vitesse fixe traditionnelles.
La tendance vers la génération vapeur on-site par générateurs électriques (electric steam generators) plutôt que chaudières centrales gaz/fuel réduit les pertes de distribution et améliore le bilan carbone dans les régions à électricité décarbonée. Les générateurs vapeur pure intégrés aux autoclaves éliminent le besoin de boucles de distribution vapeur complexes, simplifiant la validation et réduisant les risques contamination.
La récupération et recyclage des condensats propres (clean steam condensates) pour réalimentation des générateurs économise eau purifiée, ressource précieuse nécessitant traitement énergivore (osmose inverse, électrodéionisation). Les systèmes de monitoring de conductivité en continu garantissent que seuls les condensats conformes aux spécifications WFI sont recyclés.
Les initiatives « Green GMP » encouragées par les autorités réglementaires reconnaissent que sustainability et qualité ne sont pas antagonistes. L’EMA et la FDA valorisent désormais les approches réduisant gaspillages (lean manufacturing), optimisant ressources, et minimisant déchets, à condition que la qualité produit et la sécurité patient demeurent inchangées.
8.2 Digitalisation, Industry 4.0, et smart autoclaves
La transformation digitale (Industry 4.0) révolutionne les autoclaves pharmaceutiques. Les smart autoclaves intègrent des capteurs IoT (Internet of Things), analytics prédictifs, machine learning, et connectivité cloud, transformant des équipements isolés en composants d’écosystèmes digitaux intelligents.
Les capteurs sans fil autonomes (batterie longue durée ou récupération énergie) positionnés dans les charges transmettent en temps réel les profils température-humidité vers des systèmes analytics cloud. Ces données, agrégées sur des milliers de cycles, alimentent des modèles prédictifs identifiant les patterns précurseurs de pannes (predictive maintenance). Un algorithme machine learning détecte qu’une dérive progressive du temps de montée en température (heat-up time) de 5% sur 3 mois précède typiquement une panne d’échangeur thermique, déclenchant une intervention préventive évitant l’arrêt non-planifié.
Les digital twins (jumeaux numériques) répliquent virtuellement l’autoclave physique, simulant en temps réel son comportement thermodynamique. Ces modèles, calibrés par données réelles IoT, prédisent l’impact de modifications opératoires (nouveau pattern de chargement, modification paramètres) sans nécessiter essais physiques, accélérant drastiquement le développement process.
La blockchain trouve des applications émergentes pour la traçabilité inaltérable. Chaque cycle de stérilisation génère un hash cryptographique unique enregistré dans une blockchain privée pharmaceutique, garantissant l’immutabilité des données et simplifiant les audits réglementaires. Les smart contracts automatisent la libération des lots (batch release) lorsque tous les critères qualité sont satisfaits.
L’intelligence artificielle optimise les cycles de stérilisation. Des algorithmes génétiques explorent des millions de combinaisons paramètres (températures, durées, profils pression) pour identifier les cycles minimisant temps/énergie tout en garantissant le SAL requis, concept de « Green Sterilization Cycles » émergeant dans la littérature scientifique.
8.3 Alternatives et méthodes complémentaires de stérilisation
Bien que l’autoclave vapeur reste la référence gold standard, des méthodes alternatives gagnent en importance pour les applications où la chaleur humide est incompatible.
La stérilisation par oxyde d’éthylène (EtO), procédé basse température (<60°C), stérilise les dispositifs thermosensibles (électronique, optique, polymères fragiles). Toutefois, EtO, cancérigène et explosif, fait face à des restrictions environnementales croissantes (EPA regulations USA, REACH Europe) et nécessite des périodes d’aération longues (7-14 jours) pour éliminer les résidus toxiques.
La stérilisation par rayonnement (gamma, e-beam, X-ray) opère à température ambiante, pénètre profondément les emballages, et ne laisse aucun résidu. Les doses typiques 25 kGy assurent un SAL 10⁻⁶. Cependant, certains polymères subissent une dégradation radiologique (chaînes scission, crosslinking), et les infrastructures centralisées d’irradiation imposent une logistique complexe.
Le peroxyde d’hydrogène vaporisé (VHP – Vaporized Hydrogen Peroxide), système basse température générant un plasma H₂O₂, stérilise efficacement les surfaces et les charges à lumières restreintes. Les systèmes VHP trouvent application croissante pour la bio-décontamination de salles blanches, d’isolateurs aseptiques, et de RABS (Restricted Access Barrier Systems).
L’ozone, oxydant puissant, émerge comme alternative écologique (décomposition spontanée en O₂). Les autoclaves ozone, encore expérimentaux, promettent stérilisation basse température sans résidus toxiques. Néanmoins, leur validation réglementaire reste incomplète, limitant l’adoption commerciale.
Ces alternatives complètent plutôt que remplacent l’autoclave vapeur. L’approche optimale sélectionne la méthode selon les caractéristiques du produit : autoclave pour thermostables, EtO/irradiation pour thermosensibles, VHP pour surfaces et équipements. Le concept de « sterilization portfolio » diversifié assure flexibilité et résilience face aux contraintes réglementaires évolutives.
8.4 Standardisation internationale et harmonisation réglementaire
L’industrie pharmaceutique globalisée bénéficierait immensément d’une harmonisation réglementaire complète. Les initiatives ICH (International Council for Harmonisation), PIC/S (Pharmaceutical Inspection Co-operation Scheme), et WHO (World Health Organization) progressent vers cet objectif mais des différences persistent.
ICH Q7 (Good Manufacturing Practice Guide for Active Pharmaceutical Ingredients) fournit un framework harmonisé FDA/EMA/PMDA pour les principes actifs. L’extension de ces principes aux produits finis stériles (ICH Q7A proposé) harmoniserait les exigences de stérilisation terminale. Les chapitres généraux des pharmacopées (USP, Ph. Eur., JP) s’alignent progressivement via le Pharmacopoeial Discussion Group (PDG), réduisant les divergences techniques.
PIC/S, regroupant 58 autorités réglementaires (2024), promeut l’uniformité des inspections GMP et la reconnaissance mutuelle des certifications. Un site pharmaceutique inspecté selon standards PIC/S est reconnu par toutes les autorités membres, éliminant les inspections redondantes et réduisant les barrières commerciales.
La révision WHO Technical Report Series No. 961 Annex 6 (Sterile Pharmaceutical Products) fournit des guidelines pour les marchés émergents (Afrique, Asie, Amérique Latine) ne disposant pas de frameworks réglementaires sophistiqués. L’adoption de ces standards WHO facilite l’accès aux médicaments essentiels stériles dans les régions sous-desservies.
Les standards ISO (17665, 11137, 11135, 14937) constituent la base technique internationale transcendant les juridictions. Leur référencement par les régulations nationales (FDA Standards Recognition Program, EU harmonized standards) crée une convergence de facto. Les futurs efforts viseront l’harmonisation complète des méthodes de validation, critères d’acceptation, et formats de documentation, réalisant la vision d’une « Global Pharmaceutical Sterilization Standard » unique.
CONCLUSION
L’autoclave dans l’industrie pharmaceutique incarne bien plus qu’un simple équipement technique. Il représente la matérialisation physique de l’engagement fondamental de l’industrie envers la sécurité des patients et la qualité des produits. Chaque cycle de stérilisation, exécuté selon des protocoles rigoureux validés, constitue une barrière critique entre les micro-organismes pathogènes et les millions de patients dépendant des médicaments stériles pour leur survie et leur bien-être.
La sophistication croissante des autoclaves pharmaceutiques modernes – intégrant digitalisation, automation, analytics prédictifs, et sustainability – reflète l’évolution continue d’une technologie centenaire pour répondre aux défis du 21ème siècle. Les autoclaves d’aujourd’hui, pilotés par des systèmes informatiques complexes, moniteurs en temps réel par des réseaux de capteurs IoT, et validés selon des standards scientifiques rigoureux, auraient été inimaginables il y a seulement deux décennies.
Toutefois, malgré ces avancées technologiques impressionnantes, les principes fondamentaux demeurent inchangés : température, temps, vapeur de qualité. Cette continuité rassure. Elle démontre que la stérilisation par autoclave, basée sur des lois physiques immuables, conserve sa pertinence face aux évolutions réglementaires, aux innovations thérapeutiques, et aux transformations industrielles.
Les défis futurs – sustainability environnementale, harmonisation réglementaire globale, intégration digitale, et émergence de thérapies avancées (cell & gene therapies) nécessitant des approches de stérilisation innovantes – stimuleront l’innovation continue. Les fabricants d’autoclaves, les ingénieurs de validation, les régulateurs, et les professionnels pharmaceutiques collaboreront pour développer les solutions de demain, garantissant que la stérilisation par autoclave reste le gold standard pendant les décennies à venir.
L’autoclave pharmaceutique, pilier méconnu mais indispensable, continuera silencieusement son travail critique : protéger la santé publique, lot après lot, cycle après cycle, avec une fiabilité et une efficacité inégalées. Son importance ne saurait être surestimée dans un monde où les infections nosocomiales causent des centaines de milliers de décès annuels, et où chaque médicament injectable administré doit être absolument exempt de contamination microbienne. L’autoclave, gardien invisible de notre sécurité sanitaire, mérite reconnaissance et respect.
Sources principales :
OTOSCOPE WELCH ALLYN MACROVIEW
CYCLES AUTOCLAVE SUR SMARTPHONE