Blog
LA CLASSIFICATION DE SPAULDING EN CHIRURGIE : UN PILIER ESSENTIEL DE LA PRÉVENTION DES INFECTIONS
Introduction
En 1957, le Dr Earle H. Spaulding révolutionna le domaine de la prévention des infections nosocomiales en proposant une approche rationnelle pour la désinfection et la stérilisation des dispositifs médicaux. Cette classification, aujourd’hui universellement reconnue sous le nom de « Classification de Spaulding », constitue l’un des piliers fondamentaux de la sécurité des patients dans les établissements de santé du monde entier.
La pertinence de cette classification réside dans sa logique claire et intuitive : elle catégorise les dispositifs médicaux selon le risque d’infection qu’ils présentent lors de leur utilisation. Après plus de six décennies, ce système demeure d’une actualité saisissante, témoignant de la vision avant-gardiste de son créateur. Les Centers for Disease Control and Prevention (CDC) américains, la Food and Drug Administration (FDA), l’Organisation mondiale de la santé (OMS), ainsi que les organismes de réglementation européens ont tous adopté et intégré cette classification dans leurs directives officielles.
L’importance cruciale de cette approche se manifeste dans les chiffres alarmants des infections nosocomiales : aux États-Unis, environ 2 millions de patients contractent annuellement une infection associée aux soins, entraînant près de 80 000 décès. En Europe, plus de 9 millions d’infections nosocomiales surviennent chaque année. Au Japon, grâce à une application rigoureuse de ces principes, le taux d’infections du site opératoire a considérablement diminué, passant de 10% dans les années 2000 à 5% en 2020.
Chapitre 1 : Fondements de la Classification de Spaulding
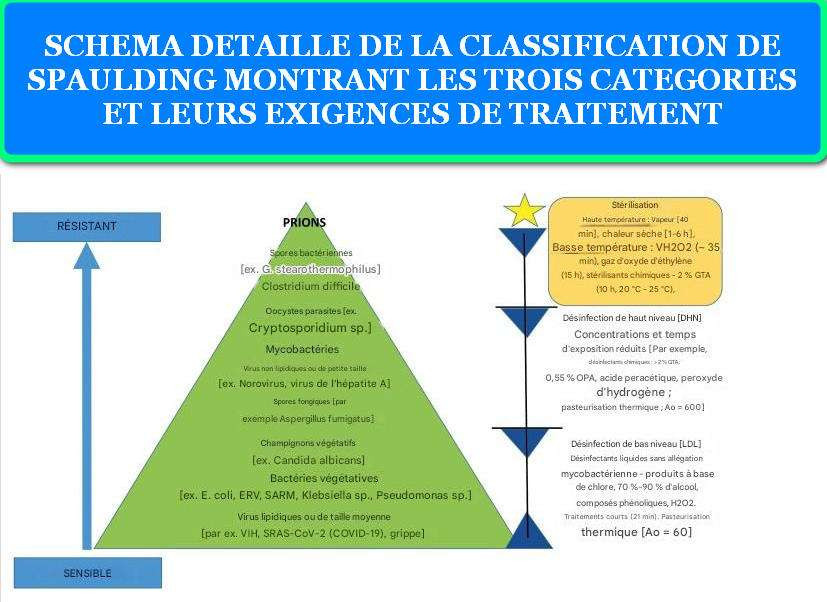
La classification de Spaulding repose sur un principe fondamental : le niveau de risque infectieux d’un dispositif médical est directement corrélé au type de tissu avec lequel il entre en contact. Cette approche scientifique divise l’ensemble des dispositifs médicaux en trois catégories distinctes, chacune nécessitant un niveau spécifique de décontamination.
Les Trois Catégories Principales
1. Dispositifs Critiques : Ces instruments présentent un risque élevé d’infection car ils pénètrent dans les tissus stériles ou le système vasculaire. Toute contamination microbienne peut entraîner une transmission pathogène directe. Cette catégorie exige une stérilisation complète, éliminant tous les micro-organismes, y compris les spores bactériennes résistantes.
2. Dispositifs Semi-critiques : Ces équipements entrent en contact avec les muqueuses ou la peau non intacte. Bien que les muqueuses soient généralement résistantes aux spores bactériennes communes, elles demeurent sensibles aux bactéries végétatives, mycobactéries et virus. Une désinfection de haut niveau est requise pour ces dispositifs.
3. Dispositifs Non-critiques : Ces objets ne touchent que la peau intacte, qui constitue une barrière efficace contre la plupart des micro-organismes. Une désinfection de niveau intermédiaire ou bas suffit généralement pour ces dispositifs.
Principes Scientifiques et Microbiologiques
La classification s’appuie sur une compréhension approfondie de la résistance microbienne. Les micro-organismes présentent des niveaux de résistance variables aux agents désinfectants et stérilisants. Les spores bactériennes, notamment celles de Bacillus et Clostridium, constituent les formes les plus résistantes, nécessitant des procédés de stérilisation intense. À l’inverse, les virus enveloppés et les bactéries végétatives sont généralement plus sensibles aux désinfectants.
Cette hiérarchie de résistance microbienne établit un ordre croissant : virus enveloppés < bactéries végétatives < champignons < virus non-enveloppés < mycobactéries < spores bactériennes. Cette gradation guide directement le choix des méthodes de décontamination selon la catégorie Spaulding du dispositif.
Niveaux d’Activité Germicide
Spaulding a également identifié trois niveaux d’activité germicide correspondant aux exigences de chaque catégorie :
- Niveau élevé (Stérilisation) : Destruction de tous les micro-organismes, incluant les spores bactériennes. Temps d’exposition prolongé et conditions strictes.
- Niveau intermédiaire (Désinfection de haut niveau) : Élimination de tous les micro-organismes excepté les spores bactériennes en petit nombre. Efficace contre mycobactéries, virus et champignons.
- Niveau faible (Désinfection de niveau bas à intermédiaire) : Destruction des bactéries végétatives, certains champignons et virus enveloppés. Inefficace contre les spores et mycobactéries résistantes.
Chapitre 2 : Dispositifs Critiques
Les dispositifs critiques représentent la catégorie la plus exigeante de la classification de Spaulding. Leur contact direct avec les tissus stériles, le système vasculaire ou les cavités corporelles normalement stériles impose une stérilisation absolue. Toute contamination microbienne, même minime, peut entraîner des conséquences dramatiques : septicémie, endocardite, infections profondes ou décès du patient.
Définition Détaillée et Exemples Précis
Les dispositifs critiques englobent une vaste gamme d’instruments et d’équipements médicaux. Les instruments chirurgicaux constituent l’exemple le plus évident : scalpels, pinces, ciseaux, écarteurs, implants orthopédiques, prothèses cardiaques et matériel de suture. Ces outils pénètrent directement dans les tissus stériles lors des interventions chirurgicales.
Les cathéters représentent une autre catégorie majeure : cathéters cardiaques pour cathétérisme cardiaque, cathéters veineux centraux, cathéters urinaires, sondes endotrachéales et cathéters de dialyse. Ces dispositifs créent un accès direct au système circulatoire ou aux organes internes, contournant les barrières naturelles de l’organisme.
Les implants médicaux, permanents ou temporaires, nécessitent également une stérilisation parfaite : prothèses articulaires, stimulateurs cardiaques, défibrillateurs implantables, stents vasculaires, matériel d’ostéosynthèse et dispositifs intraoculaires. Leur insertion dans l’organisme et leur contact prolongé avec les tissus internes exigent une absence totale de contamination microbienne.

Méthodes de Stérilisation Obligatoires
Stérilisation à la Vapeur (Autoclavage) : Cette méthode demeure la référence gold standard pour les dispositifs thermostables. L’autoclave génère de la vapeur d’eau saturée sous pression, atteignant des températures de 121°C à 134°C. Le processus combine trois facteurs synergiques : température élevée, humidité et pression. Les cycles typiques durent 15 à 30 minutes selon la température et la charge. Cette méthode présente l’avantage d’être économique, rapide, non toxique et hautement efficace contre tous les micro-organismes.
Stérilisation à l’Oxyde d’Éthylène (EtO) : Réservée aux dispositifs thermosensibles, cette méthode utilise un gaz alkylant qui détruit les micro-organismes en modifiant leur ADN et leurs protéines. Le processus s’effectue à basse température (37-63°C) mais nécessite des temps de cycle prolongés (2-24 heures) et des phases d’aération pour éliminer les résidus toxiques. L’EtO pénètre efficacement les matériaux poreux et les emballages, mais requiert des installations spécialisées et une surveillance stricte des résidus.
Stérilisation au Peroxyde d’Hydrogène en Phase Plasma : Cette technologie moderne utilise le peroxyde d’hydrogène vaporisé activé par radiofréquence pour créer un plasma à basse température. Le processus génère des radicaux libres hautement réactifs qui détruisent les micro-organismes. Cette méthode présente l’avantage d’être rapide (45-75 minutes), non toxique et compatible avec les dispositifs électroniques sensibles.
Stérilisants Chimiques Liquides : Utilisés pour les dispositifs ne supportant ni la chaleur ni les autres méthodes, ces produits incluent le glutaraldéhyde à 2,4%, l’acide peracétique à 0,2%, et le peroxyde d’hydrogène à 7,5%. Ces agents nécessitent une immersion complète, un temps de contact prolongé (3-12 heures) et un rinçage stérile minutieux.
Protocoles de Validation et Contrôle de Routine
La validation des procédés de stérilisation constitue une exigence réglementaire fondamentale. Elle comprend trois phases distinctes : la qualification d’installation (QI), la qualification opérationnelle (QO) et la qualification de performance (QP). La QI vérifie l’installation correcte de l’équipement selon les spécifications. La QO confirme le fonctionnement conforme de tous les systèmes. La QP démontre l’efficacité stérilisante dans les conditions d’utilisation réelles.
Le contrôle de routine s’appuie sur trois types d’indicateurs complémentaires. Les indicateurs physiques (température, pression, temps) confirment le respect des paramètres de cycle. Les indicateurs chimiques changent de couleur ou d’aspect lors de l’exposition aux conditions de stérilisation. Les indicateurs biologiques, contenant des spores de Geobacillus stearothermophilus pour la vapeur ou Bacillus atrophaeus pour l’EtO, représentent le test le plus rigoureux de l’efficacité stérilisante.
Chapitre 3 : Dispositifs Semi-critiques
Les dispositifs semi-critiques occupent une position intermédiaire dans la classification de Spaulding, présentant des défis uniques en matière de décontamination. Leur contact avec les muqueuses ou la peau non intacte nécessite une désinfection de haut niveau (DHN) plutôt qu’une stérilisation complète, tout en maintenant un niveau de sécurité élevé pour le patient.
Définition et Caractéristiques
Les muqueuses, bien qu’elles constituent une barrière protectrice, sont plus perméables que la peau intacte et présentent une sensibilité particulière à certains micro-organismes. Les bactéries végétatives, les mycobactéries, les champignons et les virus peuvent franchir cette barrière et causer des infections. Cependant, les spores bactériennes sont généralement moins préoccupantes car les muqueuses saines possèdent des mécanismes de défense efficaces contre ces formes résistantes.
Exemples Détaillés de Dispositifs Semi-critiques
Endoscopes flexibles : Ces instruments sophistiqués représentent l’exemple le plus complexe de la catégorie semi-critique. Les gastroscopes, colonoscopes, bronchoscopes et duodénoscopes possèdent des canaux internes étroits, des optiques délicates et des composants électroniques sensibles. Leur design complexe avec des angles droits, des surfaces rugueuses et des espaces difficiles d’accès complique considérablement le processus de décontamination.
Équipements d’anesthésie et de ventilation : Les circuits respiratoires, masques faciaux, sondes d’intubation réutilisables et équipements de ventilation entrent en contact direct avec les voies respiratoires. Leur contamination peut entraîner des pneumonies nosocomiales, particulièrement préoccupantes chez les patients immunocompromis.
Instruments d’examen spécialisés : Les laryngoscopes, cystoscopes, hystéroscopes, arthroscopes et spéculums vaginaux nécessitent une DHN rigoureuse. Leurs surfaces peuvent être contaminées par des sécrétions corporelles contenant des pathogènes opportunistes.

Désinfection de Haut Niveau : Agents et Protocoles
Glutaraldéhyde (≥2,4%) : Cet aldéhyde reste l’agent de référence pour la DHN depuis plusieurs décennies. Sa formulation stabilisée maintient une efficacité optimale pendant 14 à 28 jours selon la concentration et les conditions d’utilisation. Le temps de contact minimal est de 20 minutes à température ambiante, réduit à 5 minutes à 35°C dans certains systèmes automatisés validés. Le glutaraldéhyde présente une excellente activité contre tous les micro-organismes pathogènes, incluant les mycobactéries résistantes et les virus non-enveloppés.
Peroxyde d’hydrogène (7,5%) : Cette solution oxydante démontre une efficacité rapide avec un temps de contact de 6 minutes à température ambiante. Son mécanisme d’action repose sur la formation de radicaux libres qui endommagent les structures cellulaires microbiennes. L’avantage principal réside dans l’absence de résidus toxiques, se décomposant en eau et oxygène.
Acide peracétique (0,2%) : Cet agent sporocide puissant agit en 5 minutes à température ambiante. Sa formulation stabilisée avec des inhibiteurs de corrosion le rend compatible avec la plupart des matériaux médicaux. L’acide peracétique présente l’avantage d’être efficace en présence de matières organiques résiduelles.
Ortho-phtalaldéhyde (OPA) : Ce désinfectant de nouvelle génération offre plusieurs avantages par rapport au glutaraldéhyde : absence d’activation préalable, stabilité supérieure, temps de contact réduit (5 minutes à 25°C) et compatibilité matérielle excellente. Cependant, son coût plus élevé et sa tendance à colorer les surfaces en gris limitent parfois son utilisation.
Problématiques Spécifiques des Endoscopes
Les endoscopes flexibles présentent des défis particuliers qui ont conduit à plusieurs épidémies d’infections nosocomiales documentées. Entre 2013 et 2015, les duodénoscopes ont été impliqués dans au moins 9 épidémies causées par des bactéries multirésistantes aux États-Unis, affectant plus de 200 patients malgré le respect apparent des protocoles de retraitement.
Ces incidents ont révélé les limites de la DHN pour certains endoscopes complexes. Les mécanismes d’élévateur des duodénoscopes, en particulier, créent des espaces difficilement accessibles où peuvent persister des biofilms microbiens résistants. Cette problématique a conduit certains experts à proposer une reclassification des duodénoscopes de la catégorie semi-critique vers critique, impliquant une stérilisation systématique.
Chapitre 4 : Dispositifs Non-critiques
Les dispositifs non-critiques constituent la catégorie la plus vaste et la moins risquée de la classification de Spaulding. Leur contact exclusif avec la peau intacte, barrière naturelle efficace contre la plupart des micro-organismes, permet des protocoles de décontamination simplifiés tout en maintenant la sécurité des patients.
Définition et Principe Fondamental
La peau intacte représente la première ligne de défense de l’organisme contre les infections. Sa structure cornée, son pH acide, sa flore commensale et ses mécanismes de desquamation naturelle créent un environnement hostile pour la plupart des pathogènes. Cette efficacité protectrice justifie les exigences de décontamination réduites pour les dispositifs non-critiques.
Cependant, cette catégorie se subdivise en deux sous-groupes distincts selon les directives du CDC : les dispositifs de soins aux patients et les surfaces environnementales. Cette distinction reflète des niveaux de risque et des fréquences de contact variables.
Exemples de Dispositifs Non-critiques
Dispositifs de soins directs : Les tensiomètres, stéthoscopes, thermomètres non invasifs, béquilles, déambulateurs et oxymètres de pouls entrent en contact direct mais superficiel avec la peau des patients. Bien que le risque infectieux soit minimal, ces dispositifs peuvent servir de vecteurs de transmission croisée entre patients s’ils ne sont pas correctement décontaminés.
Équipements de support : Les bassins de lit, urinoirs, tables de consultation, chaises roulantes et lits d’hôpital constituent des surfaces de contact prolongé. Leur contamination par des sécrétions corporelles peut créer des réservoirs microbiens, particulièrement préoccupants dans les unités accueillant des patients immunodéprimés.
Surfaces environnementales : Les poignées de porte, rampes d’escalier, surfaces de travail, téléphones, ordinateurs et interrupteurs représentent des surfaces fréquemment touchées. Leur rôle dans la transmission indirecte d’infections par contamination des mains du personnel soignant ou des patients est désormais bien documenté.

Protocoles de Désinfection
Désinfection de niveau intermédiaire : Recommandée pour les dispositifs présentant un risque accru de contamination par des pathogènes résistants. Les composés phénoliques, les solutions d’hypochlorite de sodium (500-5000 ppm), l’alcool isopropylique (70%) et les composés d’ammonium quaternaire constituent les agents de référence. Ces produits éliminent efficacement les bactéries végétatives, la plupart des virus et champignons en 1-10 minutes de contact.
Désinfection de niveau bas : Suffisante pour les surfaces à faible risque de contamination. Les solutions d’alcool à 70%, les composés d’ammonium quaternaire dilués et certains produits phénoliques à faible concentration offrent une décontamination adéquate en 30-60 secondes d’exposition.
Protocoles de Nettoyage Environnemental
Le nettoyage environnemental hospitalier suit des protocoles structurés visant à prévenir la contamination croisée. Les surfaces sont classées selon leur fréquence de contact : surfaces fréquemment touchées (nettoyage quotidien minimum), surfaces occasionnellement touchées (nettoyage hebdomadaire) et surfaces rarement touchées (nettoyage selon besoin).
La méthodologie « de propre vers sale » et « de haut vers bas » minimise la redistribution des contaminants. L’utilisation de lingettes imprégnées à usage unique ou de systèmes de nettoyage à microfibre avec solutions désinfectantes appropriées garantit l’efficacité du processus.
Chapitre 5 : Application en Europe
L’Europe présente un paysage réglementaire harmonisé mais nuancé dans l’application de la classification de Spaulding. Chaque pays membre a développé ses propres spécificités tout en respectant les directives européennes communes, créant un ensemble cohérent de pratiques de haute qualité.
France : Excellence et Rigueur Réglementaire
La France a développé un cadre réglementaire particulièrement rigoureux pour la stérilisation des dispositifs médicaux. La Société Française des Sciences de la Stérilisation (SF2S) et la Société Française d’Hygiène Hospitalière (SF2H) publient régulièrement des guides de bonnes pratiques faisant référence au niveau international.
Le « Guide de bonnes pratiques de traitement des dispositifs médicaux réutilisables » de la SF2H, dans sa version 2022, constitue la référence nationale. Ce document de 400 pages détaille l’application de la classification de Spaulding selon les normes européennes EN ISO 17665 (stérilisation à la vapeur), EN ISO 11135 (stérilisation à l’oxyde d’éthylène) et EN ISO 11137 (stérilisation par irradiation).
L’organisation française des services de stérilisation suit le modèle des Unités de Stérilisation Centrale (USC), centralisées au niveau régional ou hospitalier. L’Assistance Publique-Hôpitaux de Paris (AP-HP), premier centre hospitalier universitaire européen, a développé des protocoles exemplaires. Ses 39 hôpitaux appliquent des procédures standardisées traitant plus de 2 millions d’instruments par mois selon la classification de Spaulding.
La réglementation française impose une traçabilité complète des dispositifs critiques et semi-critiques. Chaque instrument doit être identifié, son cycle de retraitement documenté et sa libération autorisée par un pharmacien hospitalier qualifié. Cette exigence, unique en Europe, garantit une sécurité maximale mais impose des contraintes logistiques importantes.
Allemagne : Précision Technique et Innovation
L’Allemagne applique la classification de Spaulding selon les normes DIN (Deutsche Industrie Norm) transposées des standards ISO européens. Le Robert Koch Institute (RKI), équivalent allemand du CDC américain, publie des recommandations détaillées pour l’application des protocoles de décontamination.
Les hôpitaux allemands se distinguent par l’adoption précoce de technologies innovantes. Les systèmes de stérilisation flash (rapid sterilization) sont largement utilisés pour les urgences chirurgicales, avec des cycles vapeur de 3-4 minutes à 134°C pour les instruments non emballés. Cette pratique, encadrée par des protocoles stricts, optimise l’efficacité opérationnelle.
La certification ISO 13485:2016 (systèmes qualité pour dispositifs médicaux) est systématiquement exigée pour tous les services de stérilisation hospitaliers. Cette certification, renouvelée annuellement, couvre l’ensemble de la chaîne de retraitement : collecte, nettoyage, contrôle, conditionnement, stérilisation, stockage et distribution.
L’Allemagne a également développé des systèmes de traçabilité électronique avancés, utilisant des puces RFID pour suivre chaque instrument depuis sa fabrication jusqu’à son utilisation clinique. Cette approche technologique, intégrée dans les systèmes d’information hospitaliers, permet une gestion optimisée des stocks et une traçabilité parfaite en cas d’incident.
Royaume-Uni : Standards NHS et Accréditation
Le National Health Service (NHS) britannique a élaboré des directives spécifiques pour l’application de la classification de Spaulding dans ses 1 200 établissements. Les « Guidelines for Decontamination » du Department of Health constituent le référentiel national, actualisé régulièrement pour intégrer les évolutions technologiques et épidémiologiques.
Le système britannique privilégie l’accréditation par des organismes tiers indépendants. L’Institute of Decontamination Sciences (IDSc) certifie les techniciens et superviseurs selon des standards rigoureux. Cette certification, obligatoire pour les postes de responsabilité, garantit la compétence professionnelle et la mise à jour des connaissances.
Les audits qualité sont systématiques et inopinés. La Care Quality Commission (CQC) inspecte régulièrement les services de stérilisation, avec des sanctions pouvant aller jusqu’à la fermeture temporaire en cas de non-conformités majeures. Cette approche réglementaire stricte maintient un niveau élevé de sécurité sanitaire.
Le Royaume-Uni a également développé des centres de stérilisation régionaux ultra-modernes, mutualisant les moyens pour plusieurs établissements. Ces plateformes industrielles, certifiées ISO 13485 et ISO 14001 (environnement), traitent quotidiennement des dizaines de milliers d’instruments selon la classification de Spaulding.
Chapitre 6 : Application au Japon
Le Japon représente un modèle d’excellence dans l’application de la classification de Spaulding, conjuguant tradition de qualité, innovation technologique et culture de la sécurité du patient. L’évolution remarquable des taux d’infections nosocomiales japonais témoigne de l’efficacité de cette approche systémique.
Japanese Nosocomial Infections Surveillance (JNIS)
Établi en 1998 par la Japanese Society for Environmental Infections (JSEI), le système JNIS constitue le plus vaste réseau de surveillance des infections nosocomiales en Asie. Ce système collecte des données de plus de 400 hôpitaux, représentant plus de 200 000 lits et 2 millions de patients annuels.
Les résultats du JNIS démontrent une amélioration spectaculaire : le taux global d’infections du site opératoire a chuté de 10,2% dans les années 2000 à 7,1% en 2007, puis à 5,2% en 2020. Cette progression reflète l’application rigoureuse de la classification de Spaulding et l’amélioration continue des protocoles de décontamination.
Standards GS1 et Traçabilité Avancée
Le Japon a révolutionné la gestion des instruments chirurgicaux en adoptant massivement les standards GS1 (Global Standards One). L’Université de Fukui Hospital a développé un système de gestion intégré utilisant les codes DataMatrix pour identifier chaque instrument individuel.
Ce système lie l’identité du patient, le planning opératoire et les informations instrumentales dans une base de données centralisée. Chaque instrument porte un marquage permanent DataMatrix gravé au laser, résistant aux cycles de stérilisation répétés. Cette traçabilité permet un suivi complet depuis la fabrication jusqu’à l’utilisation clinique.
Exemples Concrets d’Excellence
Université d’Osaka Hospital : Cet établissement de 1 086 lits a obtenu la certification ISO 13485:2016 pour son département de stérilisation centrale. L’hôpital traite quotidiennement plus de 3 000 instruments selon des protocoles stricts basés sur la classification de Spaulding. Leur taux d’infections nosocomiales (2,1%) figure parmi les plus bas mondialement.
Université de Tokyo Hospital : Le Central Supply Service de cet hôpital universitaire a développé des protocoles innovants intégrant nettoyage automatisé, désinfection contrôlée, conditionnement sous atmosphère protectrice et stérilisation validée. Leur système de double contrôle qualité (physique et biologique) garantit une libération sécurisée des charges.
Tokushima University Hospital : Pionnier dans l’utilisation de la robotique pour le tri et la préparation des instruments, cet établissement a automatisé 70% de ses processus de retraitement. L’intégration de capteurs IoT (Internet of Things) permet un monitoring en temps réel des paramètres de stérilisation.
Culture Qualité et Sécurité Patient
La culture japonaise du « Kaizen » (amélioration continue) imprègne profondément les pratiques de stérilisation. Les équipes organisent des cercles qualité hebdomadaires pour analyser les incidents, optimiser les procédures et partager les bonnes pratiques. Cette approche participative responsabilise chaque acteur et maintient un niveau d’excellence constant.
La formation du personnel suit des standards rigoureux établis par la Japanese Association for Infection Prevention and Control (JAIPC). Les techniciens doivent valider des modules théoriques et pratiques, renouvelés tous les trois ans. Cette certification professionnelle garantit la compétence et la mise à jour des connaissances.

Chapitre 7 : Application aux États-Unis
Les États-Unis, berceau de la classification de Spaulding, ont développé le cadre réglementaire le plus complet au monde pour son application. Les directives du CDC et les standards de la FDA constituent la référence internationale, influençant les pratiques de décontamination dans tous les pays développés.
Cadre Réglementaire Federal : CDC et FDA
Le « Guideline for Disinfection and Sterilization in Healthcare Facilities (2008) » du CDC reste le document de référence mondial. Cette directive de 158 pages détaille l’application de la classification de Spaulding pour chaque catégorie de dispositifs, intégrant les évolutions technologiques et épidémiologiques des cinquante dernières années.
La FDA (Food and Drug Administration) régule les dispositifs médicaux selon une classification parallèle (Classes I, II, III) mais complémentaire à celle de Spaulding. Les Class II et III devices nécessitent une validation préalable à la mise sur le marché (510(k) ou PMA), incluant la démonstration de l’efficacité des protocoles de décontamination recommandés.
Standards AAMI et Reconnaissance FDA
L’Association for the Advancement of Medical Instrumentation (AAMI) développe les standards techniques reconnus par la FDA. Les normes ANSI/AAMI ST79 (steam sterilization), ST58 (chemical indicators), et ST55 (table-top steam sterilizers) constituent les références techniques nationales.
Ces standards évoluent régulièrement pour intégrer les innovations technologiques. La révision 2017 d’ANSI/AAMI ST79 a ainsi intégré les nouvelles technologies de monitoring biologique en temps réel et les systèmes de traçabilité électronique.
Recommandations Spécifiques par Catégorie
Dispositifs Critiques : Le CDC recommande prioritairement la stérilisation vapeur pour tous les dispositifs thermostables, en raison de sa « plus grande marge de sécurité due à sa fiabilité, constance et létalité ». Les cycles flash sont autorisés uniquement pour les urgences chirurgicales, avec des restrictions strictes d’utilisation.
Validation des Procédés : Chaque nouveau dispositif ou modification de procédé nécessite une validation complète selon les standards FDA. Cette validation comprend des tests de résistance thermique microbienne, de pénétration stérilisante et de sécurité matérielle sur des cycles répétés.
Contrôle Qualité Biologique : Les indicateurs biologiques doivent être utilisés quotidiennement pour les stérilisateurs vapeur et à chaque charge pour les méthodes alternatives (EtO, H2O2). Les spores de référence (Geobacillus stearothermophilus pour vapeur, Bacillus atrophaeus pour EtO) sont fournies par des laboratoires certifiés FDA.
Évolutions Réglementaires Depuis 1981
Le tableau original du CDC de 1981 a subi six modifications majeures reflétant les progrès scientifiques et technologiques. L’élimination du formaldéhyde-alcool (toxicité excessive), l’ajout du peroxyde d’hydrogène et de l’acide peracétique (efficacité supérieure), et la suppression des phénoliques et iodophores comme désinfectants de haut niveau (efficacité insuffisante contre certains pathogènes) illustrent cette évolution continue.
La révision 2019 a intégré de nouveaux pathogènes préoccupants : Clostridium difficile, Candida auris, et les coronavirus émergents. Ces ajouts reflètent l’adaptation permanente de la classification aux défis épidémiologiques contemporains.
Exemples Institutionnels d’Excellence
Mayo Clinic : Cette institution de renommée mondiale a développé des protocoles de stérilisation exemplaires dans ses trois campus (Minnesota, Floride, Arizona). Leur Central Sterile Supply Department traite plus de 40 000 instruments hebdomadaires avec un taux de non-conformité inférieur à 0,01%. Leur système de traçabilité RFID permet un suivi en temps réel de chaque dispositif.
Johns Hopkins Hospital : Pionnier dans la validation des nouveaux procédés de stérilisation, cet hôpital universitaire collabore avec la FDA pour évaluer les technologies émergentes. Leur laboratoire de recherche en stérilisation teste annuellement plus de 50 nouveaux dispositifs médicaux selon les protocoles Spaulding.
Cleveland Clinic : Leader dans l’automatisation des processus de retraitement, cette institution a développé des systèmes robotisés intégrant intelligence artificielle pour l’optimisation des cycles de stérilisation. Leur approche prédictive réduit de 30% les temps de retraitement tout en maintenant la sécurité maximale.
Chapitre 8 : Normes Internationales
L’harmonisation internationale des pratiques de stérilisation repose sur un ensemble cohérent de normes ISO (International Organization for Standardization) qui traduisent les principes de Spaulding en exigences techniques précises. Ces standards facilitent les échanges commerciaux et garantissent un niveau de sécurité homogène à l’échelle mondiale.
ISO 17665 : Stérilisation à la Chaleur Humide
La norme ISO 17665:2006, révisée en 2024, constitue la référence mondiale pour la stérilisation vapeur. Elle spécifie les exigences pour le développement, la validation et le contrôle de routine des procédés de stérilisation des dispositifs médicaux par chaleur humide. Cette norme s’applique aux stérilisateurs de toutes tailles, des autoclaves de laboratoire aux installations industrielles.
Les exigences de validation comprennent trois phases distinctes : qualification de l’installation (QI), qualification opérationnelle (QO) et qualification de performance (QP). La QI vérifie la conformité de l’installation aux spécifications techniques. La QO confirme le fonctionnement correct de tous les systèmes. La QP démontre l’efficacité stérilisante dans les conditions d’utilisation réelles avec la charge la plus défavorable.
| Température | Temps minimum | Applications typiques |
|---|---|---|
| 121°C | 15 minutes | Instruments simples, milieux de culture |
| 134°C | 3 minutes | Instruments chirurgicaux emballés, textiles |
| 138°C | 18 secondes | Cycles flash pour urgences |
ISO 11137 : Stérilisation par Irradiation
Cette norme tripartite (11137-1, 11137-2, 11137-3) régit la stérilisation par rayonnements ionisants, méthode privilégiée pour les dispositifs à usage unique thermosensibles. L’irradiation gamma (Cobalt-60), les faisceaux d’électrons accélérés et les rayons X constituent les trois technologies validées.
La détermination de la dose stérilisante suit deux approches complémentaires. La Méthode 1 établit la dose à partir de la charge microbienne initiale (bioburden) du produit. La Méthode 2 utilise des doses standardisées (15, 25 ou 50 kGy) validées pour des catégories de produits spécifiques. Le Niveau d’Assurance de Stérilité (SAL) requis de 10^-6 garantit moins d’une chance sur un million qu’un micro-organisme viable survive au traitement.
ISO 11135 : Stérilisation à l’Oxyde d’Éthylène
Révisée en 2014, cette norme encadre la stérilisation par oxyde d’éthylène (EtO) pour les dispositifs thermosensibles. L’EtO présente un excellent pouvoir de pénétration dans les matériaux poreux et les emballages complexes, mais nécessite des précautions particulières en raison de sa toxicité et de ses propriétés cancérigènes.
Les paramètres critiques comprennent la concentration en EtO (450-1200 mg/L), la température (37-63°C), l’humidité relative (45-85%) et le temps d’exposition (1-24 heures selon les conditions). La phase d’aération post-stérilisation élimine les résidus toxiques selon les limites définies par l’ISO 10993-7 : 25 ppm d’EtO et 250 ppm de chlorhydrine d’éthylène pour les dispositifs en contact permanent avec le patient.
ISO 14937 : Critères Généraux de Caractérisation
Cette norme transversale établit les principes généraux pour la caractérisation d’un agent stérilisant et le développement, la validation et le contrôle de routine d’un procédé de stérilisation. Elle s’applique à toutes les technologies de stérilisation, incluant les méthodes émergentes comme le peroxyde d’hydrogène vaporisé, l’ozone et les radiations ultraviolettes.
Les critères d’efficacité microbicide doivent être démontrés contre un spectre représentatif de micro-organismes : bactéries végétatives, spores bactériennes, champignons, levures et virus. La norme définit également les exigences de sécurité matérielle, de résidus toxiques et d’impact environnemental.
EN 556-1 : Exigences pour Dispositifs Stériles
Cette norme européenne, adoptée par 34 pays, spécifie les exigences pour qu’un dispositif médical puisse être étiqueté « STÉRILE ». Elle établit deux conditions impératives : la probabilité de présence d’un micro-organisme viable doit être inférieure ou égale à 10^-6, et cette performance doit être documentée par des preuves scientifiques valides.
L’étiquetage « STÉRILE » implique des responsabilités légales pour le fabricant, incluant la traçabilité complète du processus, la maintenance de la stérilité jusqu’à l’utilisation, et la déclaration des conditions de stockage et d’utilisation. Cette norme constitue la base réglementaire pour la libre circulation des dispositifs médicaux stériles en Europe.
Chapitre 9 : Défis Contemporains
Soixante-cinq ans après sa conception, la classification de Spaulding fait face à des défis inédits qui questionnent certains de ses postulats originels. L’émergence de nouveaux pathogènes, l’évolution des pratiques médicales et la complexification technologique imposent une adaptation continue de cette approche fondamentale.
Émergence de Pathogènes Résistants (MDROs)
Les micro-organismes multirésistants aux antibiotiques (MDROs) représentent une menace croissante pour la sécurité des patients. Candida auris, champignon émergent identifié en 2009, présente une résistance exceptionnelle aux désinfectants usuels et persiste plusieurs mois sur les surfaces environnementales. Les épidémies nosocomiales causées par ce pathogène ont révélé l’insuffisance des protocoles de désinfection traditionnels pour les dispositifs non-critiques.
Clostridium difficile, producteur de spores particulièrement résistantes, nécessite des désinfectants sporocides (hypochlorite de sodium) plutôt que les désinfectants usuels à base d’alcool ou d’ammonium quaternaire. Cette exigence spécifique complique l’application uniforme des protocoles Spaulding dans les services à risque élevé.
Les bactéries hautement résistantes (BHRe) comme Klebsiella pneumoniae carbapénémase (KPC) ou Acinetobacter baumannii multirésistant survivent prolongément dans l’environnement hospitalier et résistent à de nombreux désinfectants. Leur dissémination via les dispositifs médicaux contaminés impose des protocoles renforcés dépassant parfois les recommandations Spaulding classiques.
Biofilms et Tolérance Adaptative
La formation de biofilms sur les surfaces des dispositifs médicaux constitue un défi majeur non anticipé lors de l’élaboration de la classification originelle. Ces structures tridimensionnelles, composées de micro-organismes enrobés dans une matrice polymérique, présentent une résistance 10 à 1000 fois supérieure aux désinfectants comparativement aux cellules planctoniques.
Les endoscopes flexibles, avec leurs canaux internes étroits et leurs surfaces rugueuses, favorisent particulièrement la formation de biofilms. Les investigations post-épidémies ont révélé la persistance de biofilms de Pseudomonas aeruginosa, Enterobacter cloacae et mycobactéries atypiques malgré l’application rigoureuse des protocoles de désinfection de haut niveau.
La tolérance adaptative, phénomène par lequel les micro-organismes développent une résistance temporaire aux stress environnementaux, complique davantage la situation. Les bactéries exposées de façon sub-léthale aux désinfectants peuvent acquérir une tolérance accrue, réduisant l’efficacité des traitements ultérieurs.
Complexité Croissante des Dispositifs Médicaux
L’évolution technologique a produit des dispositifs médicaux d’une complexité inimaginable en 1957. Les endoscopes modernes intègrent des fibres optiques, des composants électroniques, des capteurs miniaturisés et des mécanismes articulés créant de multiples espaces confinés difficiles d’accès pour les agents de décontamination.
Les robots chirurgicaux, instruments réutilisables de haute technologie, présentent des défis particuliers : thermosensibilité des composants électroniques, matériaux composites incompatibles avec certains désinfectants, géométries complexes empêchant la pénétration des agents stérilisants. Ces contraintes imposent des compromis entre sécurité microbiologique et préservation fonctionnelle.
Les dispositifs implantables temporaires (pompes à ballonnet intra-aortique, oxygénateurs extracorporels, dispositifs d’assistance ventriculaire) combinent contact avec les tissus stériles et composants électroniques sensibles. Leur classification Spaulding (critique) entre en conflit avec leurs limitations technologiques, nécessitant des approches alternatives.
Proposition de Reclassification des Endoscopes
Face aux épidémies récurrentes liées aux endoscopes, plusieurs experts proposent une reclassification des duodénoscopes et échoendoscopes de la catégorie semi-critique vers critique. Cette évolution majeure impliquerait une stérilisation systématique plutôt qu’une désinfection de haut niveau, augmentant significativement la marge de sécurité.
Les arguments en faveur de cette reclassification incluent : la complexité architecturale empêchant une décontamination efficace, les conséquences dramatiques des infections (mortalité de 40-50% pour les bactériémies à entérobactéries résistantes), l’insuffisance démontrée de la désinfection de haut niveau dans certaines configurations, et la disponibilité croissante de technologies de stérilisation basse température compatibles.
Cette proposition rencontre néanmoins des obstacles pratiques : coût économique de la stérilisation versus désinfection, durée prolongée des cycles de stérilisation impactant la disponibilité des équipements, compatibilité limitée de certains endoscopes avec les procédés de stérilisation, et résistance culturelle des professionnels habitués aux protocoles actuels.
Développement Durable et Approche « Quintuple Helix »
Les préoccupations environnementales croissantes questionnent la durabilité des pratiques de stérilisation actuelles. La consommation énergétique des autoclaves, l’utilisation d’agents chimiques potentiellement écotoxiques, la production de déchets contaminés et l’impact carbone des dispositifs à usage unique imposent une réflexion globale sur l’écologie de la décontamination.
L’approche « Quintuple Helix » propose une collaboration structurée entre cinq acteurs : académiques (recherche fondamentale), industriels (innovation technologique), professionnels de santé (expertise clinique), régulateurs (cadre normatif) et société civile (acceptabilité sociale). Cette synergie multisectorielle vise à développer des solutions de décontamination efficaces, sûres, économiques et durables.
Chapitre 10 : Meilleures Pratiques et Recommandations
L’application réussie de la classification de Spaulding repose sur un ensemble de meilleures pratiques éprouvées, fruit de décennies d’expérience clinique et de recherche scientifique. Ces recommandations constituent le socle d’un programme de décontamination sécurisé et efficace.
Importance Cruciale du Nettoyage Préalable
Le nettoyage constitue l’étape fondamentale, préalable obligatoire à toute désinfection ou stérilisation efficace. Cette phase élimine la charge microbienne, les résidus organiques et les particules susceptibles de protéger les micro-organismes contre l’action des agents biocides. L’adage « on ne stérilise que ce qui est propre » résume parfaitement cette exigence absolue.
Le nettoyage manuel nécessite une formation spécialisée du personnel et l’utilisation d’agents compatibles avec les matériaux des dispositifs. Les détergents enzymatiques, particulièrement efficaces contre les protéines sanguines, doivent être utilisés selon les concentrations et temps de contact recommandés. Le brossage mécanique, réalisé sous la surface du bain pour éviter les aérosolisations contaminantes, décroche les souillures adhérentes.
Le nettoyage automatisé, privilégié pour sa reproductibilité et sa sécurité, utilise des laveurs-désinfecteurs programmés selon des cycles validés. Ces équipements combinent action mécanique (jets sous pression), chimique (détergents spécialisés) et thermique (montées en température progressives) pour garantir un nettoyage optimal et une désinfection thermique préliminaire.
Validation Régulière des Procédés
La validation constitue un processus documenté établissant qu’un procédé produira de façon reproductible les résultats escomptés. Pour la stérilisation, cette validation comprend trois composantes : qualification de l’installation (conformité technique), qualification opérationnelle (fonctionnement nominal) et qualification de performance (efficacité stérilisante).
La revalidation périodique s’impose selon un calendrier prédéfini : annuelle pour les stérilisateurs vapeur, semestrielle pour les technologies alternatives, après chaque maintenance majeure ou modification de procédure. Cette revalidation utilise les mêmes protocoles que la validation initiale, garantissant le maintien des performances dans le temps.
Les études de challenge, utilisant des charges difficiles à stériliser (density packs, test packs), vérifient la robustesse du procédé dans des conditions défavorables. Ces tests, réalisés avec des indicateurs biologiques positionnés aux points critiques, confirment la pénétration stérilisante dans l’ensemble de la charge.
Formation Continue du Personnel
La compétence humaine constitue le facteur critique de succès de tout programme de décontamination. Le personnel doit maîtriser les principes théoriques de la microbiologie, les spécificités techniques de chaque procédé, les protocoles de sécurité et les procédures de contrôle qualité.
La formation initiale, d’une durée minimale de 40 heures selon les standards internationaux, couvre l’ensemble des aspects techniques et réglementaires. Cette formation théorique s’accompagne d’une période de tutorat pratique permettant l’acquisition des gestes techniques sous supervision experte.
La mise à jour continue des connaissances s’effectue par des sessions de formation régulières (trimestrielles), des audits de pratiques, la participation à des congrès professionnels et l’accès à la littérature scientifique actualisée. Les certifications professionnelles, délivrées par des organismes reconnus comme l’IAHCSMM (International Association of Healthcare Central Service Materiel Management) ou le CBSPD (Certification Board for Sterile Processing and Distribution), attestent du maintien des compétences.
Traçabilité et Documentation
La traçabilité complète du cycle de vie de chaque dispositif médical réutilisable constitue une exigence réglementaire incontournable. Cette traçabilité, rendue possible par les systèmes informatisés modernes, enregistre l’historique complet depuis la réception jusqu’à l’utilisation clinique : nettoyage, désinfection/stérilisation, contrôles effectués, dates, opérateurs, numéro de lot.
Les systèmes de codes-barres bidimensionnels (DataMatrix) ou d’identification par radiofréquence (RFID) permettent un suivi automatisé en temps réel. Cette technologie réduit les erreurs de saisie manuelle, accélère les processus et facilite les rappels de lots en cas de non-conformité détectée a posteriori.
Audit et Contrôle Qualité
Les programmes d’audit internes réguliers évaluent la conformité des pratiques aux procédures établies. Ces audits, réalisés par des équipes indépendantes formées aux techniques d’audit, utilisent des grilles standardisées couvrant tous les aspects du processus de retraitement.
Les indicateurs de performance, collectés et analysés mensuellement, incluent : taux de conformité des cycles de stérilisation, délais de retraitement, incidents et non-conformités, résultats des contrôles microbiologiques. Ces données alimentent les revues de direction et orientent les actions d’amélioration continue.
Conclusion
Après plus de six décennies d’application clinique, la classification de Spaulding demeure un pilier incontournable de la prévention des infections nosocomiales. Sa clarté conceptuelle, sa logique scientifique et sa facilité d’application expliquent sa pérennité remarquable malgré les bouleversements technologiques et épidémiologiques survenus depuis 1957.
L’analyse comparative des pratiques en Europe, au Japon et aux États-Unis révèle une convergence remarquable vers des standards d’excellence partagés. Cette harmonisation internationale, portée par les normes ISO et les directives des organismes de santé publique, garantit un niveau de sécurité homogène pour les patients du monde entier.
Les données épidémiologiques confirment l’efficacité de cette approche : la réduction progressive des infections du site opératoire au Japon (de 10% à 5% en vingt ans), la diminution des épidémies liées aux dispositifs médicaux aux États-Unis grâce au renforcement des protocoles CDC, et l’amélioration continue des indicateurs en Europe témoignent de l’impact positif d’une application rigoureuse des principes de Spaulding.
Cependant, les défis contemporains nécessitent une adaptation continue de cette classification. L’émergence de pathogènes multirésistants, la complexité croissante des dispositifs médicaux, les contraintes économiques et environnementales imposent des évolutions majeures. La proposition de reclasser certains endoscopes à haut risque de la catégorie semi-critique vers critique illustre cette nécessaire capacité d’adaptation.
La formation continue des professionnels, l’investissement dans des équipements performants, la validation rigoureuse des procédés et l’audit régulier des pratiques constituent les piliers d’un programme de prévention efficace. Ces investissements, bien que coûteux à court terme, génèrent des bénéfices considérables en termes de réduction de la morbi-mortalité, de diminution des durées d’hospitalisation et d’optimisation des ressources sanitaires.
En cette ère de médecine de précision et de technologies disruptives, la classification de Spaulding conserve toute sa pertinence en offrant un cadre conceptuel clair, adapté aux besoins contemporains tout en restant fidèle aux principes scientifiques fondamentaux. Son application universelle, de Tokyo à Paris, de Berlin à New York, transcende les frontières et les cultures pour servir un objectif commun : la sécurité et le bien-être des patients.
La vision d’Earle H. Spaulding, formulée il y a plus d’un demi-siècle, continue d’éclairer les pratiques contemporaines et guidera certainement les innovations futures. Cette pérennité exceptionnelle témoigne de la profondeur de sa réflexion et de l’universalité des principes qu’il a établis. Dans un monde médical en transformation accélérée, la classification de Spaulding reste un phare stable, guidant les professionnels de santé vers l’excellence en matière de prévention des infections nosocomiales.
« La sécurité du patient n’est pas négociable. La rigueur dans l’application des protocoles de décontamination constitue le fondement inébranlable de cette sécurité. »
Article scientifique rédigé en 2025 – Basé sur les directives internationales les plus récentes (CDC, FDA, OMS, normes ISO)
