Blog
LA STÉRILISATION PAR CHALEUR HUMIDE : PRINCIPES, APPLICATIONS ET AVANTAGES
La stérilisation par chaleur humide représente l’une des méthodes les plus anciennes, les plus fiables et les plus largement utilisées pour l’élimination complète des micro-organismes pathogènes. Développée au XIXe siècle par Louis Pasteur et perfectionnée par Charles Chamberland avec l’invention de l’autoclave en 1879, cette technique révolutionnaire a transformé la pratique médicale et industrielle moderne.
Dans le contexte médical contemporain, où la sécurité des patients constitue une priorité absolue, la stérilisation par chaleur humide demeure la méthode de référence pour le traitement des instruments chirurgicaux, des dispositifs médicaux réutilisables et de nombreux produits pharmaceutiques. Son efficacité prouvée contre l’ensemble du spectre microbien, incluant les bactéries végétatives, les spores résistantes, les virus et même les prions, en fait un procédé incontournable dans les établissements de santé du monde entier.
L’importance de cette technologie s’étend bien au-delà du domaine médical. Dans l’industrie pharmaceutique, agroalimentaire, cosmétique et biotechnologique, la stérilisation par chaleur humide garantit la qualité microbiologique des produits, protège la santé publique et assure la conformité aux réglementations sanitaires internationales les plus strictes. Cette méthode combine efficacité, rapidité, rentabilité économique et respect de l’environnement, caractéristiques qui expliquent sa position dominante dans le panorama des technologies de stérilisation actuelles.
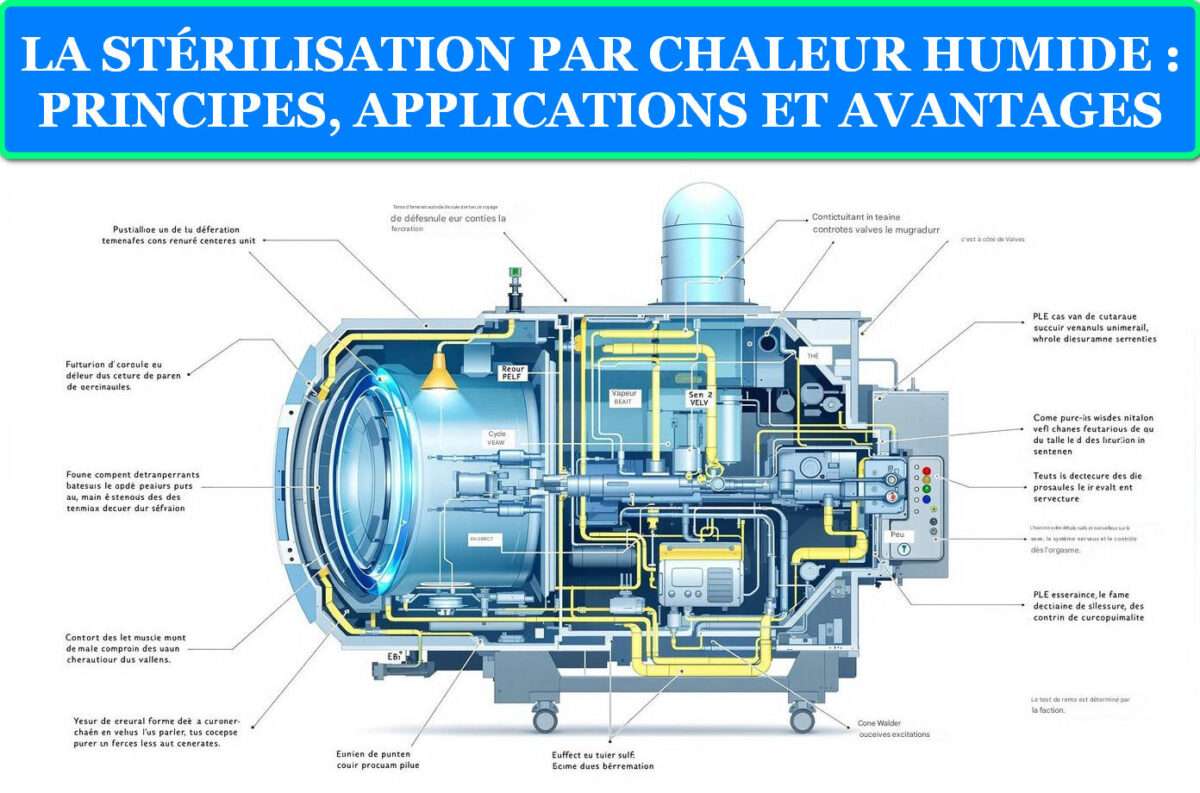
Chapitre 1 : Principes Fondamentaux de la Stérilisation par Chaleur Humide
Définition et Concept de Stérilisation
La stérilisation par chaleur humide, également appelée stérilisation à la vapeur d’eau saturée, constitue un procédé physique qui utilise la combinaison synergique de la température élevée, de la pression et de l’humidité pour détruire de manière irréversible tous les micro-organismes présents sur ou dans les matériaux traités. Cette méthode se distingue fondamentalement de la simple désinfection par sa capacité à éliminer non seulement les formes végétatives des micro-organismes, mais également leurs formes de résistance les plus tenaces, notamment les spores bactériennes.
Le principe fondamental repose sur l’utilisation de vapeur d’eau saturée sous pression, créant un environnement hostile où les conditions thermodynamiques excèdent largement les seuils de résistance de tous les organismes vivants connus. Cette approche garantit un niveau d’assurance de stérilité (SAL – Sterility Assurance Level) de 10⁻⁶, signifiant qu’il existe moins d’une chance sur un million qu’un micro-organisme viable survive au processus.
Bases Thermodynamiques : Relation Température-Pression
La stérilisation par chaleur humide exploite les lois fondamentales de la thermodynamique, particulièrement la relation entre la température et la pression de la vapeur d’eau saturée. Cette relation, décrite par l’équation de Clausius-Clapeyron, établit qu’à chaque température correspond une pression de vapeur saturée spécifique, et inversement.
Dans un autoclave, l’eau est chauffée dans une enceinte fermée, créant de la vapeur sous pression. L’augmentation de la pression permet d’élever significativement la température de la vapeur au-delà du point d’ébullition normal de l’eau (100°C à pression atmosphérique). Ainsi, à une pression de 1 bar au-dessus de la pression atmosphérique, la température de la vapeur saturée atteint 121°C, tandis qu’à 2,2 bars supplémentaires, elle s’élève à 134°C.
Paramètres Standards de Stérilisation
| Température | Pression (bar relatif) | Temps minimum | Application |
|---|---|---|---|
| 121°C | 1,0 | 20 minutes | Instruments non emballés |
| 126°C | 1,4 | 15 minutes | Textiles, matériaux poreux |
| 134°C | 2,2 | 10 minutes | Instruments emballés |
Propriétés de la Vapeur Saturée
La vapeur saturée possède des propriétés physiques uniques qui en font l’agent stérilisant idéal. Contrairement à la vapeur surchauffée ou à l’air chaud, la vapeur saturée présente un coefficient de transfert thermique exceptionnellement élevé, permettant une transmission rapide et homogène de la chaleur aux surfaces et à l’intérieur des matériaux.
Lors de la condensation de la vapeur saturée sur les surfaces plus froides, il se produit un transfert instantané d’énergie thermique considérable (chaleur latente de vaporisation : 2260 kJ/kg à 100°C). Ce phénomène assure une montée en température extrêmement rapide des objets à stériliser, minimisant ainsi les temps d’exposition nécessaires et préservant l’intégrité des matériaux thermosensibles.
Mécanismes de Destruction Microbienne
L’efficacité létale de la chaleur humide résulte de multiples mécanismes d’action synergiques qui perturbent irrémédiablement les structures cellulaires essentielles des micro-organismes. Le mécanisme principal implique la dénaturation thermique des protéines cytoplasmiques et enzymatiques, processus irréversible qui abolit toute activité métabolique.
La présence d’humidité amplifie considérablement l’effet destructeur de la chaleur par rapport à la chaleur sèche. L’eau facilite la pénétration de la chaleur à travers les enveloppes cellulaires et favorise l’hydrolyse des liaisons peptidiques des protéines. Ce processus explique pourquoi la stérilisation par chaleur humide nécessite des températures inférieures et des temps d’exposition plus courts que la stérilisation par chaleur sèche pour obtenir des résultats équivalents.
Dénaturation des Protéines et Rupture Membranaire
Au niveau moléculaire, l’exposition à la chaleur humide provoque la rupture des liaisons hydrogène et des ponts disulfure qui maintiennent la structure tridimensionnelle native des protéines. Cette dénaturation entraîne la perte irréversible de l’activité enzymatique et de la fonction des protéines structurelles essentielles à la viabilité cellulaire.
Simultanément, l’élévation de température modifie la fluidité des membranes cellulaires en perturbant l’organisation des phospholipides membranaires. Cette altération compromet l’intégrité de la barrière cellulaire, provoquant des fuites du contenu cytoplasmique et la perte de l’homéostasie ionique, conduisant inéluctablement à la mort cellulaire.
Dans le cas spécifique des spores bactériennes, structures de résistance particulièrement tenaces, la chaleur humide agit en hydratant et en déstabilisant les couches protectrices externes (cortex et téguments), permettant ainsi la pénétration de la chaleur jusqu’au cœur métaboliquement inactif de la spore. Une fois le noyau sporulaire atteint, la dénaturation des protéines essentielles rend impossible toute germination ultérieure.
Chapitre 2 : L’Autoclave – Équipement et Fonctionnement
Description Technique de l’Autoclave
L’autoclave moderne constitue un système complexe d’ingénierie de précision conçu pour créer et maintenir des conditions de stérilisation parfaitement contrôlées et reproductibles. Cet équipement se compose essentiellement d’une enceinte pressurisée en acier inoxydable capable de résister à des pressions élevées et à des températures extrêmes, entourée d’une enveloppe isolante thermique pour optimiser l’efficacité énergétique et assurer la sécurité des opérateurs.
La conception de l’autoclave intègre des systèmes redondants de sécurité et de contrôle qui garantissent le respect strict des paramètres de stérilisation. Chaque composant est dimensionné selon des normes d’ingénierie strictes et fait l’objet de certifications réglementaires rigoureuses, notamment selon les standards européens EN 285 et EN 13060, ainsi que les directives FDA américaines.
Composants Principaux
La chambre de stérilisation, fabriquée en acier inoxydable 316L résistant à la corrosion, constitue le cœur de l’autoclave. Ses parois épaisses sont calculées pour supporter des pressions de service pouvant atteindre 3,5 bars relatifs tout en maintenant une parfaite étanchéité. La surface intérieure, polie miroir, facilite le nettoyage et minimise les sites de rétention microbienne.
Le générateur de vapeur, intégré ou externe selon les modèles, produit la vapeur saturée nécessaire au processus. Il incorpore des systèmes de purification de l’eau alimentaire pour éliminer les impuretés susceptibles de compromettre la qualité de la vapeur ou de provoquer des dépôts calcaires. Les spécifications requièrent généralement une eau conforme aux standards de l’eau pour préparations injectables.
Le système de vannes automatisées contrôle précisément les flux de vapeur, d’air et de condensats. Les vannes d’admission de vapeur, de purge d’air et d’évacuation des condensats sont pilotées par des actionneurs pneumatiques ou électriques, assurant une séquence de fonctionnement parfaitement synchronisée. Des vannes de sécurité calibrées protègent l’installation contre les surpressions accidentelles.
Les capteurs de température et de pression, éléments critiques du système de contrôle, sont implantés stratégiquement dans la chambre pour surveiller en temps réel l’homogénéité des conditions de stérilisation. Ces sondes, étalonnées selon des procédures métrologiques tracées, transmettent leurs mesures à un système de contrôle informatisé qui pilote automatiquement l’ensemble du cycle.
Types d’Autoclaves
Les autoclaves gravitaires, également appelés autoclaves à déplacement gravitaire, constituent la technologie la plus simple et la plus économique. Dans ces appareils, l’évacuation de l’air s’effectue naturellement par différence de densité, l’air froid et lourd étant chassé vers le bas par la vapeur chaude plus légère. Cette technologie convient parfaitement pour la stérilisation d’instruments métalliques non emballés et de récipients ouverts.
Les autoclaves à pré-vide représentent une évolution technologique majeure qui améliore considérablement l’efficacité de pénétration de la vapeur. Une pompe à vide évacue l’air de la chambre avant l’admission de vapeur, créant un vide partiel qui facilite la pénétration de la vapeur dans les matériaux poreux, les emballages et les corps creux. Cette technologie est indispensable pour la stérilisation d’instruments emballés et de textiles.
Les autoclaves à fractionnement poussent encore plus loin le concept de pré-vide en alternant plusieurs cycles d’évacuation d’air et d’admission de vapeur avant la phase de stérilisation proprement dite. Cette méthode garantit une élimination quasi-totale de l’air résiduel, optimisant ainsi les conditions de transfert thermique et réduisant les temps de stérilisation.

Cycles de Stérilisation Détaillés
Le cycle de stérilisation standard comprend plusieurs phases séquentielles parfaitement orchestrées pour garantir l’efficacité du processus. La phase de conditionnement initiale consiste à éliminer l’air contenu dans la chambre et la charge à stériliser. Cette étape critique détermine largement le succès de la stérilisation, car la présence d’air résiduel crée des zones froides qui échappent à l’action de la vapeur.
La phase de montée en température doit s’effectuer de manière contrôlée pour éviter les chocs thermiques susceptibles d’endommager les matériaux ou de créer des gradients de température dans la charge. Les systèmes modernes intègrent des rampes de température programmables qui s’adaptent aux caractéristiques thermiques des matériaux à stériliser.
Le palier de stérilisation constitue la phase critique où les conditions létales sont maintenues pendant la durée requise. La régulation de température doit maintenir les paramètres dans une tolérance de ±1°C, tandis que la pression reste stable pour préserver l’état de vapeur saturée. Des sondes de surveillance continues vérifient l’homogénéité des conditions dans l’ensemble de la chambre.
La phase de refroidissement et de séchage conclut le cycle en ramenant progressivement la charge à une température compatible avec sa manipulation. Un séchage par vide peut être appliqué pour éliminer l’humidité résiduelle des matériaux poreux et des emballages, prévenant ainsi les risques de recontamination.
Paramètres Critiques
Les paramètres de stérilisation 121°C pendant 20 minutes représentent les conditions de référence internationales pour la destruction des spores de Geobacillus stearothermophilus, micro-organisme test utilisé comme indicateur biologique standard. Ces conditions garantissent une réduction logarithmique de 12 décades de la population microbienne, soit un facteur de stérilisation de 10¹².
Le cycle 126°C pendant 15 minutes offre un compromis intéressant entre efficacité et préservation des matériaux thermosensibles. Cette température légèrement supérieure permet de réduire le temps d’exposition tout en maintenant une marge de sécurité suffisante pour les applications les plus exigeantes.
Les conditions 134°C pendant 10 minutes correspondent aux exigences des normes européennes pour la stérilisation des instruments chirurgicaux emballés. Cette température élevée assure une pénétration rapide de la chaleur à travers les emballages et garantit la destruction des agents pathogènes les plus résistants, y compris les prions responsables des encéphalopathies spongiformes.
Chapitre 3 : Mécanismes Microbiologiques
Action sur les Bactéries Végétatives
Les bactéries végétatives, formes actives et métaboliquement fonctionnelles des micro-organismes bactériens, représentent les cibles les plus vulnérables de la stérilisation par chaleur humide. Leur sensibilité thermique relativement élevée s’explique par la complexité de leurs structures cellulaires et la fragilité de leurs systèmes enzymatiques essentiels au maintien des fonctions vitales.
L’exposition à des températures de 60-80°C suffit généralement à inactiver la plupart des bactéries végétatives en quelques minutes. Cependant, les protocoles de stérilisation appliquent des conditions beaucoup plus sévères pour tenir compte des variations de résistance entre espèces et garantir une marge de sécurité absolue. Les mécanismes de destruction impliquent principalement la dénaturation des protéines membranaires et cytoplasmiques, la perturbation de la synthèse des acides nucléiques et l’altération de la perméabilité membranaire.
Certaines bactéries végétatives, notamment les mycobactéries responsables de la tuberculose, présentent une résistance thermique supérieure en raison de leur paroi cellulaire riche en lipides complexes. Ces micro-organismes nécessitent des conditions de traitement plus sévères, justifiant l’application systématique des paramètres standards de stérilisation même pour des charges apparemment peu contaminées.
Destruction des Spores Bactériennes
Les spores bactériennes constituent les formes de résistance les plus tenaces du monde microbien et représentent par conséquent le défi majeur de tout procédé de stérilisation. Ces structures de survie, produites par certains genres bactériens comme Bacillus et Clostridium, peuvent résister à des conditions environnementales extrêmes pendant des décennies, voire des siècles.
La résistance exceptionnelle des spores résulte de leur architecture complexe multicouche comprenant un cortex déshydraté, des téguments imperméables et un noyau central métaboliquement inactif contenant l’ADN et les éléments essentiels à la germination. Cette structure confère aux spores une résistance thermique de 10 à 100 fois supérieure à celle des formes végétatives correspondantes.
Le processus de destruction des spores par la chaleur humide implique plusieurs étapes séquentielles. La vapeur saturée hydrate et ramollit progressivement les couches externes protectrices, permettant la pénétration de la chaleur vers le noyau central. L’élévation de température provoque ensuite la dénaturation des protéines essentielles à la germination et la dégradation de l’ADN sporulaire, rendant impossible toute réactivation ultérieure.
Résistance Thermique Comparative
- Bactéries végétatives : 60-80°C pendant quelques minutes
- Virus enveloppés : 56-70°C pendant 10-30 minutes
- Virus non enveloppés : 80-100°C pendant 5-15 minutes
- Spores bactériennes : 121°C pendant 15-20 minutes
- Prions : 134°C pendant 18 minutes minimum
Élimination des Virus et Prions
Les virus présentent une sensibilité thermique variable selon leur structure et leur composition. Les virus enveloppés, possédant une membrane lipidique externe, se révèlent généralement plus sensibles à la chaleur que les virus non enveloppés. La dénaturation des protéines de capside et la destruction des acides nucléiques viraux constituent les mécanismes principaux de l’inactivation virale par la chaleur humide.
Les prions, agents protéiques infectieux responsables des encéphalopathies spongiformes transmissibles, représentent un défi particulier en raison de leur résistance exceptionnelle aux traitements conventionnels. Ces protéines anormalement conformées résistent aux procédures de stérilisation standard et nécessitent des conditions particulièrement sévères : 134°C pendant au moins 18 minutes selon les recommandations de l’Organisation Mondiale de la Santé.
La destruction des prions par la chaleur humide implique la dénaturation irréversible de leur structure protéique tertiaire anormale et leur agrégation subséquente en complexes non infectieux. Cette transformation nécessite des conditions thermiques extrêmes qui dépassent largement celles requises pour l’élimination des autres agents pathogènes.
Concept de Valeur F₀
La valeur F₀ (F-zéro) constitue un concept fondamental de la stérilisation thermique qui quantifie l’efficacité létale cumulée d’un traitement thermique en référence aux conditions standard de 121°C. Cette approche mathématique permet de comparer et d’optimiser différents profils de traitement thermique en tenant compte des variations de température au cours du cycle.
Le calcul de la valeur F₀ intègre le fait que l’efficacité létale de la chaleur augmente exponentiellement avec la température selon la loi d’Arrhenius. Une élévation de température de 10°C multiplie généralement l’efficacité létale par un facteur z (coefficient thermique) dont la valeur standard est de 10 pour les spores bactériennes. Ainsi, un traitement à 131°C pendant 1 minute équivaut approximativement à un traitement à 121°C pendant 10 minutes.
L’application du concept F₀ permet d’optimiser les cycles de stérilisation en tenant compte des phases de montée et de descente en température, qui contribuent également à l’effet stérilisant global. Cette approche scientifique rigoureuse garantit l’efficacité du processus tout en minimisant l’exposition thermique des matériaux traités.
Cinétique de Destruction Thermique
La cinétique de destruction thermique des micro-organismes suit généralement une loi de premier ordre, caractérisée par une diminution logarithmique de la population viable en fonction du temps d’exposition à température constante. Cette relation linéaire entre le logarithme du nombre de survivants et le temps de traitement permet de prédire mathématiquement l’efficacité d’un traitement de stérilisation.
La valeur D (decimal reduction time) représente le temps nécessaire à température constante pour réduire d’un facteur 10 (une décade logarithmique) la population microbienne. Cette valeur, spécifique à chaque micro-organisme et à chaque température, constitue un paramètre fondamental pour le dimensionnement des cycles de stérilisation. Par exemple, la valeur D₁₂₁°C de Geobacillus stearothermophilus est d’environ 1,5 à 2 minutes.
La valeur z quantifie l’influence de la température sur la résistance thermique en représentant l’élévation de température nécessaire pour diviser par 10 la valeur D. Cette constante thermique, généralement comprise entre 8 et 12°C pour les spores bactériennes, permet de calculer les équivalences entre différentes conditions de température et de temps.
Chapitre 4 : Applications Médicales et Pharmaceutiques
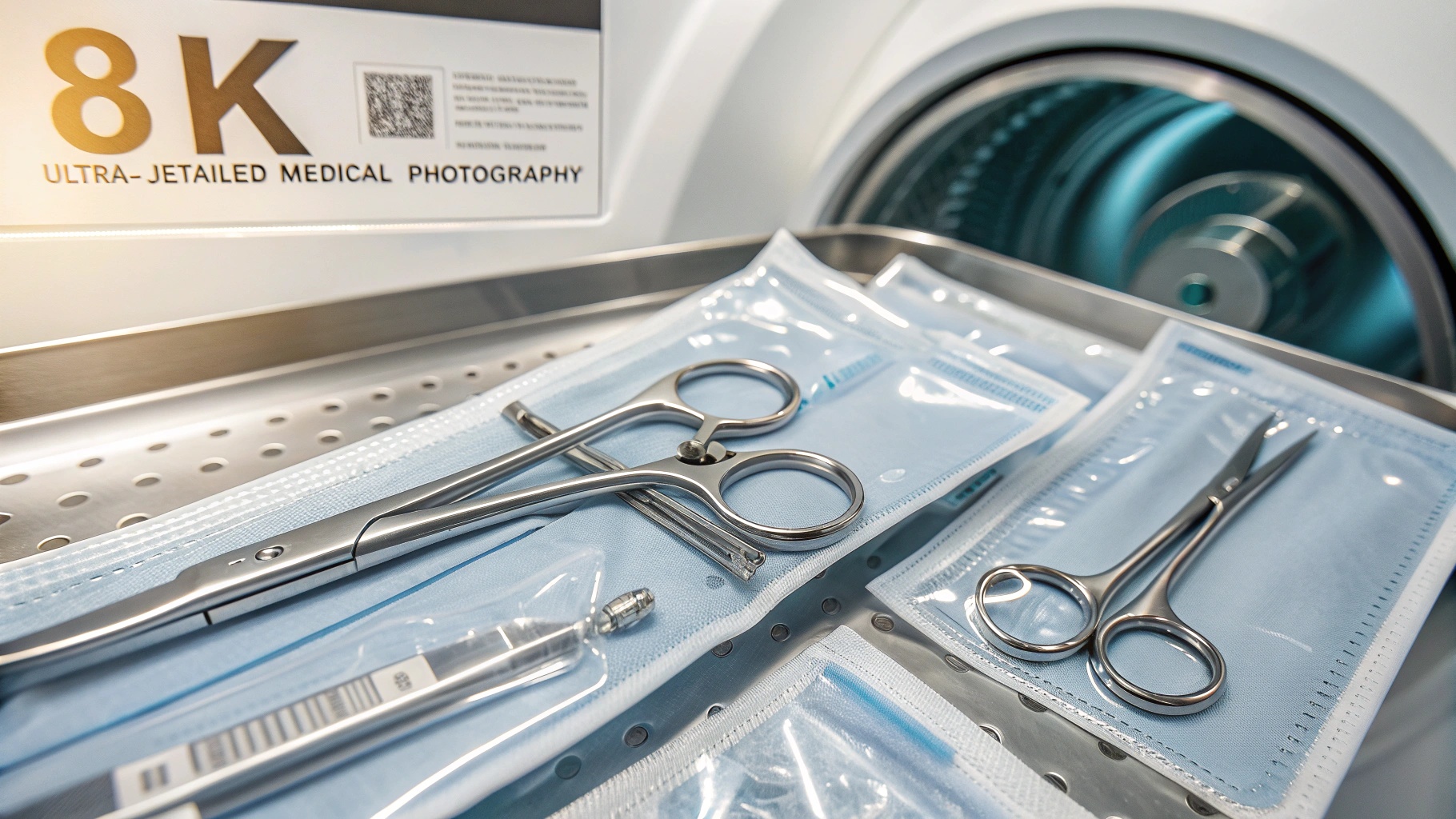
Stérilisation des Instruments Chirurgicaux
La stérilisation des instruments chirurgicaux constitue l’application la plus critique et la plus visible de la technologie de stérilisation par chaleur humide dans le domaine médical. Cette application exige un niveau de fiabilité absolu, car toute défaillance du processus peut avoir des conséquences dramatiques sur la santé des patients, allant de l’infection nosocomiale locale à la septicémie généralisée potentiellement mortelle.
Les instruments chirurgicaux modernes, fabriqués principalement en acier inoxydable de haute qualité, présentent une excellente compatibilité avec les conditions de stérilisation par chaleur humide. Leur résistance à la corrosion et leur stabilité dimensionnelle permettent de répéter les cycles de stérilisation sans altération significative de leurs propriétés mécaniques ou de leur tranchant.
Le processus de stérilisation des instruments chirurgicaux s’intègre dans une chaîne logistique complexe comprenant le pré-nettoyage au bloc opératoire, le transport sécurisé vers la centrale de stérilisation, le nettoyage approfondi par ultrasons ou laveur-désinfecteur, le conditionnement en systèmes d’emballage validés, la stérilisation proprement dite, le stockage dans des conditions contrôlées et enfin la distribution aux services utilisateurs.
Les systèmes d’emballage pour instruments chirurgicaux doivent répondre à des exigences contradictoires : permettre la pénétration de la vapeur stérilisante tout en constituant une barrière efficace contre la recontamination microbienne après stérilisation. Les matériaux couramment utilisés incluent les non-tissés spéciaux, les films plastiques poreux et les containers rigides réutilisables dotés de filtres spécifiques.
Dispositifs Médicaux Réutilisables
Les dispositifs médicaux réutilisables représentent une catégorie vaste et hétérogène d’équipements qui nécessitent une stérilisation entre chaque utilisation pour prévenir les infections croisées. Cette catégorie englobe les endoscopes rigides, les instruments de diagnostic, les équipements de monitoring réutilisables, les prothèses temporaires et de nombreux accessoires médicaux.
La diversité des matériaux constitutifs de ces dispositifs pose des défis particuliers pour la stérilisation par chaleur humide. Alors que les composants métalliques tolèrent généralement bien les conditions standard, les éléments en plastique, caoutchouc ou matériaux composites peuvent présenter des limitations de température ou de compatibilité avec l’humidité. Une analyse préalable de compatibilité est donc indispensable pour chaque nouveau dispositif.
Les dispositifs complexes comportant des lumières étroites, des cavités fermées ou des mécanismes articulés nécessitent une attention particulière pour assurer la pénétration effective de la vapeur stérilisante. Des accessoires spécifiques, tels que les connecteurs de lumière et les adaptateurs de pression, peuvent être nécessaires pour garantir l’efficacité du processus dans les zones difficiles d’accès.
Production Pharmaceutique Stérile
L’industrie pharmaceutique utilise massivement la stérilisation par chaleur humide pour la production de médicaments stériles, notamment les préparations injectables, les collyres, les solutions de perfusion et les produits destinés à l’administration parentérale. Cette application industrielle se caractérise par des volumes de production importants et des exigences réglementaires particulièrement strictes.
Les autoclaves pharmaceutiques industriels sont des équipements de grande capacité, souvent dotés de chambres de plusieurs mètres cubes, capables de traiter simultanément des milliers d’unités de produits finis. Ces installations intègrent des systèmes de validation en continu, des enregistrements automatisés complets et des dispositifs de traçabilité permettant de documenter chaque étape du processus pour chaque lot de production.
La stérilisation terminale des produits pharmaceutiques liquides en récipients scellés présente l’avantage de traiter simultanément le contenant et le contenu, éliminant les risques de recontamination post-stérilisation. Cependant, cette approche nécessite une validation approfondie pour démontrer l’absence d’altération des principes actifs et de l’intégrité des récipients sous l’effet des conditions thermiques appliquées.
Préparations Injectables
Les préparations injectables représentent la classe de médicaments aux exigences de stérilité les plus strictes, car elles sont administrées directement dans la circulation sanguine ou les tissus profonds, contournant les barrières naturelles de défense de l’organisme. La stérilisation par chaleur humide demeure la méthode de choix pour ces produits lorsque leur stabilité thermique le permet.
La formulation des préparations injectables destinées à la stérilisation terminale doit tenir compte de la stabilité thermique des principes actifs et des excipients aux conditions de stérilisation. Les études de stabilité en conditions de stress thermique permettent d’optimiser les formulations et de définir les paramètres de stérilisation compatibles avec le maintien de l’efficacité thérapeutique.
Les récipients pour préparations injectables, généralement en verre borosilicate de type I ou en plastique de qualité pharmaceutique, doivent résister aux contraintes thermiques et mécaniques du processus de stérilisation sans libération de substances extractibles susceptibles de compromettre la sécurité du produit. Des tests d’intégrité spécifiques vérifient l’absence de microfissures ou de déformations après stérilisation.
Applications Pharmaceutiques Principales
- Solutions injectables : Sérums physiologiques, solutions de glucose, antibiotiques
- Préparations ophtalmiques : Collyres, solutions de lavage oculaire
- Solutions de perfusion : Nutrition parentérale, électrolytes
- Produits biologiques : Vaccins thermostables, sérums
- Milieux de culture : Bouillons, géloses pour diagnostic
Milieux de Culture en Microbiologie
La préparation de milieux de culture stériles constitue une application fondamentale de la stérilisation par chaleur humide en microbiologie diagnostique et de recherche. Ces substrats nutritifs, destinés à la croissance contrôlée de micro-organismes, doivent être exempts de toute contamination microbienne tout en préservant leurs propriétés nutritives et leurs caractéristiques physico-chimiques.
Les milieux de culture gélosés présentent des défis particuliers en raison de leur nature thermogélifiante. La température de stérilisation doit être suffisamment élevée pour assurer l’efficacité antimicrobienne tout en évitant la dégradation thermique des composants nutritifs thermolabiles. Les conditions standard de 121°C pendant 15 minutes représentent généralement un compromis optimal pour la plupart des formulations.
Certains milieux enrichis contenant des composants thermosensibles comme le sang, le sérum ou des facteurs de croissance spécifiques nécessitent des approches particulières. La stérilisation fractionnée ou l’addition aseptique post-stérilisation de composants thermolabiles préalablement stérilisés par filtration constituent des alternatives techniques validées.
Normes ISO 17665
La norme internationale ISO 17665 « Stérilisation des produits de santé – Chaleur humide » constitue le référentiel technique et réglementaire incontournable pour toutes les applications de stérilisation par chaleur humide dans le domaine médical et pharmaceutique. Cette norme détaille les exigences de développement, validation et contrôle de routine des procédés de stérilisation par chaleur humide.
Les exigences de la norme ISO 17665 couvrent l’ensemble du cycle de vie du procédé de stérilisation, depuis la phase de développement et d’optimisation jusqu’à la surveillance de routine en passant par la validation initiale complète. Chaque étape fait l’objet de spécifications techniques précises et d’exigences documentaires rigoureuses.
La validation selon ISO 17665 comprend obligatoirement des études de distribution de température, des tests de pénétration de chaleur avec sondes internes aux charges, des défis biologiques avec indicateurs calibrés et des études de simulation de panne pour démontrer la robustesse du procédé. Cette approche scientifique garantit la fiabilité et la reproductibilité des résultats de stérilisation.
Chapitre 5 : Applications Industrielles et Agroalimentaires
Industrie Alimentaire : Conserves et Préparations
L’industrie agroalimentaire représente l’un des secteurs d’application les plus anciens et les plus développés de la stérilisation par chaleur humide, avec une histoire remontant aux travaux pionniers de Nicolas Appert au début du XIXe siècle. Les technologies modernes d’appertisation appliquent les principes de la stérilisation par chaleur humide à une échelle industrielle massive, traitant quotidiennement des millions d’unités de produits alimentaires dans le monde entier.
Les conserves alimentaires traditionnelles constituent l’application la plus visible de cette technologie. Les autoclaves alimentaires industriels, véritables installations de plusieurs mètres de diamètre, traitent simultanément des milliers de boîtes de conserve, de bocaux ou de barquettes dans des conditions parfaitement contrôlées. Les paramètres de stérilisation sont adaptés à chaque type de produit en fonction de son pH, de sa composition et de ses caractéristiques de transfert thermique.
Les produits alimentaires acides (pH < 4,6) bénéficient de conditions de stérilisation moins sévères car l’acidité inhibe la croissance des micro-organismes pathogènes les plus dangereux, notamment Clostridium botulinum. À l’inverse, les produits peu acides nécessitent des traitements thermiques plus intensifs pour garantir la sécurité microbiologique et la stabilité de conservation à température ambiante.
Les nouvelles technologies d’emballage souple, comme les sachets retortables et les barquettes plastiques thermo-scellées, ont révolutionné l’industrie alimentaire en permettant la stérilisation de produits préparés complexes tout en préservant leurs qualités organoleptiques et nutritionnelles. Ces emballages innovants résistent aux contraintes thermiques de la stérilisation tout en offrant une présentation attrayante et une praticité d’utilisation optimale.
Industrie Cosmétique
L’industrie cosmétique utilise la stérilisation par chaleur humide pour garantir la sécurité microbiologique de certains produits sensibles, particulièrement ceux destinés au contour des yeux, aux muqueuses ou aux peaux sensibles. Cette application nécessite une approche particulièrement délicate en raison de la sensibilité thermique de nombreux actifs cosmétiques et de l’importance des propriétés sensorielles des produits finis.
Les émulsions cosmétiques présentent des défis spécifiques car la stabilité de l’émulsion peut être compromise par les conditions thermiques de stérilisation. Des études de formulation approfondies permettent d’optimiser la composition en émulsifiants et stabilisants pour maintenir l’intégrité du produit tout au long du processus de stérilisation.
Les ustensiles et accessoires cosmétiques réutilisables, tels que les pinceaux professionnels, les éponges de qualité supérieure et les instruments de soins esthétiques, bénéficient également de la stérilisation par chaleur humide pour garantir des conditions d’hygiène irréprochables dans les instituts de beauté et les centres de soins.
Laboratoires de Recherche
Les laboratoires de recherche constituent un secteur d’application majeur de la stérilisation par chaleur humide, avec des besoins particulièrement diversifiés et exigeants. La recherche biomédicale, la microbiologie, la biotechnologie et de nombreuses autres disciplines scientifiques dépendent étroitement de la disponibilité d’équipements, de milieux et de réactifs parfaitement stériles.
La verrerie de laboratoire représente l’application la plus courante dans ce secteur. Erlenmeyers, tubes à essai, boîtes de Petri, pipettes et nombreux autres équipements en verre borosilicate supportent parfaitement les conditions de stérilisation standard. La stérilisation groupée de grandes quantités de verrerie dans des autoclaves de laboratoire optimise l’efficacité opérationnelle des équipes de recherche.
Les solutions tampons, les milieux de culture spécialisés et les réactifs biologiques font également l’objet de stérilisation par chaleur humide lorsque leur stabilité thermique le permet. Cette approche garantit l’absence de contamination microbienne susceptible de fausser les résultats expérimentaux ou de compromettre la culture de lignées cellulaires précieuses.
Les équipements de fermentation et de bioréacteurs utilisés en biotechnologie nécessitent une stérilisation in situ particulièrement rigoureuse. Les systèmes de stérilisation à la vapeur intégrés permettent de traiter l’ensemble du circuit de fermentation, y compris les cuves, les conduites, les vannes et les capteurs, garantissant ainsi des conditions aseptiques optimales pour les cultures microbiennes ou cellulaires.
Biotechnologie
L’industrie biotechnologique moderne repose fondamentalement sur la maîtrise de la stérilisation par chaleur humide pour la production de produits biologiques de haute valeur ajoutée. Les bioréacteurs industriels, d’une capacité pouvant atteindre plusieurs milliers de litres, nécessitent des procédures de stérilisation extrêmement rigoureuses pour éviter toute contamination susceptible de compromettre des productions représentant des investissements considérables.
La stérilisation SIP (Sterilization In Place) constitue une technologie de pointe qui permet de traiter l’ensemble d’une installation de production biotechnologique sans démontage des équipements. La vapeur stérilisante circule dans tous les circuits de l’installation selon des séquences programmées, garantissant l’atteinte des conditions létales dans chaque point du système.
Les milieux de culture industriels utilisés en biotechnologie contiennent souvent des composants coûteux et sophistiqués dont la préservation lors de la stérilisation constitue un enjeu économique majeur. L’optimisation des cycles de stérilisation permet de minimiser la dégradation thermique tout en maintenant un niveau de sécurité microbiologique absolu.
Traitement des Déchets Médicaux
Le traitement des déchets médicaux par stérilisation par chaleur humide constitue une application environnementale cruciale qui contribue à la protection de la santé publique et de l’environnement. Cette technologie permet de rendre inertes les déchets potentiellement infectieux avant leur élimination finale, réduisant considérablement les risques de transmission d’agents pathogènes.
Les autoclaves de traitement des déchets sont des équipements industriels robustes conçus pour traiter de gros volumes de déchets hétérogènes dans des conditions particulièrement sévères. Ces installations intègrent des systèmes de broyage préalable pour optimiser la pénétration de la vapeur et des dispositifs de traitement des effluents pour prévenir toute contamination environnementale.
La validation des procédés de traitement des déchets médicaux nécessite des études spécifiques tenant compte de la diversité des matériaux traités et de leurs caractéristiques de transfert thermique. Des indicateurs biologiques spécifiquement positionnés dans les charges permettent de vérifier l’efficacité du traitement dans les conditions réelles d’utilisation.

Chapitre 6 : Avantages et Bénéfices
Efficacité Prouvée Contre Tous les Micro-organismes
L’efficacité de la stérilisation par chaleur humide contre l’ensemble du spectre microbien constitue son avantage le plus fondamental et le plus universellement reconnu. Cette méthode démontre une capacité de destruction remarquable contre tous les types de micro-organismes pathogènes connus, depuis les bactéries végétatives les plus fragiles jusqu’aux spores bactériennes les plus résistantes, en passant par les virus, les champignons et même les prions.
Cette efficacité universelle résulte des mécanismes d’action multiples et synergiques de la chaleur humide qui attaquent simultanément plusieurs cibles cellulaires vitales. Contrairement aux méthodes chimiques qui peuvent présenter des spectres d’action limités ou des phénomènes de résistance, la chaleur humide agit sur des processus biologiques fondamentaux impossibles à contourner par adaptation microbienne.
Les données scientifiques accumulées depuis plus d’un siècle d’utilisation confirment de manière irréfutable la fiabilité de cette méthode. Les études de validation microbiologique réalisées selon les protocoles normalisés internationaux démontrent systématiquement l’obtention de niveaux d’assurance de stérilité de 10⁻⁶, soit une probabilité de survie microbienne inférieure à une chance sur un million.
Cette efficacité prouvée explique pourquoi la stérilisation par chaleur humide demeure la méthode de référence internationale pour toutes les applications critiques où la sécurité microbiologique ne peut souffrir aucun compromis. Les autorités réglementaires du monde entier, qu’il s’agisse de la FDA américaine, de l’EMA européenne ou des agences sanitaires nationales, reconnaissent cette méthode comme le gold standard de la stérilisation.
Rapidité du Procédé vs Chaleur Sèche
La rapidité remarquable de la stérilisation par chaleur humide par rapport à la stérilisation par chaleur sèche constitue un avantage opérationnel majeur qui impacte directement la productivité et l’efficacité des établissements utilisateurs. Cette supériorité temporelle résulte des propriétés thermodynamiques exceptionnelles de la vapeur d’eau saturée.
Les coefficients de transfert thermique de la vapeur saturée dépassent de plusieurs ordres de grandeur ceux de l’air chaud sec. Cette différence fondamentale permet d’obtenir des montées en température quasi-instantanées des objets à stériliser, réduisant drastiquement les temps de cycle global. Là où la chaleur sèche nécessite typiquement 2 à 4 heures pour obtenir une stérilisation efficace, la chaleur humide atteint des résultats équivalents en 15 à 60 minutes selon les applications.
Cette rapidité se traduit par des bénéfices économiques considérables dans les environnements à forte rotation d’instruments, comme les blocs opératoires, les services d’urgences ou les industries pharmaceutiques. La réduction des temps de cycle permet d’augmenter significativement le débit de traitement des équipements de stérilisation, optimisant ainsi le retour sur investissement et réduisant les besoins en stock d’instruments de réserve.
La rapidité du procédé contribue également à la préservation de la qualité des matériaux traités en minimisant leur exposition aux conditions thermiques. Cette caractéristique s’avère particulièrement précieuse pour les matériaux thermosensibles ou les dispositifs complexes comportant des éléments délicats susceptibles de se dégrader lors d’expositions thermiques prolongées.
Pénétration Optimale dans les Matériaux Poreux
La capacité exceptionnelle de pénétration de la vapeur d’eau saturée dans les matériaux poreux, les textiles et les corps creux constitue un avantage décisif de la stérilisation par chaleur humide. Cette propriété résulte des caractéristiques physiques uniques de la vapeur qui lui permettent de s’infiltrer dans les moindres interstices et de condenser au contact des surfaces, libérant instantanément son énergie thermique.
Les textiles médicaux, tels que les champs opératoires, les blouses chirurgicales et les compresses, bénéficient particulièrement de cette propriété. La vapeur pénètre efficacement entre les fibres, assurant une stérilisation homogène de l’ensemble du matériau, y compris dans les zones les plus denses ou les plus difficilement accessibles. Cette pénétration optimale garantit l’élimination de tous les micro-organismes présents, même ceux logés au cœur des structures fibreuses.
Les instruments à lumières étroites, comme les endoscopes rigides, les canules ou les tubulures médicales, présentent des défis particuliers pour la stérilisation en raison de la difficulté d’accès des agents stérilisants aux surfaces internes. La vapeur d’eau saturée surmonte efficacement ces obstacles grâce à sa capacité à circuler dans les espaces confinés et à condenser sur toutes les surfaces, même les plus inaccessibles.
Cette propriété de pénétration permet également la stérilisation efficace de charges complexes et hétérogènes, où des instruments de formes et de matériaux différents sont traités simultanément. La vapeur s’adapte naturellement à la géométrie de chaque objet, assurant une distribution thermique homogène indépendamment de la complexité de la charge.
Rentabilité Économique
La rentabilité économique exceptionnelle de la stérilisation par chaleur humide constitue un facteur déterminant dans son choix par les établissements de santé et les industries. Cette rentabilité résulte de la combinaison de plusieurs facteurs : coûts d’investissement modérés, frais de fonctionnement réduits, maintenance simplifiée et absence de consommables coûteux.
Les coûts d’investissement des autoclaves, bien que significatifs, demeurent généralement inférieurs à ceux des technologies alternatives comme l’irradiation gamma ou la stérilisation par plasma. De plus, la durée de vie exceptionnelle de ces équipements, souvent supérieure à 20 ans avec une maintenance appropriée, amortit largement l’investissement initial sur la période d’utilisation.
Les frais de fonctionnement se limitent essentiellement aux coûts énergétiques (électricité ou gaz pour la production de vapeur) et à la consommation d’eau purifiée. Ces coûts variables restent très modérés comparés aux consommables spécifiques requis par d’autres méthodes de stérilisation, comme les cartouches de plasma, les ampoules d’oxyde d’éthylène ou les indicateurs de contrôle spécialisés.
La simplicité relative de la technologie facilite la maintenance et réduit les coûts de service après-vente. Les compétences techniques requises pour l’entretien des autoclaves sont largement disponibles, contrairement aux technologies de pointe qui nécessitent des interventions de spécialistes hautement qualifiés et coûteux.
Analyse Comparative des Coûts (pour 1000 cycles/an)
| Méthode | Investissement initial | Coût par cycle | Maintenance annuelle |
|---|---|---|---|
| Chaleur humide | 50 000 – 200 000 € | 2 – 5 € | 3 000 – 8 000 € |
| Oxyde d’éthylène | 100 000 – 300 000 € | 15 – 25 € | 8 000 – 15 000 € |
| Plasma H₂O₂ | 150 000 – 400 000 € | 20 – 35 € | 10 000 – 20 000 € |
Absence de Résidus Toxiques
L’absence totale de résidus toxiques constitue un avantage majeur de la stérilisation par chaleur humide qui contribue significativement à la sécurité des patients et à la protection de l’environnement. Contrairement aux méthodes de stérilisation chimique qui peuvent laisser des traces de substances potentiellement nocives, la stérilisation par vapeur d’eau ne génère aucun sous-produit toxique.
Les méthodes de stérilisation chimique, comme l’oxyde d’éthylène ou le formaldéhyde, nécessitent des phases de désorption prolongées pour éliminer les résidus chimiques susceptibles de provoquer des réactions allergiques, des irritations ou des toxicités systémiques chez les patients. Ces contraintes imposent des délais supplémentaires entre la stérilisation et l’utilisation des dispositifs, compliquant la gestion logistique et augmentant les besoins en stock.
La vapeur d’eau utilisée en stérilisation se condense simplement en eau pure lors du refroidissement, ne laissant aucune trace chimique sur les surfaces traitées. Cette caractéristique permet une utilisation immédiate des dispositifs stérilisés dès la fin du cycle, sans risque pour la sécurité des patients ou du personnel médical.
Cette absence de résidus toxiques simplifie également considérablement la gestion des déchets et des effluents générés par le processus de stérilisation. Aucun traitement spécial n’est requis pour les condensats ou les émissions gazeuses, contrairement aux méthodes chimiques qui nécessitent des systèmes de captation et de neutralisation coûteux et complexes.
Facilité de Validation et Contrôle
La facilité remarquable de validation et de contrôle de la stérilisation par chaleur humide constitue un avantage opérationnel considérable qui facilite grandement la mise en conformité réglementaire et la gestion qualité. Cette facilité résulte du caractère mesurable et prévisible des paramètres physiques impliqués dans le processus.
Les paramètres critiques de la stérilisation par chaleur humide – température, pression et temps – sont directement mesurables par des instruments de précision étalonnés selon des références métrologiques nationales ou internationales. Cette traçabilité métrologique permet d’établir des preuves objectives et reproductibles de l’efficacité du processus, facilitant grandement les audits réglementaires et les certifications qualité.
Les systèmes de contrôle modernes intègrent des enregistrements automatiques en continu de tous les paramètres critiques, générant automatiquement une documentation complète de chaque cycle de stérilisation. Cette documentation électronique facilite la traçabilité, réduit les risques d’erreurs de transcription et simplifie les analyses statistiques de performance du processus.
La validation biologique du processus peut être réalisée facilement à l’aide d’indicateurs biologiques standardisés et commercialement disponibles. Ces indicateurs, contenant des spores de Geobacillus stearothermophilus de résistance thermique calibrée, fournissent une confirmation directe de l’efficacité du processus sans nécessiter d’équipements d’analyse sophistiqués.
Impact Environnemental Réduit
L’impact environnemental particulièrement réduit de la stérilisation par chaleur humide constitue un atout majeur dans le contexte actuel de développement durable et de responsabilité environnementale des établissements de santé et des industries. Cette caractéristique résulte de l’utilisation exclusive d’énergie thermique et de vapeur d’eau, substances naturelles non polluantes.
Contrairement aux méthodes de stérilisation utilisant des gaz toxiques ou des rayonnements ionisants, la stérilisation par chaleur humide ne génère aucune émission nocive pour l’environnement. Les seuls effluents produits sont la vapeur d’eau condensée et les eaux de refroidissement, qui peuvent être directement rejetées dans les réseaux d’assainissement conventionnels sans traitement préalable.
La consommation énergétique des autoclaves modernes a été considérablement optimisée grâce aux progrès de l’isolation thermique, de la récupération de chaleur et de l’automatisation des cycles. Les systèmes de récupération de vapeur permettent de réutiliser une partie de l’énergie thermique pour préchauffer l’eau d’alimentation, réduisant significativement la consommation énergétique globale.
L’absence de déchets dangereux générés par le processus simplifie la gestion environnementale et réduit les coûts de traitement des déchets spéciaux. Cette caractéristique contraste favorablement avec les méthodes chimiques qui produisent des déchets classés comme dangereux nécessitant des filières de traitement spécialisées et coûteuses.
Chapitre 7 : Validation et Contrôle Qualité
Validation des Cycles de Stérilisation
La validation des cycles de stérilisation constitue une exigence réglementaire absolue qui garantit de manière scientifique et documentée l’efficacité et la reproductibilité du processus de stérilisation. Cette démarche rigoureuse s’inscrit dans le cadre des Bonnes Pratiques de Fabrication (BPF) et des normes internationales ISO 17665, établissant un protocole méthodologique strict pour démontrer que le procédé atteint systématiquement les objectifs de stérilité requis.
Le processus de validation comprend trois phases distinctes et complémentaires : la qualification de l’installation (QI) qui vérifie la conformité de l’équipement aux spécifications techniques, la qualification opérationnelle (QO) qui démontre le fonctionnement correct de tous les systèmes dans les conditions normales d’utilisation, et la qualification de performance (QP) qui prouve l’efficacité du processus avec des charges réelles représentatives.
La validation initiale nécessite la réalisation d’au moins trois cycles consécutifs réussis dans les conditions les plus défavorables (worst case) identifiées lors de l’analyse de risque. Cette approche garantit que le procédé reste efficace même dans les situations les plus critiques, démontrant sa robustesse et sa fiabilité opérationnelle.
Les études de validation doivent être répétées périodiquement lors de revalidations programmées, généralement annuelles, ainsi qu’après toute modification significative de l’équipement, du processus ou des produits traités. Cette maintenance de l’état validé assure la continuité de la conformité réglementaire et la pérennité de l’assurance qualité.
Tests de Distribution de Température
Les tests de distribution de température, également appelés études de mapping thermique, constituent une étape fondamentale de la validation qui vise à caractériser l’homogénéité spatiale des conditions thermiques dans l’ensemble de la chambre de stérilisation. Ces études permettent d’identifier les zones froides potentielles où les conditions de stérilisation pourraient être sous-optimales.
La méthodologie standard implique le positionnement stratégique de multiples sondes de température calibrées (généralement 9 à 16 sondes) réparties selon une grille tridimensionnelle couvrant l’ensemble du volume utile de la chambre. Ces sondes, reliées à un système d’acquisition de données, enregistrent en continu l’évolution de la température à chaque emplacement tout au long du cycle de stérilisation.
L’analyse des données recueillies permet de calculer les gradients thermiques, d’identifier la position du point froid (cold spot) et de déterminer le temps nécessaire pour atteindre l’homogénéité thermique dans l’ensemble de la charge. Ces informations critiques servent à optimiser les paramètres du cycle et à définir les configurations de chargement acceptables.
Les critères d’acceptation typiques exigent que l’écart de température entre le point le plus chaud et le point le plus froid n’excède pas 2 à 3°C pendant la phase de stérilisation. Cette uniformité garantit que toutes les zones de la charge reçoivent un traitement thermique suffisant pour assurer la stérilité.
Tests de Pénétration de Chaleur
Les tests de pénétration de chaleur complètent les études de distribution en caractérisant la cinétique de transfert thermique à l’intérieur des produits et des emballages à stériliser. Ces études sont particulièrement critiques pour les charges complexes, les produits liquides en récipients fermés ou les dispositifs comportant des zones difficiles d’accès.
La méthodologie consiste à positionner des sondes thermocouple miniatures à des emplacements stratégiques à l’intérieur des produits, typiquement au centre géométrique des récipients ou dans les zones identifiées comme les plus difficiles à chauffer. Ces sondes internes permettent de mesurer directement la température au cœur du produit et de déterminer le temps nécessaire pour atteindre les conditions létales.
Les données de pénétration thermique permettent de calculer précisément la valeur F₀ délivrée au point le plus froid de la charge, garantissant que même les zones les moins exposées reçoivent un traitement thermique suffisant. Cette approche scientifique rigoureuse élimine toute incertitude quant à l’efficacité du processus.
Les profils thermiques obtenus guident l’optimisation des cycles de stérilisation en permettant d’ajuster les temps de palier pour compenser les délais de pénétration thermique. Cette optimisation minimise l’exposition thermique globale tout en maintenant une marge de sécurité suffisante pour garantir la stérilité.
Indicateurs Biologiques (Geobacillus stearothermophilus)
Les indicateurs biologiques constituent le gold standard de la validation microbiologique des procédés de stérilisation par chaleur humide. Ces dispositifs contiennent une population calibrée et standardisée de spores de Geobacillus stearothermophilus (anciennement Bacillus stearothermophilus), micro-organisme sélectionné pour sa résistance thermique exceptionnelle et sa parfaite reproductibilité.
Les spores de G. stearothermophilus présentent une valeur D₁₂₁°C d’environ 1,5 à 2,0 minutes et une valeur z de 10°C, caractéristiques qui en font un organisme test idéal. Leur résistance thermique dépasse largement celle de tous les micro-organismes pathogènes connus, garantissant qu’un cycle capable de détruire ces spores éliminera nécessairement tous les contaminants potentiels.
Les indicateurs biologiques commerciaux se présentent sous diverses formes : ampoules auto-contenues, bandelettes de papier, suspensions liquides ou systèmes à lecture rapide par fluorescence. Chaque format offre des avantages spécifiques selon les applications, mais tous contiennent une population sporulaire calibrée généralement comprise entre 10⁵ et 10⁶ spores par unité.
Le protocole de validation standard requiert le positionnement d’indicateurs biologiques aux emplacements les plus critiques de la charge, notamment au point froid identifié lors des études de distribution thermique. Après exposition au cycle de stérilisation, les indicateurs sont incubés dans des conditions optimales de croissance pour détecter toute survie microbienne. L’absence de croissance après incubation confirme l’efficacité du processus.
Indicateurs Chimiques
Les indicateurs chimiques complètent les indicateurs biologiques en fournissant une vérification immédiate et visuelle de l’exposition aux conditions de stérilisation. Ces dispositifs subissent un changement de couleur ou d’apparence irréversible lorsqu’ils sont exposés aux paramètres de stérilisation, permettant une détection rapide des défaillances du processus.
Les indicateurs chimiques sont classés selon six catégories normalisées (classes 1 à 6) en fonction de leur complexité et de leur spécificité. Les indicateurs de classe 1 (indicateurs de passage) fournissent une simple confirmation d’exposition à la stérilisation. Les indicateurs de classe 5 (indicateurs intégrateurs) simulent la réponse des spores bactériennes et fournissent une vérification semi-quantitative de l’efficacité du cycle.
L’utilisation d’indicateurs chimiques externes sur chaque emballage et d’indicateurs internes dans chaque charge constitue une exigence réglementaire standard. Cette double vérification permet de distinguer les articles traités des articles non traités et de détecter rapidement les problèmes de pénétration de vapeur dans les emballages.
Les indicateurs chimiques offrent l’avantage d’une lecture immédiate, contrairement aux indicateurs biologiques qui nécessitent plusieurs jours d’incubation. Cette rapidité permet de libérer les charges stérilisées sans délai dans les applications critiques, tout en conservant les indicateurs biologiques comme confirmation définitive de l’efficacité du processus.
Enregistrements et Traçabilité
Les systèmes d’enregistrement et de traçabilité constituent l’ossature documentaire de l’assurance qualité en stérilisation. Chaque cycle de stérilisation génère un ensemble complet de données qui doivent être conservées pendant des durées définies par les réglementations (généralement 5 à 30 ans selon les pays et les applications).
Les autoclaves modernes intègrent des systèmes informatisés d’enregistrement qui capturent automatiquement tous les paramètres critiques avec une fréquence d’échantillonnage élevée (typiquement une mesure par seconde). Ces systèmes génèrent des courbes de stérilisation complètes montrant l’évolution de la température, de la pression et des autres paramètres pertinents tout au long du cycle.
Les données électroniques sont généralement complétées par des enregistrements papier imprimés immédiatement après chaque cycle, fournissant une redondance de sécurité et facilitant la révision visuelle rapide par les opérateurs et les contrôleurs qualité. Ces documents sont signés par le personnel qualifié attestant de la conformité du cycle avant libération de la charge.
La traçabilité complète nécessite l’établissement de liens documentaires entre les charges stérilisées, les patients ou les lots de production concernés, permettant ainsi un rappel ciblé en cas de détection d’anomalies a posteriori. Les systèmes informatisés modernes facilitent grandement cette traçabilité par l’utilisation de codes-barres, de puces RFID et de bases de données intégrées.
Maintenance Préventive
Un programme de maintenance préventive rigoureux et systématique constitue un pilier essentiel de la fiabilité et de la conformité continues des autoclaves. Cette approche proactive vise à détecter et corriger les dérives potentielles avant qu’elles n’affectent l’efficacité du processus ou ne provoquent des pannes coûteuses.
Le programme de maintenance préventive doit couvrir l’ensemble des composants critiques : vérification et calibration régulières des capteurs de température et de pression, inspection des joints d’étanchéité et des vannes, contrôle des systèmes de sécurité, nettoyage des filtres et des purgeurs, vérification de la qualité de la vapeur et analyse de l’eau d’alimentation.
La fréquence des interventions de maintenance est définie en fonction des recommandations du fabricant, de l’intensité d’utilisation et de l’historique de performance de chaque appareil. Les opérations courantes sont généralement réalisées mensuellement ou trimestriellement, tandis que les révisions majeures interviennent annuellement ou après un nombre défini de cycles.
Toutes les interventions de maintenance doivent être documentées dans un journal de bord de l’équipement, incluant la nature des opérations réalisées, les mesures effectuées, les pièces remplacées et l’identité des intervenants. Cette documentation permet de reconstituer l’historique complet de l’appareil et facilite l’investigation en cas de problème.
Normes Réglementaires
Le cadre réglementaire de la stérilisation par chaleur humide s’articule autour d’un ensemble cohérent de normes internationales, européennes et nationales qui définissent les exigences techniques, les protocoles de validation et les bonnes pratiques de fabrication applicables.
La norme ISO 17665 « Stérilisation des produits de santé – Chaleur humide » constitue le référentiel technique international principal. Cette norme détaille les exigences relatives au développement, à la validation et au contrôle de routine des procédés de stérilisation par chaleur humide, fournissant un cadre méthodologique complet et scientifiquement fondé.
Les normes EN 285 et EN 13060 définissent les exigences spécifiques aux autoclaves à vapeur d’eau utilisés respectivement dans les grandes installations de stérilisation et dans les petits stérilisateurs de cabinet. Ces normes précisent les spécifications de conception, de construction, de performance et d’essai des équipements.
Les Bonnes Pratiques de Fabrication pharmaceutique (BPF/GMP) intègrent des chapitres spécifiques à la stérilisation qui imposent des exigences strictes en matière de validation, de contrôle en continu, de formation du personnel et de documentation. Le respect de ces exigences est vérifié lors des inspections réglementaires régulières effectuées par les autorités sanitaires.
Chapitre 8 : Limitations et Précautions
Matériaux Incompatibles
Malgré ses nombreux avantages, la stérilisation par chaleur humide présente des limitations importantes liées à l’incompatibilité de certains matériaux avec les conditions thermiques et hygrométriques du processus. La connaissance précise de ces incompatibilités est essentielle pour éviter la dégradation des dispositifs médicaux et garantir leur fonctionnalité après stérilisation.
Les matériaux thermoplastiques constituent la catégorie la plus problématique. Le polyéthylène, le polypropylène de bas point de fusion, le PVC et de nombreux autres polymères courants se déforment, ramollissent ou fondent aux températures de stérilisation standard. Ces matériaux nécessitent des méthodes alternatives comme la stérilisation à basse température par oxyde d’éthylène ou plasma de peroxyde d’hydrogène.
Les instruments électroniques et les dispositifs comportant des composants sensibles à l’humidité ou à la chaleur sont généralement incompatibles avec la stérilisation par chaleur humide. Les circuits imprimés, les batteries, les écrans LCD et de nombreux capteurs électroniques peuvent subir des dommages irréversibles lors de l’exposition aux conditions de stérilisation.
Certains matériaux absorbent l’humidité de manière excessive pendant le cycle de stérilisation, pouvant entraîner un gonflement, une altération dimensionnelle ou une modification des propriétés mécaniques. Les poudres, les huiles, les lubrifiants et les matériaux hydrophobes ne peuvent généralement pas être stérilisés efficacement par chaleur humide en raison de l’impossibilité de pénétration de la vapeur.
Risques de Corrosion
La corrosion constitue un risque majeur associé à la stérilisation par chaleur humide, particulièrement pour les instruments métalliques de précision. L’environnement agressif créé par la combinaison de températures élevées, d’humidité saturée et de cycles thermiques répétés favorise divers mécanismes de corrosion susceptibles de compromettre l’intégrité et la fonctionnalité des dispositifs.
Les aciers au carbone et les alliages faiblement résistants à la corrosion sont particulièrement vulnérables et peuvent développer rapidement une corrosion généralisée (rouille) ou une corrosion localisée (piqûres). Même les aciers inoxydables de haute qualité peuvent subir une corrosion en présence d’impuretés dans la vapeur, particulièrement les chlorures qui favorisent la corrosion par piqûres.
La qualité de la vapeur utilisée joue un rôle critique dans la prévention de la corrosion. Une vapeur contenant des contaminants chimiques (chlorures, sulfates, métaux lourds) ou présentant une fraction sèche insuffisante peut entraîner des dépôts corrosifs sur les surfaces métalliques. Le respect des spécifications strictes de qualité de la vapeur selon les normes applicables est donc impératif.
Les mesures préventives incluent l’utilisation de matériaux résistants à la corrosion (acier inoxydable 316L, titane, alliages spéciaux), l’application de revêtements protecteurs, le séchage complet après stérilisation, et un programme de maintenance incluant l’inspection régulière et le traitement anticorrosion des instruments. La formation du personnel aux bonnes pratiques de manipulation et de stockage contribue également à minimiser les risques de corrosion.
Emballages Inappropriés
Le choix d’emballages appropriés constitue un facteur critique du succès de la stérilisation par chaleur humide. Des emballages inadaptés peuvent compromettre l’efficacité du processus en empêchant la pénétration de la vapeur, ou inversement, échouer à maintenir la stérilité après traitement en raison d’une barrière microbienne insuffisante.
Les emballages complètement étanches à la vapeur, comme les conteneurs hermétiques sans filtres ou les sachets plastiques imperméables, empêchent la pénétration de la vapeur stérilisante et créent des zones non stérilisées à l’intérieur. Ces emballages doivent être systématiquement proscrits pour la stérilisation par chaleur humide.
Les matériaux d’emballage doivent résister aux conditions de stérilisation sans se dégrader, se déchirer ou perdre leurs propriétés de barrière. Les non-tissés médicaux spécialement conçus pour la stérilisation, les films poreux spéciaux et les containers avec filtres validés constituent les options appropriées. Chaque type d’emballage doit faire l’objet d’une validation spécifique démontrant sa compatibilité avec le processus.
Le sur-emballage ou l’emballage excessivement serré peut créer des obstacles à la circulation de la vapeur et générer des poches d’air qui compromettent l’efficacité du traitement. Des protocoles précis d’emballage doivent être établis, incluant des limites de poids maximal par emballage, des spécifications de disposition des articles et des règles de chargement des autoclaves.
Mesures de Sécurité
L’exploitation d’autoclaves nécessite le respect rigoureux de mesures de sécurité pour protéger le personnel contre les risques inhérents à la manipulation d’équipements sous pression élevée et à haute température. Ces risques incluent les brûlures par vapeur, les blessures par explosion et les accidents liés à la manipulation de charges lourdes.
Les dispositifs de sécurité intégrés aux autoclaves modernes comprennent des systèmes de verrouillage de porte qui empêchent l’ouverture tant que la pression n’est pas revenue à la pression atmosphérique, des soupapes de sécurité calibrées qui protègent contre les surpressions, des systèmes de détection de fuite et des arrêts d’urgence facilement accessibles.
Le personnel opérateur doit recevoir une formation approfondie couvrant les principes de fonctionnement des autoclaves, les procédures opératoires standard, la reconnaissance des dysfonctionnements, les premiers secours en cas d’accident et les procédures d’urgence. Cette formation doit être documentée et faire l’objet de recyclages réguliers.
L’utilisation d’équipements de protection individuelle appropriés est obligatoire lors de la manipulation des autoclaves. Les gants thermiques résistants à la chaleur, les lunettes de protection, les blouses adaptées et les chaussures de sécurité constituent l’équipement minimal. Des procédures écrites détaillées doivent définir les pratiques sécuritaires de chargement, de déchargement et de maintenance.
L’installation des autoclaves doit respecter les codes de sécurité applicables aux équipements sous pression, incluant des dégagements suffisants, une ventilation adéquate, des systèmes d’évacuation d’urgence de la vapeur et une signalisation claire des dangers. Des inspections réglementaires périodiques par des organismes agréés garantissent le maintien de la conformité aux exigences de sécurité.
Conclusion
La stérilisation par chaleur humide demeure, après plus d’un siècle d’utilisation et de perfectionnement, la méthode de stérilisation de référence dans les domaines médical, pharmaceutique et industriel. Cette position prééminente résulte d’une combinaison unique d’avantages qui en font une technologie inégalée : efficacité universelle contre tous les micro-organismes, rapidité opérationnelle, pénétration optimale, rentabilité économique, absence de résidus toxiques et facilité de validation.
Les principes scientifiques qui sous-tendent cette méthode, fondés sur les lois de la thermodynamique et les mécanismes biologiques de destruction microbienne, sont parfaitement maîtrisés et documentés. Les technologies modernes d’autoclavage intègrent des systèmes de contrôle sophistiqués, des dispositifs de sécurité redondants et des capacités de traçabilité complète qui garantissent la fiabilité et la conformité réglementaire des processus.
Les applications de la stérilisation par chaleur humide continuent de s’étendre et de se diversifier, touchant non seulement les secteurs traditionnels de la santé et de la pharmacie, mais également de nouveaux domaines comme la biotechnologie avancée, les dispositifs médicaux innovants et les technologies médicales de pointe. Cette adaptabilité témoigne de la pertinence durable de cette technologie dans un environnement en constante évolution.
Les développements futurs s’orientent vers l’optimisation énergétique des équipements, l’intégration de l’intelligence artificielle pour la surveillance prédictive et la maintenance, l’amélioration des systèmes de traçabilité par blockchain, et le développement de cycles ultra-rapides pour répondre aux exigences de réactivité des services d’urgence modernes. Ces innovations promettent d’accroître encore l’efficience et la fiabilité de cette technologie fondamentale.
Dans le contexte actuel d’exigences accrues en matière de sécurité sanitaire, de qualité pharmaceutique et de développement durable, la stérilisation par chaleur humide représente une solution éprouvée, économique et respectueuse de l’environnement. Son rôle essentiel dans la protection de la santé publique et la sécurité des patients demeurera central dans les décennies à venir, consolidant sa position comme pierre angulaire des technologies de stérilisation modernes.
