Blog
L’AUTOCLAVE EN MICROBIOLOGIE : UN OUTIL INDISPENSABLE POUR LA STÉRILISATION ET LA SÉCURITÉ
L’autoclave représente l’une des innovations technologiques les plus fondamentales de la microbiologie moderne, constituant l’épine dorsale de la sécurité biologique dans tous les laboratoires de recherche, établissements de santé et installations industrielles du monde entier. Cet instrument de stérilisation à vapeur saturée sous pression a révolutionné les pratiques scientifiques et médicales depuis sa conception au XIXe siècle, permettant l’élimination fiable et reproductible de tous les micro-organismes pathogènes et non-pathogènes. Ce guide exhaustif explore les principes fondamentaux de l’autoclavage, les technologies modernes, les protocoles de validation, et les applications critiques de cet outil indispensable pour garantir la sécurité microbiologique.
1. Fondements Historiques et Scientifiques de l’Autoclave
Évolution Historique et Innovations Technologiques
L’histoire de l’autoclave débute en 1679 avec Denis Papin et son « digesteur à vapeur », précurseur conceptuel de l’autoclave moderne. L’évolution vers les applications médicales et scientifiques s’accélère au XIXe siècle avec les travaux de Louis Pasteur sur la stérilisation, culminant avec le développement du premier autoclave médical par Charles Chamberland en 1879. Cette innovation révolutionne immédiatement les pratiques chirurgicales et laboratoires, réduisant drastiquement les infections nosocomiales.
L’évolution technologique moderne intègre des systèmes de contrôle électroniques sophistiqués, des capteurs de température et pression haute précision, et des programmes automatisés garantissant la reproductibilité des cycles de stérilisation. Les autoclaves contemporains incorporent des interfaces utilisateur intuitives, des systèmes de traçabilité numérique, et des mécanismes de sécurité multicouches prévenant les accidents et garantissant l’efficacité des processus.
Principes Physico-Chimiques de la Stérilisation
La stérilisation par autoclave repose sur l’action léthale combinée de la température élevée, de la pression, de l’humidité et du temps d’exposition. La vapeur d’eau saturée, agent stérilisant primaire, pénètre efficacement les structures cellulaires microbiennes, dénature les protéines essentielles, et détruit les acides nucléiques nécessaires à la reproduction microbienne. Cette action multimodale garantit l’élimination de l’ensemble du spectre microbien, incluant les spores bactériennes les plus résistantes.
Le mécanisme de mort microbienne implique la coagulation des protéines cytoplasmiques et la dénaturation des enzymes vitales sous l’effet de la chaleur humide. La pression élevée facilite la pénétration de la vapeur dans les structures complexes et accélère les réactions de dénaturation. Cette synergie température-pression-humidité-temps constitue le fondement scientifique de l’efficacité universellement reconnue de l’autoclavage.
2. Principes de Fonctionnement et Technologies Modernes
Cycles de Stérilisation et Paramètres Critiques
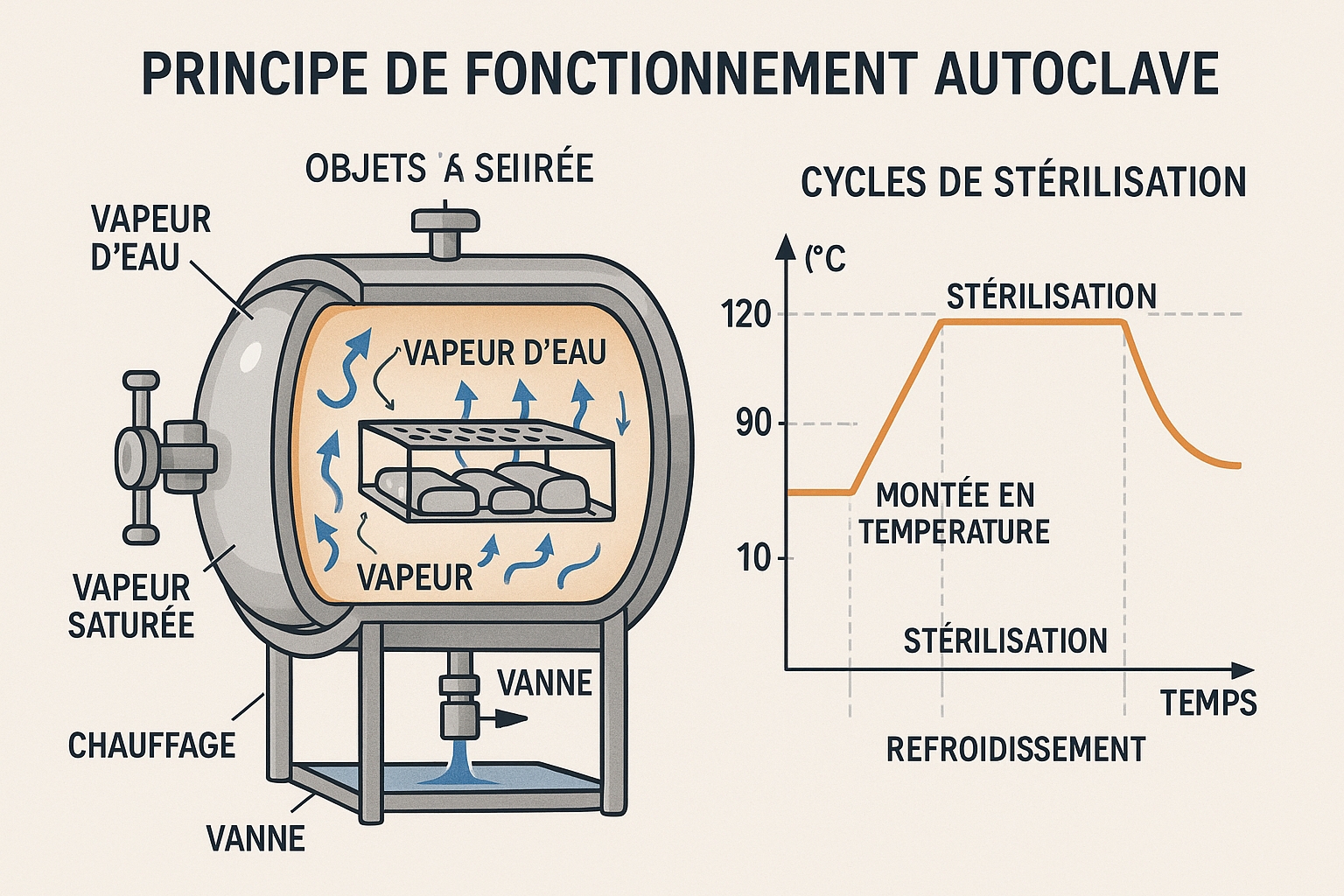
L’autoclavage standard s’articule autour de trois phases distinctes : la phase de montée en température et pression avec évacuation de l’air, la phase de plateau de stérilisation à température et pression constantes, et la phase de refroidissement contrôlé avec retour aux conditions ambiantes. Chaque phase nécessite une surveillance rigoureuse des paramètres critiques pour garantir l’efficacité stérilisante.
Les paramètres standards universellement reconnus incluent une température de 121°C (250°F) maintenue pendant 15-20 minutes sous une pression de 15 psi (1 bar manométrique) pour les charges standard. Les protocoles alternatifs utilisent des températures plus élevées (132°C-135°C) avec des temps d’exposition réduits (3-4 minutes) pour optimiser les cycles sans compromettre l’efficacité. La sélection du protocole dépend de la nature des matériaux traités et des contraintes opérationnelles du laboratoire.
Technologies de Déplacement d’Air et Vide Prévacuum
Les autoclaves à déplacement gravitationnel, technologie traditionnelle, éliminent l’air de la chambre par déplacement naturel avec la vapeur plus dense. Cette méthode simple et fiable convient parfaitement aux charges liquides et à la verrerie de laboratoire, mais peut présenter des limitations pour les charges complexes ou les matériaux poreux nécessitant une pénétration optimale de la vapeur.
Les systèmes pré-vide (prévacuum) utilisent des pompes à vide pour éliminer activement l’air avant injection de la vapeur, garantissant une pénétration homogène dans toutes les structures. Cette technologie avancée excelle dans la stérilisation des textiles, instruments complexes, et charges mixtes, réduisant significativement les temps de cycle tout en améliorant l’efficacité stérilisante.
Systèmes de Contrôle et Monitoring Avancés
Les autoclaves modernes intègrent des systèmes de contrôle microprocesseur sophistiqués surveillant continuellement tous les paramètres critiques. Ces systèmes enregistrent les données de température, pression, et temps avec une résolution temporelle élevée, générant automatiquement des rapports de cycle et des alertes en cas de déviations des paramètres programmés.
L’intégration de capteurs redondants et d’algorithmes de validation en temps réel garantit la détection précoce des anomalies et la sécurité opérationnelle. Les interfaces tactiles modernes facilitent la programmation, la surveillance, et la documentation des cycles, tandis que la connectivité réseau permet l’intégration aux systèmes de gestion laboratoire (LIMS) pour une traçabilité complète.
3. Applications en Microbiologie et Recherche Biomédicale
Stérilisation des Milieux de Culture et Réactifs
La préparation des milieux de culture stériles constitue une application fondamentale de l’autoclave en microbiologie. L’autoclavage élimine tous les contaminants microbiens des bouillons nutritifs, géloses, et milieux spécialisés tout en préservant leurs propriétés nutritionnelles et leur pH optimal. Les protocoles de stérilisation varient selon la composition des milieux, les milieux riches nécessitant des temps plus longs pour compenser l’effet protecteur des protéines.
Les réactifs thermostables (solutions salines, tampons aqueux, eau distillée) bénéficient de l’autoclavage pour garantir leur stérilité sans altération de leurs propriétés chimiques. L’utilisation de contenants appropriés (flacons, erlenmeyers, tubes) avec des systèmes de fermeture permettant l’évacuation de l’air optimise la pénétration de la vapeur et prévient les surpressions dangereuses.
Décontamination des Déchets Biologiques
L’autoclavage constitue la méthode de référence pour la décontamination des déchets biologiques avant élimination, réduisant drastiquement les risques de contamination environnementale et de transmission d’agents pathogènes. Les cultures microbiennes, tissus biologiques, et matériels contaminés nécessitent des cycles prolongés (45-60 minutes à 121°C) pour garantir l’inactivation complète des agents infectieux.
Les protocoles de décontamination varient selon le niveau de confinement biologique des agents traités. Les déchets de niveau BSL-1 et BSL-2 suivent des procédures standard, tandis que les matériels BSL-3 et BSL-4 nécessitent des protocoles renforcés avec validation biologique systématique. La documentation rigoureuse de la décontamination constitue une exigence réglementaire pour la traçabilité et la responsabilité environnementale.
Stérilisation de l’Instrumentation de Laboratoire
La verrerie de laboratoire (pipettes, boîtes de Pétri, erlenmeyers, béchers) représente une catégorie majeure d’équipements nécessitant une stérilisation régulière. L’autoclavage préserve l’intégrité du verre borosilicaté tout en éliminant tous les contaminants microbiens, garantissant la fiabilité des résultats expérimentaux et la sécurité des manipulations.
Les instruments métalliques (pinces, scalpels, seringues réutilisables) tolèrent parfaitement les conditions d’autoclavage standard. L’emballage approprié dans des contenants perméables à la vapeur (papier médical, cassettes perforées) facilite la stérilisation tout en maintenant la stérilité jusqu’à utilisation. Les cycles de séchage prolongés éliminent l’humidité résiduelle susceptible de favoriser la corrosion des métaux sensibles.
4. Validation et Contrôle Qualité de la Stérilisation
Indicateurs Biologiques et Tests de Spores
Les indicateurs biologiques constituent l’étalon-or pour la validation de l’efficacité de la stérilisation, utilisant des spores de Geobacillus stearothermophilus comme micro-organismes test en raison de leur résistance exceptionnelle aux conditions d’autoclavage. Ces spores, présentes à des concentrations standardisées (10⁵ à 10⁶ UFC), doivent être complètement inactivées pour valider l’efficacité du cycle de stérilisation.
Les tests biologiques s’effectuent au minimum hebdomadairement dans les laboratoires de recherche, quotidiennement dans les environnements cliniques critiques, et lors de chaque modification de procédure ou maintenance d’équipement. L’incubation post-autoclavage des indicateurs à 56°C pendant 48 heures révèle la présence éventuelle de spores survivantes par virage colorimétrique ou turbidité du milieu de culture.
Indicateurs Chimiques et Physiques
Les indicateurs chimiques (bandes thermosensibles, pastilles de fusion, encres thermochromiques) fournissent une évaluation rapide de l’exposition aux conditions de stérilisation. Ces dispositifs changent de couleur ou d’état physique lorsqu’ils atteignent des températures spécifiques, offrant une validation immédiate de l’efficacité du cycle sans nécessiter d’incubation prolongée.
Les indicateurs physiques incluent la surveillance continue de la température, pression, et temps via les systèmes de monitoring intégrés. L’enregistrement graphique ou numérique de ces paramètres constitue une documentation légale de la conformité des cycles et facilite l’identification des déviations ou dysfonctionnements potentiels.
Protocoles de Validation et Fréquence des Tests
La validation initiale d’un autoclave nécessite des tests biologiques répétés sur plusieurs cycles consécutifs pour démontrer la reproductibilité et l’efficacité constante. Cette qualification opérationnelle inclut l’évaluation des charges maximales, des configurations de chargement complexes, et des cycles à différentes températures pour établir les limites opérationnelles validées.
La surveillance de routine combine indicateurs biologiques hebdomadaires, indicateurs chimiques quotidiens, et monitoring physique continu. Les déviations détectées déclenchent immédiatement des investigations approfondies, des actions correctives, et une revalidation complète avant la remise en service de l’équipement.
5. Sécurité et Protocoles Opérationnels
Équipements de Protection Individuelle et Mesures Préventives
L’utilisation sécuritaire des autoclaves nécessite des équipements de protection individuelle spécialisés incluant blouses de laboratoire à manches longues, lunettes de sécurité ou écrans faciaux, chaussures fermées, et gants thermo-résistants pour la manipulation des matériels chauds. Ces équipements protègent contre les brûlures par vapeur, les projections de liquides chauds, et les contacts avec des surfaces métalliques surchauffées.
Les mesures préventives incluent l’inspection systématique des joints d’étanchéité, des soupapes de sécurité, et des systèmes de verrouillage avant chaque utilisation. La vérification des niveaux d’eau, de l’intégrité des sondes de température, et du fonctionnement des dispositifs d’alarme prévient les incidents et garantit la fiabilité opérationnelle.
Procédures d’Urgence et Gestion des Incidents
Les protocoles d’urgence définissent les actions immédiates en cas de surpression, de fuite de vapeur, ou de dysfonctionnement des systèmes de sécurité. L’arrêt d’urgence, l’évacuation de la zone, et l’alerte des services techniques constituent les premières mesures avant l’intervention de personnel qualifié pour l’évaluation et la réparation.
La gestion des incidents inclut la documentation détaillée des anomalies, l’analyse des causes racines, et l’implémentation d’actions correctives pour prévenir la récurrence. Les incidents majeurs nécessitent une revalidation complète de l’équipement et une révision des procédures opérationnelles avant la remise en service.
Formation du Personnel et Certification
La formation du personnel couvre les principes de fonctionnement, les procédures opérationnelles standard, la reconnaissance des anomalies, et les mesures d’urgence. Cette formation théorique et pratique doit être régulièrement actualisée pour intégrer les évolutions technologiques et réglementaires.
La certification périodique du personnel garantit la maîtrise des compétences techniques et la conformité aux bonnes pratiques. Les programmes de formation continue incluent les retours d’expérience sur les incidents, les innovations technologiques, et les évolutions des standards de sécurité.
6. Maintenance Préventive et Gestion Technique
Programmes de Maintenance Planifiée
La maintenance préventive des autoclaves suit des calendriers rigoureux incluant des inspections quotidiennes, hebdomadaires, mensuelles, et annuelles selon la complexité des vérifications. Les contrôles quotidiens portent sur les niveaux de fluides, l’état des joints, et le fonctionnement des indicateurs, tandis que les maintenances périodiques incluent la calibration des sondes, le test des soupapes, et l’inspection des composants internes.
Les interventions spécialisées (calibration métrologique, tests d’étanchéité sous pression, validation thermique) nécessitent l’intervention de techniciens certifiés utilisant des équipements de mesure traçables aux étalons nationaux. Ces maintenances préventives prolongent la durée de vie des équipements et garantissent la fiabilité à long terme des performances de stérilisation.
Gestion des Pièces de Rechange et Obsolescence
La gestion préventive des pièces de rechange critique (joints, sondes, vannes de sécurité) évite les arrêts prolongés et maintient la continuité opérationnelle. L’identification des composants critiques, l’établissement de stocks de sécurité, et la planification des remplacements préventifs optimisent la disponibilité des équipements.
La gestion de l’obsolescence technologique inclut la planification des mises à niveau, l’évaluation des technologies de remplacement, et la migration progressive vers des systèmes plus performants. Cette approche proactive évite les ruptures technologiques et maintient la conformité aux évolutions réglementaires.
Documentation et Traçabilité
La documentation exhaustive des maintenances, calibrations, et interventions constitue une exigence réglementaire et une nécessité opérationnelle. Les dossiers techniques incluent les rapports d’intervention, les certificats de calibration, les résultats de validation, et l’historique des modifications pour assurer la traçabilité complète.
Les systèmes de gestion de maintenance assistée par ordinateur (GMAO) facilitent la planification, l’exécution, et le suivi des activités de maintenance. Ces outils informatisés optimisent les coûts, améliorent la fiabilité, et génèrent automatiquement les rapports de conformité réglementaire.
7. Applications Spécialisées et Innovations Technologiques
Autoclaves de Recherche Haute Performance
Les laboratoires de recherche avancée utilisent des autoclaves spécialisés adaptés aux contraintes spécifiques de leurs applications. Les autoclaves haute capacité traitent de gros volumes d’échantillons, tandis que les modèles haute température (150°C-200°C) stérilisent des matériaux résistants ou accélèrent les processus pour optimiser la productivité.
Les autoclaves à cycles programmables offrent une flexibilité maximale avec des profils température-temps personnalisés selon les matériaux traités. Ces systèmes intègrent des rampes de montée et descente en température contrôlées, des paliers multiples, et des cycles de séchage adaptés aux exigences spécifiques de chaque application de recherche.
Technologies Émergentes et Automatisation
L’automatisation croissante intègre des systèmes de chargement-déchargement robotisés, des convoyeurs automatiques, et des interfaces avec les systèmes de gestion laboratoire (LIMS). Ces innovations réduisent la manipulation manuelle, minimisent les risques de contamination croisée, et optimisent l’efficacité opérationnelle des laboratoires haute productivité.
Les technologies émergentes incluent la stérilisation assistée par micro-ondes, les systèmes plasma-vapeur hybrides, et les autoclaves à induction électromagnétique. Ces innovations visent à réduire les temps de cycle, améliorer l’efficacité énergétique, et traiter des matériaux sensibles impossibles à autoclaver conventionnellement.
Intégration IoT et Intelligence Artificielle
L’Internet des Objets (IoT) révolutionne la surveillance des autoclaves avec des capteurs connectés transmettant en temps réel les données opérationnelles vers des plateformes cloud. Cette connectivité facilite la maintenance prédictive, la surveillance à distance, et l’optimisation des performances par analyse des données historiques.
L’intelligence artificielle appliquée aux données d’autoclavage identifie les patterns anomaliques, prédit les défaillances potentielles, et optimise automatiquement les paramètres de cycles. Ces algorithmes d’apprentissage automatique améliorent continuellement les performances tout en réduisant les coûts opérationnels et les risques d’incidents.
8. Réglementation et Conformité
Standards Internationaux et Certifications
Les autoclaves de laboratoire doivent respecter de nombreux standards internationaux incluant ISO 17665 pour la stérilisation vapeur, ASME BPVC pour la construction des appareils sous pression, et EN 285 pour les autoclaves hospitaliers. Ces normes définissent les exigences de conception, fabrication, installation, et validation pour garantir la sécurité et l’efficacité.
Les certifications CE (Europe), FDA (États-Unis), et Health Canada valident la conformité réglementaire et autorisent la commercialisation dans les juridictions respectives. L’obtention et le maintien de ces certifications nécessitent des audits réguliers, des mises à jour documentaires, et la démonstration continue de la conformité aux évolutions réglementaires.
Bonnes Pratiques de Laboratoire (BPL)
Les Bonnes Pratiques de Laboratoire imposent des exigences strictes pour l’utilisation, la maintenance, et la documentation des autoclaves dans les études réglementaires. Ces standards couvrent la qualification des équipements, la formation du personnel, la validation des méthodes, et la traçabilité complète des opérations.
La conformité BPL nécessite des procédures opérationnelles standardisées (SOP), des systèmes de gestion documentaire validés, et des audits internes réguliers. Les inspections réglementaires vérifient l’application rigoureuse de ces standards et peuvent imposer des actions correctives en cas de non-conformités.
Évolutions Réglementaires et Adaptation
L’évolution constante des réglementations internationales nécessite une veille réglementaire active et une adaptation continue des pratiques. Les nouvelles exigences de cybersécurité pour les équipements connectés, les standards environnementaux renforcés, et les protocoles de gestion des risques émergents transforment progressivement les pratiques d’exploitation.
L’anticipation des évolutions réglementaires par la participation aux groupes de travail normatifs, la collaboration avec les organismes certificateurs, et l’investissement dans les technologies conformes garantit la pérennité des opérations et évite les obsolescences prématurées.
9. Considérations Économiques et Optimisation
Analyse Coût-Bénéfice et Retour sur Investissement
L’évaluation économique des autoclaves intègre les coûts d’acquisition, d’installation, d’exploitation, et de maintenance sur la durée de vie complète de l’équipement. Cette analyse total cost of ownership (TCO) guide les décisions d’investissement et compare objectivement les alternatives technologiques disponibles.
Le retour sur investissement inclut les gains de productivité, la réduction des coûts de décontamination externe, l’amélioration de la sécurité biologique, et la conformité réglementaire. Les laboratoires à forte activité rentabilisent rapidement leurs investissements en autoclaves haute performance grâce aux gains d’efficacité et de fiabilité.
Optimisation Énergétique et Durabilité
Les autoclaves modernes intègrent des technologies d’optimisation énergétique incluant la récupération de chaleur, l’isolation thermique renforcée, et les systèmes de gestion intelligente de l’énergie. Ces innovations réduisent significativement les coûts opérationnels tout en diminuant l’empreinte environnementale.
La durabilité environnementale considère l’efficacité énergétique, la consommation d’eau, les émissions de vapeur, et la recyclabilité des matériaux de construction. Les certifications environnementales (Energy Star, LEED) valorisent ces performances et influencent progressivement les décisions d’achat des organisations soucieuses de responsabilité environnementale.
Stratégies d’Acquisition et de Financement
Les stratégies d’acquisition incluent l’achat direct, la location-financement, et les contrats de service complets intégrant équipement, maintenance, et consommables. Cette flexibilité contractuelle s’adapte aux contraintes budgétaires et aux besoins opérationnels spécifiques de chaque organisation.
Les modèles de financement innovants proposent des paiements basés sur l’utilisation, des garanties de performance, et des contrats de résultat liant la rémunération aux performances réelles. Ces approches partenariales optimisent les coûts tout en transférant les risques techniques vers des spécialistes expérimentés.
10. Perspectives d’Évolution et Innovations Futures
Technologies de Stérilisation Avancées
L’évolution technologique explore des alternatives et améliorations à l’autoclavage traditionnel, incluant la stérilisation par plasma froid, les rayonnements ionisants pulsés, et les champs électriques haute fréquence. Ces technologies visent à traiter des matériaux thermosensibles tout en maintenant l’efficacité microbicide de l’autoclavage.
Les systèmes hybrides combinent plusieurs mécanismes stérilisants (vapeur + ozone, température + UV-C, pression + plasma) pour optimiser l’efficacité tout en réduisant l’agressivité du traitement. Ces innovations permettent l’élargissement du spectre des matériaux stérilisables et l’amélioration des performances énergétiques.
Intelligence Artificielle et Optimisation Prédictive
L’intelligence artificielle révolutionne la gestion des autoclaves par l’analyse prédictive des données opérationnelles, l’optimisation automatique des cycles, et la maintenance prédictive basée sur l’apprentissage automatique. Ces systèmes intelligents améliorent continuellement leurs performances en analysant les patterns d’utilisation et les corrélations entre paramètres opérationnels et résultats.
Les algorithmes d’optimisation multicritères équilibrent automatiquement efficacité stérilisante, durée de cycle, consommation énergétique, et impact sur les matériaux traités. Cette optimisation dynamique s’adapte en temps réel aux conditions opérationnelles et aux objectifs de performance définis par les utilisateurs.
Conclusion
L’autoclave demeure un pilier incontournable de la microbiologie moderne, évoluant continuellement pour intégrer les innovations technologiques tout en préservant sa fiabilité fondamentale et son efficacité universellement reconnue. Son rôle critique dans la sécurité biologique, la qualité de la recherche, et la conformité réglementaire en fait un investissement stratégique pour toute organisation manipulant des agents biologiques.
L’avenir de l’autoclavage s’oriente vers une intégration croissante des technologies numériques, une optimisation énergétique renforcée, et une automatisation intelligente préservant l’intervention humaine pour les décisions critiques. Cette évolution technologique maintient l’autoclave au cœur des stratégies de biosécurité tout en s’adaptant aux exigences contemporaines de durabilité, d’efficacité, et de traçabilité.
La maîtrise des principes, des technologies, et des bonnes pratiques d’autoclavage constitue donc une compétence fondamentale pour tous les professionnels de la microbiologie, contribuant à l’excellence scientifique et à la sécurité des manipulations biologiques dans un monde où les enjeux de biosécurité ne cessent de croître en complexité et en importance.
OTOSCOPE WELCH ALLYN MACROVIEW