Blog
LE PRINCIPE DE L’AUTOCLAVE : UN GUIDE COMPLET

INTRODUCTION
L’autoclave représente l’une des technologies de stérilisation les plus fiables et les plus largement utilisées dans le monde moderne. Depuis son invention au XIXe siècle, cet équipement essentiel a révolutionné les pratiques d’hygiène et de sécurité dans de nombreux secteurs, notamment les soins de santé, la recherche scientifique, l’industrie pharmaceutique et l’industrie alimentaire. Ce guide complet explore en détail les principes fondamentaux, le fonctionnement, les applications et les meilleures pratiques liées à l’utilisation des autoclaves.
La stérilisation par autoclave repose sur un principe scientifique éprouvé : l’utilisation combinée de la chaleur, de la pression et de l’humidité pour éliminer de manière fiable tous les micro-organismes pathogènes, y compris les spores bactériennes les plus résistantes. Cette méthode de stérilisation, également connue sous le nom de stérilisation à la vapeur saturée, offre un niveau de sécurité incomparable pour la décontamination des instruments médicaux, des équipements de laboratoire et de nombreux autres matériaux.
Dans un contexte où les infections nosocomiales représentent un défi majeur pour la santé publique et où les exigences réglementaires en matière de qualité et de sécurité ne cessent de se renforcer, la compréhension approfondie des principes de fonctionnement des autoclaves devient cruciale. Ce guide s’adresse aux professionnels de santé, aux techniciens de laboratoire, aux ingénieurs biomédicaux, aux responsables qualité et à tous ceux qui travaillent avec des autoclaves dans leur pratique professionnelle.

CHAPITRE 1 : PRINCIPES FONDAMENTAUX DE LA STÉRILISATION PAR AUTOCLAVE
1.1 Définition et concept de base
L’autoclave est un dispositif de stérilisation qui utilise de la vapeur d’eau saturée sous pression pour détruire tous les micro-organismes présents sur ou dans les objets traités. Le principe repose sur l’action létale de la chaleur humide, qui dénature les protéines et détruit les structures cellulaires des micro-organismes, incluant les bactéries, virus, champignons et spores.
La stérilisation se distingue de la désinfection par son caractère absolu : elle vise à éliminer 100% des formes de vie microbienne, y compris les spores bactériennes, qui constituent les formes de résistance les plus difficiles à éliminer. Cette efficacité totale est quantifiée par le concept de SAL (Sterility Assurance Level), généralement fixé à 10⁻⁶, ce qui signifie une probabilité d’un organisme viable sur un million d’articles traités.
1.2 Mécanismes de destruction microbienne
La destruction des micro-organismes par la chaleur humide s’effectue selon plusieurs mécanismes complémentaires :
Dénaturation protéique : Les températures élevées provoquent la rupture des liaisons hydrogène et des ponts disulfure dans les protéines, entraînant leur dénaturation irréversible. Cette altération structurelle rend les enzymes vitales non fonctionnelles, conduisant à la mort cellulaire.
Coagulation des protéines cytoplasmiques : La chaleur provoque la coagulation des protéines intracellulaires, perturbant les processus métaboliques essentiels.
Altération des membranes cellulaires : L’action combinée de la chaleur et de l’humidité modifie la perméabilité des membranes cellulaires, perturbant l’équilibre osmotique et conduisant à la lyse cellulaire.
Hydrolyse des acides nucléiques : Les températures élevées en présence d’humidité favorisent l’hydrolyse des liaisons phosphodiester dans l’ADN et l’ARN, compromettant la reproduction et la survie cellulaire.
1.3 Importance de la vapeur saturée
La vapeur saturée présente des propriétés uniques qui en font l’agent stérilisant idéal :
Pouvoir pénétrant élevé : La vapeur peut pénétrer dans les zones difficiles d’accès, assurant une stérilisation homogène même dans les espaces confinés.
Transfert de chaleur efficace : La condensation de la vapeur libère une quantité considérable d’énergie thermique (chaleur latente de vaporisation), permettant un réchauffement rapide et uniforme des objets.
Absence de résidus toxiques : Contrairement aux agents chimiques, la vapeur ne laisse aucun résidu nocif après le processus de stérilisation.
Compatibilité environnementale : L’utilisation de vapeur d’eau respecte l’environnement et ne génère pas de déchets dangereux.
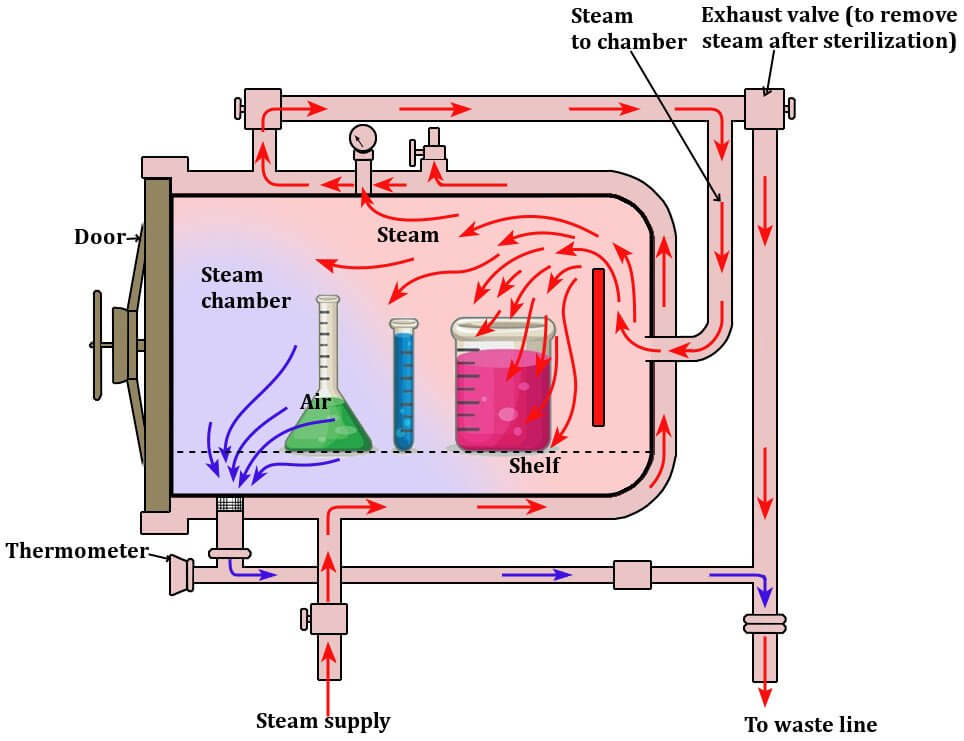
CHAPITRE 2 : THERMODYNAMIQUE ET CYCLES DE STÉRILISATION
2.1 Principes thermodynamiques
La compréhension des principes thermodynamiques est essentielle pour optimiser l’efficacité des cycles de stérilisation. La relation entre température, pression et état de la vapeur est décrite par les tables de vapeur saturée et les diagrammes de Mollier.
Température et pression de saturation : À chaque pression correspond une température de saturation spécifique. Par exemple :
- À 1 bar absolu : 121°C
- À 2 bar absolu : 134°C
- À 3 bar absolu : 143°C
Qualité de la vapeur : La vapeur utilisée pour la stérilisation doit être « saturée sèche » avec un titre en vapeur proche de 1 (100% vapeur). La présence d’eau liquide (vapeur humide) ou de surchauffe (vapeur surchauffée) réduit considérablement l’efficacité du processus Energie Plus.
2.2 Paramètres critiques de stérilisation
Les paramètres fondamentaux qui déterminent l’efficacité de la stérilisation sont :
Température : Les températures standard pour la stérilisation hospitalière sont :
- 121°C pendant 15-20 minutes (minimum pratique)
- 126°C pendant 10-15 minutes
- 134°C pendant 3-10 minutes
Temps d’exposition : Le temps nécessaire varie selon la température et la résistance thermique des micro-organismes cibles.
Pression : Maintient la vapeur à l’état saturé à la température requise et facilite la pénétration dans les matériaux poreux.
Humidité : La présence d’humidité est indispensable pour l’efficacité de la destruction microbienne.
2.3 Phases du cycle de stérilisation
Un cycle de stérilisation standard comprend plusieurs phases distinctes :

Phase de prétraitement (purge) : Élimination de l’air de la chambre par pompage ou déplacement gravitaire. Cette étape est cruciale car la présence d’air forme des poches isolantes qui protègent les micro-organismes de l’action de la vapeur.
Phase de montée en température : Injection de vapeur pour atteindre progressivement les conditions de stérilisation. La température et la pression augmentent simultanément jusqu’aux valeurs cibles.
Phase de stérilisation (plateau) : Maintien des conditions de température et pression pendant la durée requise. C’est pendant cette phase que s’effectue la destruction des micro-organismes.
Phase de refroidissement : Abaissement contrôlé de la température et de la pression pour éviter les chocs thermiques et la formation de condensats excessifs.
Phase de séchage : Élimination de l’humidité résiduelle par application d’un vide partiel et/ou circulation d’air filtré stérile.
CHAPITRE 3 : TYPES D’AUTOCLAVES ET LEURS APPLICATIONS
3.1 Classification par méthode d’évacuation de l’air
Autoclaves à déplacement par gravité (Classe N) Ces autoclaves éliminent l’air par déplacement gravitaire : la vapeur plus chaude et moins dense chasse l’air froid vers le bas et l’évacue par un drain. Ils conviennent pour la stérilisation d’objets solides non emballés et de liquides en contenants ouverts.
Avantages :
- Simplicité de conception et d’utilisation
- Coût d’acquisition et de maintenance réduit
- Fiabilité éprouvée
Limitations :
- Évacuation incomplète de l’air dans les charges complexes
- Temps de cycle relativement longs
- Applications limitées aux charges simples
Autoclaves à pré-vide (Classe B) Ces systèmes utilisent une pompe à vide pour évacuer efficacement l’air avant l’injection de vapeur. Cette technologie permet une pénétration optimale de la vapeur dans tous les types de charges, y compris les matériaux poreux, les objets creux et les emballages étanches.

Avantages :
- Évacuation complète de l’air
- Stérilisation efficace de tous types de charges
- Cycles plus courts
- Séchage amélioré
Applications typiques :
- Instruments chirurgicaux emballés
- Matériaux poreux (textiles, caoutchouc)
- Dispositifs à lumière étroite
- Charges complexes et hétérogènes
Autoclaves de classe S Catégorie intermédiaire définie par le fabricant, avec des spécifications particulières selon les applications visées.
3.2 Classification par taille et application
Autoclaves de paillasse (8-50 litres) Destinés aux petits laboratoires, cabinets médicaux et dentaires. Ils offrent une solution compacte et économique pour des volumes de stérilisation modérés.
Autoclaves de laboratoire (50-200 litres) Conçus pour les laboratoires de recherche et d’analyse, ces autoclaves combinent polyvalence et performance pour des applications variées.
Autoclaves hospitaliers (200-1000 litres) Équipements de grande capacité pour les blocs opératoires et les centrales de stérilisation hospitalières. Ils intègrent des systèmes de contrôle avancés et des fonctionnalités de traçabilité.
Autoclaves industriels (>1000 litres) Installations de production pour l’industrie pharmaceutique, alimentaire et de recherche, conçues pour des volumes importants et des exigences réglementaires strictes.

3.3 Systèmes spécialisés
Autoclaves à vapeur fluante Pour la stérilisation de liquides thermolabiles, ces systèmes maintiennent une pression constante pendant le refroidissement pour éviter l’ébullition.
Autoclaves à injection d’eau Utilisés pour les produits en solution nécessitant un refroidissement rapide et contrôlé.
Tunnels de stérilisation Systèmes continus pour la stérilisation à grande échelle de flacons, ampoules et autres contenants dans l’industrie pharmaceutique.
CHAPITRE 4 : VALIDATION ET CONTRÔLE QUALITÉ
4.1 Cadre réglementaire et normatif
La validation des autoclaves s’inscrit dans un cadre réglementaire strict, particulièrement dans les secteurs pharmaceutique et médical :
Norme EN 285 : Standard européen pour les autoclaves à vapeur, définissant les exigences de performance, d’essai et de marquage.
ISO 17665 : Norme internationale pour la stérilisation des dispositifs médicaux par chaleur humide.
FDA 21 CFR Part 820 : Réglementation américaine sur les bonnes pratiques de fabrication des dispositifs médicaux.
ICH Q7 : Lignes directrices sur les bonnes pratiques de fabrication des substances actives pharmaceutiques Ellab.
4.2 Processus de validation
La validation d’un autoclave suit une approche structurée en quatre phases :
Design Qualification (DQ) : Vérification que la conception de l’équipement répond aux spécifications requises et aux standards applicables.
Installation Qualification (IQ) : Contrôle de l’installation correcte de l’équipement selon les spécifications du fabricant et les bonnes pratiques.
Operational Qualification (OQ) : Démonstration que l’équipement fonctionne conformément aux paramètres spécifiés dans toutes les conditions d’utilisation prévues.
Performance Qualification (PQ) : Validation que l’équipement produit de manière reproductible des résultats conformes aux spécifications avec des charges réelles.

4.3 Tests de validation essentiels
Test de distribution thermique (Heat Distribution Test) Évalue l’homogénéité de température dans la chambre vide à l’aide de multiples sondes calibrées.
Test de pénétration thermique (Heat Penetration Test) Mesure le temps nécessaire pour atteindre la température de stérilisation au cœur des charges les plus défavorables.
Tests de qualité vapeur
- Test de non-condensabilité : mesure des gaz non condensables
- Test de surchauffe : vérification de l’absence de vapeur surchauffée
- Test de sécheresse : évaluation du titre en vapeur
Tests biologiques (Bio-challenge) Utilisation de spores de Geobacillus stearothermophilus (résistantes à 121°C) ou Bacillus atrophaeus (résistantes à des températures plus élevées) pour démontrer l’efficacité létale du processus.
Calcul de la valeur stérilisatrice F₀ Quantification de l’effet létal cumulé du cycle, exprimée en minutes équivalentes à 121°C avec un Z de 10°C.
4.4 Contrôles de routine
Indicateurs physiques Surveillance continue des paramètres température, pression et temps par des systèmes d’enregistrement calibrés.
Indicateurs chimiques Utilisation de témoins chimiques qui changent de couleur ou d’état sous l’effet des conditions de stérilisation (classes 1 à 6 selon ISO 11140).
Indicateurs biologiques Tests périodiques avec des spores standardisées pour vérifier l’efficacité biologique du processus.
Tests Bowie-Dick Contrôle quotidien de l’évacuation de l’air et de la pénétration de vapeur dans les autoclaves à pré-vide.
CHAPITRE 5 : APPLICATIONS SECTORIELLES
5.1 Secteur hospitalier et médical
Dans le domaine médical, les autoclaves constituent l’épine dorsale de la lutte contre les infections nosocomiales. Leurs applications incluent :
Stérilisation des instruments chirurgicaux
- Instruments métalliques réutilisables
- Textiles chirurgicaux (blouses, champs, compresses)
- Dispositifs implantables
- Équipements d’anesthésie et de réanimation
Stérilisation des dispositifs médicaux
- Endoscopes thermorésistants
- Matériel de dialyse
- Équipements de laboratoire médical
- Dispositifs de perfusion et de transfusion
Les protocoles hospitaliers exigent une traçabilité complète, incluant l’enregistrement des paramètres de chaque cycle, l’identification des charges et la documentation des contrôles qualité.

5.2 Industrie pharmaceutique
L’industrie pharmaceutique utilise les autoclaves pour garantir la stérilité des produits et équipements dans le respect des BPF (Bonnes Pratiques de Fabrication) :
Stérilisation des récipients
- Flacons, ampoules et seringues en verre
- Bouchons et systèmes de fermeture
- Équipements de conditionnement
Stérilisation des matières premières
- Excipients thermostables
- Solutions injectables
- Milieux de culture pour les contrôles microbiologiques
Dépyrogénation Élimination des endotoxines bactériennes par exposition à des températures élevées (250-300°C) dans des fours spécialisés combinant stérilisation et dépyrogénation.
5.3 Laboratoires de recherche
Les laboratoires utilisent les autoclaves pour multiples applications :
Préparation de milieux stériles
- Milieux de culture microbiologique
- Solutions tampons et réactifs
- Matériel de laboratoire (pipettes, boîtes de Petri)
Décontamination des déchets
- Déchets biologiques infectieux
- Cultures microbiennes
- Matériel souillé par des agents pathogènes
Recherche en biotechnologie
- Stérilisation d’équipements de fermentation
- Préparation d’environnements aseptiques
- Validation de procédés biotechnologiques
5.4 Industrie alimentaire
Bien que moins répandue que dans le secteur médical, la stérilisation par autoclave trouve des applications spécifiques dans l’industrie alimentaire :
Conservation des aliments
- Produits en conserve thermostables
- Préparations pour nourrissons
- Compléments nutritionnels liquides
Stérilisation des équipements
- Lignes de conditionnement aseptique
- Réservoirs et tuyauteries
- Matériel de contrôle qualité
CHAPITRE 6 : MAINTENANCE ET OPTIMISATION
6.1 Programme de maintenance préventive
Un programme de maintenance rigoureusement structuré est essentiel pour garantir la fiabilité et la longévité des autoclaves :
Maintenance quotidienne
- Inspection visuelle de l’état général
- Vérification des niveaux d’eau
- Nettoyage de la chambre et des accessoires
- Contrôle des systèmes de sécurité
Maintenance hebdomadaire
- Test des systèmes d’alarme
- Vérification des joints et étanchéités
- Contrôle des dispositifs de mesure
- Nettoyage des filtres
Maintenance mensuelle
- Calibration des sondes de température et pression
- Vérification des pompes à vide
- Contrôle des systèmes de génération vapeur
- Test des cycles de sécurité
Maintenance annuelle
- Validation complète des performances
- Remplacement des pièces d’usure
- Mise à jour des logiciels de contrôle
- Formation du personnel utilisateur

6.2 Optimisation énergétique
L’optimisation de la consommation énergétique représente un enjeu économique et environnemental majeur :
Récupération de chaleur
- Récupération de la vapeur de détente
- Préchauffage de l’eau d’alimentation
- Systèmes de cogénération
Isolation thermique renforcée
- Matériaux isolants haute performance
- Réduction des ponts thermiques
- Optimisation de la conception des enceintes
Systèmes de contrôle avancés
- Régulation PID optimisée
- Programmation de cycles économiques
- Monitoring énergétique en temps réel
6.3 Gestion des consommables et utilités
Qualité de l’eau L’eau utilisée doit répondre à des spécifications strictes :
- Eau purifiée selon Ph. Eur. ou USP
- Conductivité < 5 µS/cm
- Teneur en chlorures < 2 ppm
- Teneur en silice < 1 ppm
Génération et distribution vapeur
- Chaudières à vapeur propre
- Réseaux de distribution isolés
- Systèmes de traitement des condensats
- Monitoring de la qualité vapeur
CHAPITRE 7 : INNOVATIONS TECHNOLOGIQUES ET TENDANCES FUTURES
7.1 Digitalisation et Industry 4.0
L’intégration des technologies numériques transforme la gestion des autoclaves :
Systèmes de monitoring connectés
- Surveillance à distance des paramètres critiques
- Analyses prédictives des pannes
- Optimisation automatique des cycles
- Intégration dans les systèmes LIMS/MES
Intelligence artificielle
- Algorithmes d’apprentissage automatique pour l’optimisation
- Détection précoce des anomalies
- Prédiction des besoins de maintenance
- Analyse de tendances et reporting automatisé
Blockchain et traçabilité
- Enregistrement inaltérable des données de stérilisation
- Traçabilité end-to-end des lots
- Certification numérique de conformité
- Audit trail sécurisé
7.2 Développements technologiques avancés
Stérilisation par plasma Technologies émergentes utilisant des plasmas froids pour la stérilisation de matériaux thermosensibles.
Systèmes hybrides Combinaison de différentes technologies (vapeur, plasma, rayonnements) pour optimiser efficacité et polyvalence.
Nanotechnologies Application de nanomatériaux pour améliorer les performances thermiques et la résistance à la corrosion.
7.3 Durabilité et impact environnemental
Réduction de l’empreinte carbone
- Cycles optimisés pour réduire la consommation énergétique
- Utilisation d’énergies renouvelables
- Conception écoresponsable des équipements
Gestion des déchets
- Minimisation des consommables
- Recyclage des matériaux
- Traitement écologique des effluents
CHAPITRE 8 : BONNES PRATIQUES ET RECOMMANDATIONS
8.1 Formation et compétences du personnel
La formation du personnel constitue un facteur critique de succès :
Formation initiale
- Principes de la stérilisation
- Fonctionnement des équipements
- Procédures opérationnelles standard
- Gestion des situations d’urgence
Formation continue
- Mise à jour réglementaire
- Nouvelles technologies
- Amélioration continue des processus
- Partage d’expériences et best practices
Certification et qualification
- Programmes de certification professionnelle
- Évaluations périodiques des compétences
- Documentation des formations
- Matrice de compétences
8.2 Gestion des risques
Analyse des risques (AMDEC)
- Identification des modes de défaillance
- Évaluation de la criticité
- Mise en place de mesures préventives
- Monitoring des risques résiduels
Plan de continuité d’activité
- Équipements de secours
- Procédures dégradées
- Partenariats de sous-traitance
- Stocks de sécurité
8.3 Amélioration continue
Indicateurs de performance
- Taux de réussite des cycles
- Disponibilité des équipements
- Consommations énergétiques
- Coûts de maintenance
Benchmarking
- Comparaison avec les meilleures pratiques sectorielles
- Échanges avec d’autres établissements
- Participation à des groupes de travail
- Veille technologique active

CONCLUSION
L’autoclave demeure un équipement incontournable pour garantir la sécurité microbiologique dans de nombreux secteurs d’activité. Sa fiabilité éprouvée, combinée aux innovations technologiques récentes, en fait un outil essentiel pour relever les défis contemporains de la stérilisation.
L’évolution vers des systèmes plus intelligents, plus efficaces énergétiquement et mieux intégrés dans les écosystèmes numériques ouvre de nouvelles perspectives d’optimisation. Cependant, le succès de ces technologies dépend fondamentalement de la maîtrise des principes de base, d’une maintenance rigoureuse et d’un personnel qualifié.
Face aux enjeux croissants de sécurité sanitaire, de qualité et de durabilité, les professionnels doivent continuer à développer leurs compétences et à adopter les meilleures pratiques. L’autoclave, loin d’être une technologie figée, continue d’évoluer pour répondre aux exigences toujours plus strictes de notre époque.
L’investissement dans la formation, la validation, la maintenance et l’innovation technologique constitue la clé du succès pour optimiser l’utilisation des autoclaves et garantir des résultats de stérilisation fiables et reproductibles. En adoptant une approche proactive et en intégrant les dernières avancées technologiques, les organisations peuvent non seulement améliorer leur efficacité opérationnelle mais aussi contribuer à l’amélioration globale de la sécurité sanitaire.
Sources et références :
- Energie Plus – Cycle de la vapeur de stérilisation
- CIMEdentaire – Principe de stérilisation par autoclave
- Ellab – Steam Sterilization Qualification & Validation
- Normes EN 285, ISO 17665, FDA 21 CFR Part 820
