⚠️QUAND LES INSTRUMENTS MÉDICAUX VONT À L’AUTOCLAVE SANS ÊTRE NETTOYÉS:CONSÉQUENCES CATASTROPHIQUES

Instruments chirurgicaux contaminés par du sang et des débris organiques – une menace directe pour la sécurité des patients si stérilisés sans nettoyage préalable
I. Le Principe Fondamental Violé : « Nettoyer d’Abord, Stériliser Ensuite »
Dans le monde de la stérilisation médicale, il existe un principe absolu et inviolable : « On ne peut pas stériliser la saleté » (You cannot sterilize dirt). Cette maxime, répétée dans tous les programmes de formation en stérilisation à travers le monde, résume une vérité biologique et physique fondamentale : la stérilisation n’est efficace que sur des instruments propres.
1.1 Pourquoi le Nettoyage Est-il Absolument Indispensable ?
Le nettoyage préalable à la stérilisation n’est pas une simple « bonne pratique » ou une recommandation optionnelle. C’est une nécessité absolue pour quatre raisons scientifiques critiques :
Les matières organiques (sang, tissus, mucus, pus) et inorganiques (sels minéraux, résidus médicamenteux) forment une barrière physique qui protège les micro-organismes des agents stérilisants. Imaginez des bactéries « encapsulées » dans une matrice de protéines coagulées et de débris cellulaires – la vapeur d’eau de l’autoclave ne peut tout simplement pas les atteindre.
Mécanisme : Les protéines sanguines (albumine, globulines) coagulent sous l’effet de la chaleur initiale de l’autoclave, créant une croûte dure qui isole les micro-organismes du contact direct avec la vapeur stérilisante. Les spores bactériennes, déjà naturellement résistantes, deviennent pratiquement invulnérables lorsqu’elles sont emprisonnées dans ces débris organiques.
Lorsque des instruments contaminés ne sont pas nettoyés rapidement (dans les 30 minutes idéalement, maximum 2 heures), les bactéries commencent à former des biofilms – des communautés microbiennes structurées enveloppées dans une matrice auto-produite de polysaccharides, protéines et ADN.
Résistance extrême : Les biofilms sont 1000 fois plus résistants aux désinfectants et stérilisants que les bactéries planctoniques (flottantes). La matrice extracellulaire du biofilm agit comme un bouclier impénétrable. Les bactéries à l’intérieur du biofilm entrent également dans un état métabolique ralenti, les rendant moins vulnérables aux agents antimicrobiens qui ciblent les cellules en croissance active.
Micro-organismes formant des biofilms : Pseudomonas aeruginosa, Staphylococcus aureus (y compris SARM), Enterococcus, Escherichia coli, Candida albicans (levure).

Image au microscope électronique à balayage d’un biofilm de Staphylococcus aureus – structure complexe protégeant les bactéries contre la stérilisation
La bioburden (charge biologique) désigne le nombre de micro-organismes viables présents sur un instrument avant la stérilisation. Plus cette charge est élevée, plus le processus de stérilisation doit être intense et prolongé pour garantir la destruction complète.
Principe du SAL (Sterility Assurance Level) : La stérilisation vise un niveau d’assurance de stérilité de 10⁻⁶ (une chance sur un million qu’un micro-organisme survive). Ce calcul repose sur une réduction logarithmique de la population microbienne. Si on commence avec 10⁶ bactéries au lieu de 10² (charge après nettoyage), il faudrait un cycle de stérilisation 10 000 fois plus long pour atteindre le même SAL – ce qui est évidemment impossible sans endommager les instruments.
Normes internationales :
- ISO 14937 : Exige une réduction de la bioburden par le nettoyage avant stérilisation
- AAMI ST79 (USA) : Recommande une bioburden <250 UFC (unités formant colonies) après nettoyage
- EN 285 (Europe) : Nécessite validation du processus de nettoyage
Les prions – agents responsables des maladies à prions comme la maladie de Creutzfeldt-Jakob (MCJ), variante de la « maladie de la vache folle » – représentent la menace ultime en stérilisation. Ces protéines mal repliées sont :
- Résistantes aux températures extrêmes : Survivent à 134°C pendant 18 minutes
- Résistantes aux radiations : UV, gamma, pas d’effet
- Résistantes aux désinfectants classiques : Alcools, aldéhydes, peroxyde inefficaces
- Résistantes à la dessiccation : Restent infectieux pendant des années à sec
Seul le nettoyage mécanique vigoureux peut éliminer physiquement les prions des surfaces d’instruments. Une fois « cuits » et fixés par un autoclavage sur instruments sales, les prions deviennent quasiment impossibles à éliminer. Les CDC (USA) et l’OMS recommandent la destruction par incinération d’instruments contaminés par des prions et non correctement nettoyés.
Une étude de 2020 a montré que la stérilisation par vapeur (autoclave) échoue dans 76% des cas lorsque les instruments sont souillés de sang ou de sels minéraux non nettoyés.
Source : CDC – « Poor Cleaning Can Jeopardize Sterilization »
II. Conséquences Médicales Catastrophiques : Infections et Transmission de Maladies
2.1 Infections du Site Opératoire (ISO / SSI)
Les infections du site opératoire (ISO en français, SSI – Surgical Site Infections en anglais) représentent la complication la plus fréquente et la plus coûteuse liée à l’utilisation d’instruments insuffisamment stérilisés.
• Europe : 2-5% de toutes les chirurgies (données ECDC 2024)
• USA : 157 500 ISO/an, coût de 3,5 milliards USD (CDC 2024)
• Japon : 1,2% des chirurgies (taux le plus bas, hygiène stricte)
• Chine : 3-8% selon les hôpitaux (variation importante)
• Inde : 8-15% dans certains centres (problèmes d’infrastructure)
• Mortalité : 3% des ISO sévères entraînent le décès du patient
🦠 Micro-organismes Pathogènes Transmis par Instruments Contaminés :
Bactéries aérobies :
• Staphylococcus aureus (dont SARM) – 30% des ISO
• Pseudomonas aeruginosa – 8% des ISO, hautement résistant
• Escherichia coli – 10% des ISO abdominales
• Klebsiella pneumoniae – résistance aux carbapénèmes (cauchemar)
• Acinetobacter baumannii – « superbactérie » hospitalière
Bactéries anaérobies :
• Clostridium difficile – diarrhée post-opératoire sévère
• Bacteroides fragilis – abcès profonds
Mycobactéries :
• Mycobacterium tuberculosis – transmission possible si instruments non stérilisés
• Mycobacterium chelonae – infections post-chirurgie esthétique
Champignons :
• Candida albicans – infections systémiques chez immunodéprimés
• Aspergillus spp. – infections pulmonaires gravissimes
Virus :
• VIH (Virus de l’Immunodéficience Humaine)
• VHB (Virus de l’Hépatite B) – résiste 7 jours sur instruments secs
• VHC (Virus de l’Hépatite C)
• HPV (Papillomavirus Humain) – transmission instruments gynécologiques
Prions :
• Maladie de Creutzfeldt-Jakob (MCJ) – toujours fatale
• Variante MCJ (vache folle) – incubation 10-50 ans
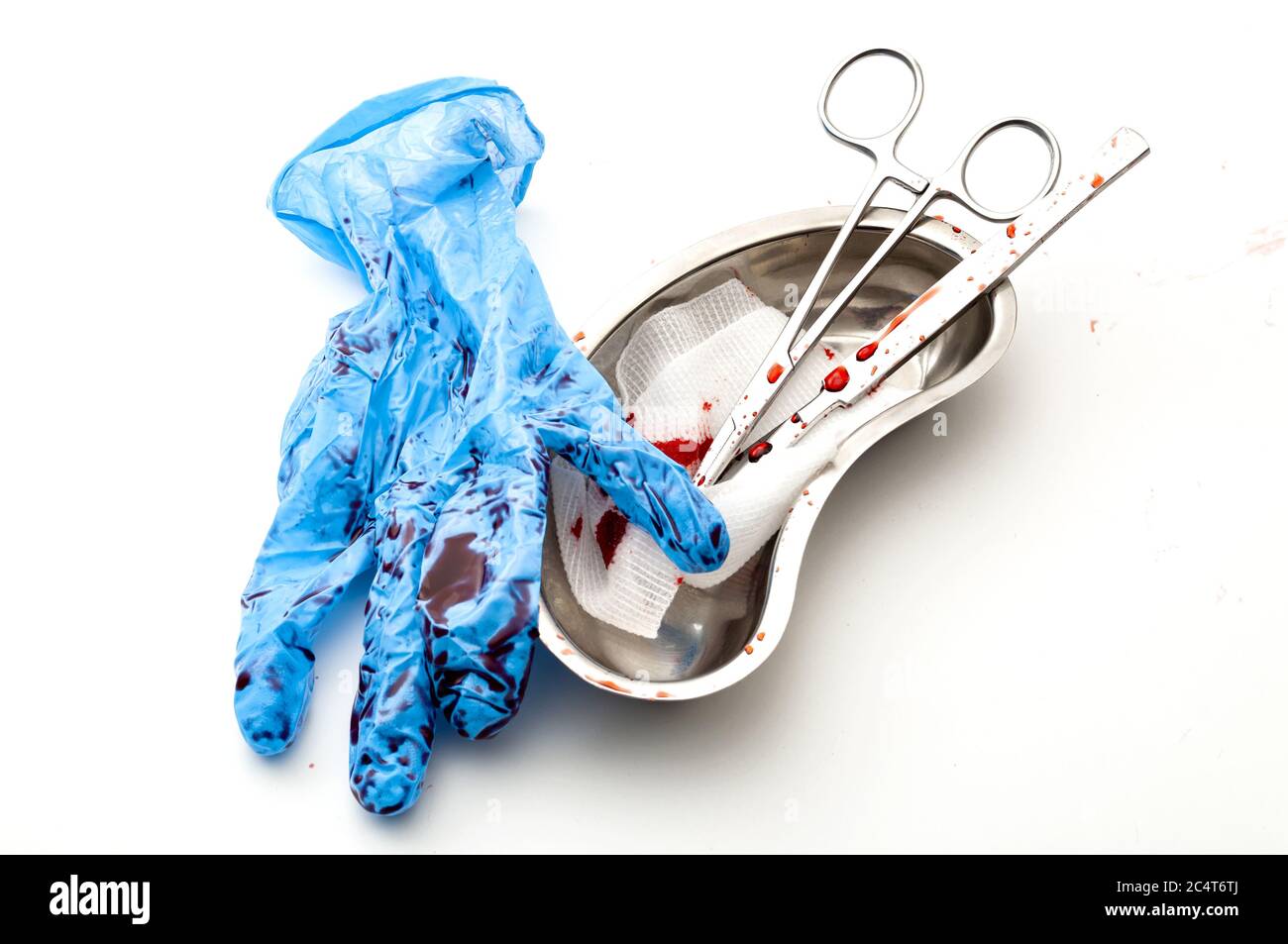
Scène post-opératoire : instruments souillés de sang, compresses, gants – tous nécessitent un nettoyage immédiat et approfondi avant toute tentative de stérilisation
2.2 Éclosions d’Infections Nosocomiales Documentées
Voici des cas réels et documentés d’épidémies causées par des instruments mal nettoyés ou non nettoyés avant stérilisation :
🇺🇸CAS USA – Hôpital de Virginie (2018)
Situation : Un hôpital universitaire prestigieux a découvert que son service de stérilisation centrale ne nettoyait pas correctement les instruments avant autoclavage pendant plus de 8 mois.
Contamination :
- Plus de 1800 patients exposés à des instruments potentiellement contaminés
- Instruments présentaient des résidus de sang séché visibles après « stérilisation »
- Tests microbiologiques révélèrent présence de Staphylococcus aureus résistant
Conséquences :
- 67 infections documentées : 43 ISO, 18 septicémies, 6 pneumonies
- 8 décès directement attribuables aux infections
- Fermeture temporaire de 4 blocs opératoires pendant 3 mois
- Coût total : 127 millions USD (indemnisations + perte revenus + remédiation)
- Directeur stérilisation licencié, sanctions FDA contre l’hôpital
- Tous les 1800 patients contactés pour dépistage VIH, VHB, VHC
Cause racine : Surcharge de travail, personnel insuffisant, pression pour « accélérer » les processus, formation inadéquate, aucun contrôle qualité sur le nettoyage pré-stérilisation.
🇪🇺CAS PAYS-BAS – Hôpitaux Maasstad (2014-2015)
Situation : Découverte fortuite lors d’un audit de routine : instruments endoscopiques (duodénoscopes) non correctement nettoyés avant désinfection haut niveau.
Contamination :
- 50 patients infectés par une souche de Klebsiella pneumoniae productrice de carbapénémase (KPC) – « superbactérie »
- Bactérie nichée dans biofilm du canal opérateur de l’endoscope
- Nettoyage manuel inadéquat + absence de brossage interne
Conséquences :
- 16 décès sur 50 patients infectés (taux mortalité 32%)
- Arrêt immédiat de toutes les procédures ERCP (cholangiopancréatographie rétrograde endoscopique)
- Rappel de 1275 patients pour tests de dépistage
- Révision complète du protocole national de retraitement des endoscopes
- Sanctions pénales envisagées contre la direction de l’hôpital
🇯🇵CAS JAPON – Clinique Dentaire Tokyo (2017)
Situation : Une clinique dentaire haut de gamme utilisait un autoclave Classe B mais ne nettoyait que superficiellement les turbines et instruments rotatifs.
Contamination :
- Sang et débris dentaires accumulés dans les canaux internes des turbines
- Autoclavage « fixait » les protéines sanguines, rendant nettoyage ultérieur impossible
- Transmission croisée de Mycobacterium chelonae
Conséquences :
- 52 patients développèrent des abcès mandibulaires atypiques
- Diagnostic difficile (mycobactérie atypique rarement suspectée)
- Traitements antibiotiques prolongés (6-12 mois par patient)
- Fermeture définitive de la clinique par le ministère de la Santé
- Dentiste propriétaire poursuivi pénalement pour « négligence criminelle »
- Perte de licence professionnelle à vie
- Coût : 8,5 millions USD en indemnisations
Révélation choquante : Inspection post-fermeture révéla que 80% des instruments avaient des résidus organiques incrustés « cuits » par des années d’autoclavage sans nettoyage correct.

Capture d’un reportage NBC News exposant des instruments chirurgicaux sales après « stérilisation » – révélant l’ampleur du problème dans certains établissements
🇨🇳CAS CHINE – Hôpital Provincial Henan (2019)
Situation : Un grand hôpital provincial avec 2000 lits utilisait un système centralisé de stérilisation mais le pré-nettoyage était effectué de manière bâclée.
Contamination :
- Instruments chirurgicaux simplement « rincés » à l’eau froide avant placement en autoclave
- Aucune utilisation de détergents enzymatiques
- Pas d’ultrasons, pas de laveur-désinfecteur
- Biofilms formés dans les articulations des instruments
Conséquences :
- Éclosion d’infections à Acinetobacter baumannii multirésistant
- 127 patients infectés en 4 mois (chirurgies orthopédiques et cardiaques)
- 31 décès (septicémie et choc septique)
- Enquête révéla que le service stérilisation était sous-financé et sous-staffé
- Directeur de l’hôpital et chef du service stérilisation arrêtés
- Condamnations pénales : 5 ans de prison ferme pour négligence grave
- Réforme nationale des standards de stérilisation hospitalière en Chine
Impact national : Ce scandale a mené à l’adoption en 2020 de la norme GB 30690 révisée, exigeant traçabilité complète et protocoles de nettoyage stricts.
🇮🇳CAS INDE – Cliniques Chirurgie Ambulatoire Mumbai (2021)
Situation : Réseau de 12 cliniques de chirurgie ambulatoire (yeux, hernies, varices) partageaient un seul centre de stérilisation centralisé.
Contamination :
- Volume d’instruments écrasant : 500-800 sets/jour à traiter
- Nettoyage « express » : trempage rapide, pas de brossage, séchage insuffisant
- Personnel non formé, turnover élevé
- Eau de robinet utilisée (haute teneur en minéraux, bactéries)
Conséquences :
- 856 infections documentées sur 18 mois (sous-estimation probable)
- Types : endophtalmies post-cataracte (63 cas de cécité), infections sites herniaires
- Pathogènes : Pseudomonas, E. coli, champignons (Fusarium)
- 23 décès (septicémies)
- Fermeture des 12 cliniques par autorités sanitaires Maharashtra
- Poursuites pénales et civiles massives
- Coût estimé : 45 millions USD (indemnisations + perte activité)
Facteurs aggravants : Infrastructure inadéquate (coupures eau/électricité fréquentes), aucun système qualité, recherche du profit maximal au détriment sécurité, absence d’inspection réglementaire efficace.
III. Le Processus de Nettoyage Correct : Étapes Détaillées et Standards Internationaux
Pour comprendre pleinement les conséquences du non-nettoyage, il est essentiel de connaître le protocole correct qui devrait être suivi dans tout établissement de soins.

Chargement correct d’instruments dans un bac à ultrasons : instruments complètement immergés, ouverts, sans contact entre eux
3.1 Les 8 Étapes du Nettoyage Pré-Stérilisation
Objectif : Empêcher le séchage des matières organiques sur les instruments.Protocole :
- Immédiatement après utilisation, essuyer grossièrement avec compresse humide
- Placer dans récipient avec solution enzymatique ou eau déminéralisée
- Ouvrir tous les instruments articulés, démonter composants si possible
- Rincer canaux/lumières d’instruments creux avec seringue d’eau
- DÉLAI CRITIQUE : Maximum 30 minutes avant nettoyage complet (idéalement immédiat)
⚠️ Conséquence du non-respect : Sang et protéines sèchent et « collent » aux surfaces – formation de biofilm en 2-4 heures – nettoyage ultérieur 10x plus difficile.
Zone : Salle de lavage (zone sale), équipement protection personnel obligatoire (gants épais, tablier imperméable, masque, lunettes).Actions :
- Démonter tous composants amovibles des instruments complexes
- Séparer instruments tranchants (risque piqûre)
- Identifier instruments nécessitant procédure spéciale (optique, micromoteurs)
- Compter et vérifier contre liste set chirurgical
Équipement : Bac avec eau tiède (35-40°C) + détergent enzymatique.Détergents enzymatiques :
- Composition : Protéases (digèrent protéines), lipases (graisses), amylases (amidon), tensioactifs
- Concentration : Selon fabricant, généralement 0,5-2%
- Température optimale : 35-45°C (enzymes inactivées >60°C)
- pH : Neutre à légèrement alcalin (7-10)
Technique :
- Immerger complètement tous instruments (pas d’émersion partielle)
- Brosser vigoureusement sous la surface de l’eau (éviter aérosols contaminés)
- Brosses nylon souple pour surfaces délicates, brosses plus dures pour instruments robustes
- Attention spéciale : articulations, dents de pinces, cannelures
- Brosses spéciales pour canaux/lumières (brosses « goupillon »)
- Durée : Minimum 2 minutes de brossage actif par instrument
Objectif : Éliminer détergent et débris grossiers avant nettoyage ultrasononique.Méthode :
- Rincer abondamment à l’eau déminéralisée ou osmosée
- Température : eau tiède (30-35°C)
- Pistolet à eau basse pression pour rincer cavités et canaux
- Secouer instruments pour évacuer eau résiduelle
Principe : Cavitation ultrasonique – bulles microscopiques implosent, créant ondes de choc qui délogent débris dans zones inaccessibles au brossage.Paramètres :
- Fréquence : 35-45 kHz (standard médical)
- Température : 40-50°C
- Solution : Détergent enzymatique ou alcalin spécial ultrasons
- Durée : 10 minutes minimum (15 min pour instruments complexes)
- Chargement : Instruments complètement immergés, ouverts, sans contact entre eux
Efficacité : Élimine 99,5% des contaminants résiduels après brossage manuel. Indispensable pour :
- Instruments avec lumières (canules, trocarts)
- Articulations complexes (ciseaux microchirurgie)
- Surfaces texturées/cannelées
- Instruments dentaires rotatifs
Alternative/Complément aux ultrasons : Appareil automatisé combinant nettoyage, rinçage, désinfection thermique et séchage.Phases du cycle :
- Phase 1 – Pré-lavage : Eau froide, élimination débris grossiers
- Phase 2 – Lavage : Eau 45-65°C + détergent alcalin, jets haute pression
- Phase 3 – Rinçage : Eau déminéralisée, multiple cycles
- Phase 4 – Désinfection thermique : Eau 90-93°C pendant 10 min (détruit bactéries végétatives)
- Phase 5 – Séchage : Air chaud filtré
Avantages : Standardisation, traçabilité, moins de manipulation humaine, désinfection intégrée.
Norme : EN ISO 15883 (Europe), AAMI ST79 (USA)
Rinçage :
- Eau déminéralisée stérile ou ultra-pure (conductivité <5 µS/cm)
- Éliminer toute trace de détergent (interfère avec stérilisation)
- Rincer canaux/lumières avec seringue
Séchage :
- Air comprimé médical filtré (séchage cavités et canaux)
- Chiffons non pelucheux stériles pour surfaces externes
- Séchage complet obligatoire : Humidité résiduelle = prolifération microbienne + formation rouille
Inspection visuelle :
- Loupe éclairante (grossissement 2-3x) obligatoire
- Vérifier absence totale de souillures : sang, tissus, taches, dépôts
- Examiner articulations, dentures, cannelures microscopiques
- Vérifier fonctionnalité (instruments s’ouvrent/ferment correctement)
- Détecter corrosion, dommages, usure
Tests chimiques :
- Test protéines résiduelles : Bandelettes détectant >5 µg protéines/cm²
- Test ATP : Mesure adénosine triphosphate (indicateur matière organique)
- Limite acceptable : <200 RLU (Relative Light Units)
⚠️ Instrument échouant inspection = Re-nettoyage complet ou retrait du service
✅ RÉSULTAT D’UN NETTOYAGE CORRECT :
Après ces 8 étapes, les instruments doivent être :
• Visuellement propres : Aucune souillure visible même à la loupe
• Microbiologiquement propres : Bioburden <250 UFC
• Chimiquement propres : Résidus protéiques <5 µg/cm²
• Fonctionnels : Pas de dommages, articulations fluides
• Secs : Aucune humidité résiduelle
• Prêts pour l’emballage et la stérilisation

Solution de nettoyage enzymatique multi-enzymatique pour bacs à ultrasons – formulation spécifique pour dissolution des protéines, lipides et glucides
IV. Conséquences Techniques sur les Instruments et l’Autoclave
4.1 Dommages Irréversibles aux Instruments
Au-delà des risques infectieux, le passage d’instruments non nettoyés à l’autoclave cause des dommages matériels permanents :
Lorsque du sang, des protéines tissulaires, ou des fluides corporels sont soumis à 134°C pendant plusieurs minutes dans un autoclave :
- Coagulation protéique irréversible : Les protéines se dénaturent et forment une couche dure, noire/brune, fusionnée avec le métal
- Carbonisation : Matières organiques se transforment en résidus carbonés incrustés
- Impossible à enlever : Même un nettoyage agressif ultérieur ne peut éliminer ces dépôts « cuits »
- Accumulation progressive : Chaque cycle aggrave le dépôt, créant des couches stratifiées
Impact fonctionnel :
- Articulations bloquées ou grippées (dépôts dans les charnières)
- Bords tranchants émoussés (scalpels, ciseaux recouverts de résidus)
- Surfaces préhensiles lisses (pinces ne serrent plus correctement)
- Canaux obstrués (instruments creux inutilisables)
Coût : Instruments de précision valant 500-5000€ pièce deviennent inutilisables et irréparables. Remplacement obligatoire.
Sels minéraux, chlorures et composés ioniques présents dans le sang et fluides corporels :
- Piqûres de corrosion : Chlorures attaquent acier inoxydable (même chirurgical)
- Corrosion galvanique : Dissimilarité métallique + électrolytes = corrosion rapide
- Oxydation sous dépôts : Résidus organiques créent zones anaérobies favorisant corrosion
- Taches permanentes : Décoloration brunâtre/rougeâtre impossible à éliminer
Zones à risque : Articulations, soudures, zones de contact métal-métal, zones de contrainte mécanique.
Instruments modernes ont des traitements de surface spécialisés :
- Anodisation : Couche protectrice aluminique (instruments aluminium)
- Passivation : Couche d’oxyde de chrome (acier inoxydable)
- Revêtements anti-adhérents : Type Téflon (certains instruments)
- Placage or/titane : Instruments microchirurgie ophtalmique
Résidus organiques « cuits » endommagent ces traitements, exposant le métal de base à corrosion et usure.
4.2 Dommages à l’Autoclave Lui-même
Résidus organiques volatilisés se condensent dans le système de génération vapeur :
- Encrassement résistances chauffantes : Dépôts carbonés réduisent efficacité thermique
- Colmatage électrovannes : Particules bloquent passages étroits
- Contamination eau générateur : Protéines dissoutes favorisent prolifération bactérienne
- Biofilm dans circuits vapeur : Bactéries thermotolerantes (Bacillus, Geobacillus) colonisent tuyauteries
Conséquence : Dégradation performances autoclave, cycles échoués, contamination croisée entre charges, maintenance accrue (coût), durée de vie réduite.
- Dépôts sur parois chambre : Résidus carbonisés se fixent sur acier inoxydable
- Dégradation joint porte : Silicone/EPDM attaqués par composés organiques agressifs
- Fuites vapeur : Joint compromis = perte étanchéité = échec cycles
V. Aspects Réglementaires et Responsabilités Légales
5.1 Cadre Réglementaire International
| Pays/Région | Réglementations Principales | Exigences Nettoyage | Sanctions |
|---|---|---|---|
| 🇪🇺 UNION EUROPÉENNE | • Règlement MDR 2017/745 • EN ISO 17664 • EN ISO 15883 |
• Protocole validé obligatoire • Traçabilité complète • Formation certifiée personnel |
• Retrait d’autorisation • Amendes jusqu’à 10M€ • Poursuites pénales |
| 🇺🇸 ÉTATS-UNIS | • FDA 21 CFR 800-1299 • AAMI ST79/ST91 • CDC Guidelines |
• Validation IQ/OQ/PQ • Audits réguliers • Registres 3+ ans |
• Warning letters FDA • Consent decrees • Amendes illimitées • Prison (négligence) |
| 🇯🇵 JAPON | • Medical Device Act • JIS T 7322 • MHLW Standards |
• Conformité stricte JIS • Documentation exhaustive • Inspections fréquentes |
• Suspension licence • Amendes sévères • Responsabilité pénale |
| 🇨🇳 CHINE | • NMPA Regulations • GB 30690/YY standards • Hospital Infection Control Law |
• Standards nationaux stricts • Inspections surprise • Système notation qualité |
• Fermeture établissement • Poursuites criminelles • Prison (cas graves) |
| 🇮🇳 INDE | • Medical Devices Rules 2017 • BIS Standards • State Health Acts |
• Conformité BIS/ISO • Enregistrement obligatoire • Audits variables |
• Amendes variables • Suspension activité • Poursuites civiles/pénales |
5.2 Responsabilités et Poursuites
⚖️ RESPONSABILITÉ LÉGALE MULTI-NIVEAUX
En cas d’infection causée par instruments mal nettoyés, la responsabilité peut être engagée à plusieurs niveaux :
1. RESPONSABILITÉ CIVILE (Indemnisation victimes) :
• Établissement de santé : Responsabilité contractuelle envers patients
• Dommages-intérêts : Préjudice physique, moral, perte revenus, souffrances
• Montants typiques : 50 000 à 5 000 000€ selon gravité
• Couverture assurance souvent refusée si négligence prouvée
2. RESPONSABILITÉ PÉNALE (Sanctions criminelles) :
• Chef d’accusation : Mise en danger de la vie d’autrui, homicide involontaire
• Cibles : Directeur établissement, responsable stérilisation, chirurgien
• Peines : Amendes lourdes + prison (jusqu’à 5 ans selon pays)
• Interdiction exercer profession médicale
3. RESPONSABILITÉ ADMINISTRATIVE :
• Autorités sanitaires : Suspension/retrait autorisations d’exploitation
• Fermeture temporaire ou définitive blocs opératoires
• Mise sous tutelle de l’établissement
• Sanctions financières administratives
4. RESPONSABILITÉ PROFESSIONNELLE :
• Ordres professionnels : Sanctions disciplinaires
• Radiation de l’ordre (médecins, infirmières)
• Perte accréditations et certifications
• Impossibilité exercer à vie dans certains cas

Biofilm mature sur surface médicale : structure complexe multicouche protégeant les bactéries – nettoyage manuel vigoureux seul capable de le détruire avant stérilisation
VI. Solutions et Prévention : Comment Garantir un Nettoyage Efficace
6.1 Infrastructure et Équipement
🏗️ INVESTISSEMENTS NÉCESSAIRES :
Zone de Lavage Dédiée :
• Salle séparée, ventilation négative (air extrait, pas diffusé)
• Lavabos profonds multiples (3 bacs minimum)
• Robinetterie mains-libres (genou/coude/cellule)
• Sols/murs imperméables, facilement lavables
• Éclairage intense (>500 lux) pour inspection
• Coût : 50 000-150 000€ selon taille
Équipements Majeurs :
• Bac à ultrasons médical : 5 000-25 000€ (capacité 3-30L)
• Laveur-désinfecteur : 40 000-150 000€ (selon capacité)
• Système purification eau : 8 000-30 000€ (osmose inverse/déminéralisation)
• Séchoir air comprimé médical : 3 000-10 000€
• Loupe éclairante inspection : 500-2 000€
• Lecteur ATP : 5 000-15 000€
Consommables Annuels :
• Détergents enzymatiques : 2 000-10 000€
• Brosses spécialisées : 500-2 000€
• Tests protéines/ATP : 1 000-5 000€
• EPI personnel (gants, masques, tabliers) : 3 000-8 000€
6.2 Ressources Humaines et Formation
👥 PERSONNEL QUALIFIÉ :
Profil Technicien Stérilisation :
• Formation initiale : Diplôme/certificat stérilisation (6-12 mois)
• Formation continue : Minimum 20h/an
• Compétences : Microbiologie, nettoyage, stérilisation, traçabilité
• Ratio recommandé : 1 technicien pour 300-500 instruments/jour
• Salaire moyen : 25 000-45 000€/an selon pays et expérience
Programme de Formation :
• Principes microbiologie et infection
• Chimie du nettoyage (détergents, pH, température)
• Techniques manuelles (brossage, rinçage)
• Utilisation équipements (ultrasons, laveur-désinfecteur)
• Inspection qualité (visuelle, tests chimiques)
• Traçabilité et documentation
• Sécurité personnelle (EPI, exposition sang)
• Pratique supervisée : 100+ heures
Supervision :
• Responsable stérilisation : Formation niveau master
• Audits internes réguliers
• Évaluation compétences annuelle
• Culture de l’excellence et zéro tolérance
6.3 Contrôle Qualité et Traçabilité
📋 SYSTÈME QUALITÉ ROBUSTE :
Tests Quotidiens :
• Inspection visuelle 100% instruments (loupe)
• Tests protéines : échantillon aléatoire 10% instruments
• Tests ATP : 5-10 instruments/jour
• Documentation résultats
Tests Hebdomadaires :
• Validation nettoyage ultrasons (plaque test protéines)
• Vérification laveur-désinfecteur (indicateurs chimiques)
• Audit échantillon sets complets
Tests Mensuels :
• Analyse microbiologique eau purification
• Test performances ultrasons (feuille aluminium)
• Calibration équipements mesure
Traçabilité Complète :
• Chaque instrument identifié (code-barres/RFID)
• Enregistrement : patient → set chirurgical → cycle nettoyage → opérateur → cycle stérilisation
• Archivage électronique minimum 5-10 ans
• Capacité rappel immédiat en cas problème
VII. Conclusion : La Stérilisation N’Existe Pas Sans Nettoyage
À travers ce document exhaustif, une vérité incontournable émerge avec une clarté absolue : stériliser des instruments médicaux sans les nettoyer d’abord n’est pas simplement une mauvaise pratique – c’est un acte dangereux, irresponsable et potentiellement criminel.
Les conséquences sont catastrophiques à tous les niveaux :
- Niveau microbiologique : Échec de la stérilisation dans 76% des cas, survie de pathogènes mortels (bactéries, virus, prions)
- Niveau clinique : Infections nosocomiales, septicémies, décès de patients
- Niveau technique : Destruction irréversible d’instruments coûteux, dommages à l’autoclave
- Niveau financier : Coûts astronomiques (indemnisations, équipement, perte réputation)
- Niveau légal : Poursuites civiles et pénales, fermeture d’établissements, prison
- Niveau éthique : Violation du serment d’Hippocrate « Primum non nocere » (D’abord, ne pas nuire)
Les exemples dramatiques documentés aux États-Unis (1800 patients exposés, 8 décès), aux Pays-Bas (16 morts par superbactérie), au Japon (52 infections mycobactériennes), en Chine (127 infections, 31 décès) et en Inde (856 infections, 23 décès dont 63 cécités) prouvent que ce n’est pas un risque théorique mais une réalité tragique qui se produit régulièrement lorsque les protocoles de nettoyage sont négligés.
🎯 MESSAGE FINAL SANS ÉQUIVOQUE
Le nettoyage préalable à la stérilisation n’est PAS optionnel.
Le nettoyage préalable à la stérilisation n’est PAS négociable.
Le nettoyage préalable à la stérilisation n’est PAS un « plus » ou une « bonne pratique ».
Le nettoyage préalable est une NÉCESSITÉ ABSOLUE et une OBLIGATION LÉGALE.
Tout professionnel de santé, tout gestionnaire d’établissement, tout responsable de stérilisation qui autorise, tolère ou pratique la stérilisation d’instruments non nettoyés :
• Met en danger la vie des patients
• Viole les normes internationales
• Commet une faute professionnelle grave
• S’expose à des sanctions pénales
• Trahit la confiance du public
Il n’y a AUCUNE excuse, AUCUNE justification, AUCUNE circonstance atténuante.
Dans un monde où les technologies médicales progressent à une vitesse vertigineuse, où la chirurgie robotique et l’intelligence artificielle révolutionnent les soins, il est paradoxal et inacceptable que des principes aussi fondamentaux que le nettoyage des instruments soient encore violés.
La solution existe. Elle est connue. Elle est validée scientifiquement. Elle est codifiée réglementairement. Elle doit simplement être appliquée sans compromis, sans exception, sans échappatoire.
Pour les patients qui confient leur vie aux professionnels de santé. Pour les familles qui font confiance au système médical. Pour l’intégrité de la profession médicale. Pour le respect de la dignité humaine.
NETTOYER D’ABORD. STÉRILISER ENSUITE. TOUJOURS. SANS EXCEPTION.
Document rédigé conformément aux normes internationales :
EN ISO 17664 • EN ISO 15883 • AAMI ST79 • CDC Guidelines • JIS T 7322 • WHO Standards
Sources : CDC, OMS, ECDC, FDA, MHLW, études cliniques publiées dans revues à comité de lecture
Ce document peut être utilisé à des fins éducatives et de sensibilisation
Mise à jour : Octobre 2025