LE TEST DE BOWIE-DICK : GARDIEN UNIVERSEL DE LA STÉRILISATION HOSPITALIÈRE
Introduction
En 1963, à l’hôpital Western General d’Édimbourg, deux pionniers de la stérilisation médicale, J.H. Bowie et J. Dick, développaient un test révolutionnaire qui allait transformer les pratiques hospitalières mondiales. Le test de Bowie-Dick, conçu initialement pour détecter les fuites d’air dans les autoclaves à pré-vide, est rapidement devenu le standard de référence international pour garantir l’efficacité de la stérilisation à la vapeur.
Cette innovation britannique répond à un enjeu critique de santé publique : la prévention des infections nosocomiales. Chaque année, ces infections contractées en milieu hospitalier affectent des millions de patients dans le monde, entraînant des complications graves et des coûts de santé considérables. Le test de Bowie-Dick constitue la première ligne de défense contre ces risques, en s’assurant que les instruments chirurgicaux sont véritablement stérilisés.

Aujourd’hui, ce test est adopté dans plus de 150 pays à travers le monde, des hôpitaux universitaires américains aux centres de santé ruraux en Inde, en passant par les cliniques high-tech du Japon. Sa simplicité d’utilisation, combinée à son efficacité prouvée, en fait un outil indispensable dans l’arsenal de la stérilisation moderne. L’Organisation Mondiale de la Santé (OMS) recommande son utilisation systématique, tandis que les autorités réglementaires nationales en font souvent une obligation légale.
Cette universalité du test de Bowie-Dick témoigne de son rôle fondamental dans l’écosystème de la sécurité des soins. De Boston à Mumbai, de Tokyo à Berlin, les techniciens de stérilisation effectuent quotidiennement ce test de trois minutes et demie qui garantit que des millions d’instruments médicaux sont véritablement stériles avant d’être utilisés sur les patients.
Principes Fondamentaux du Test Bowie-Dick
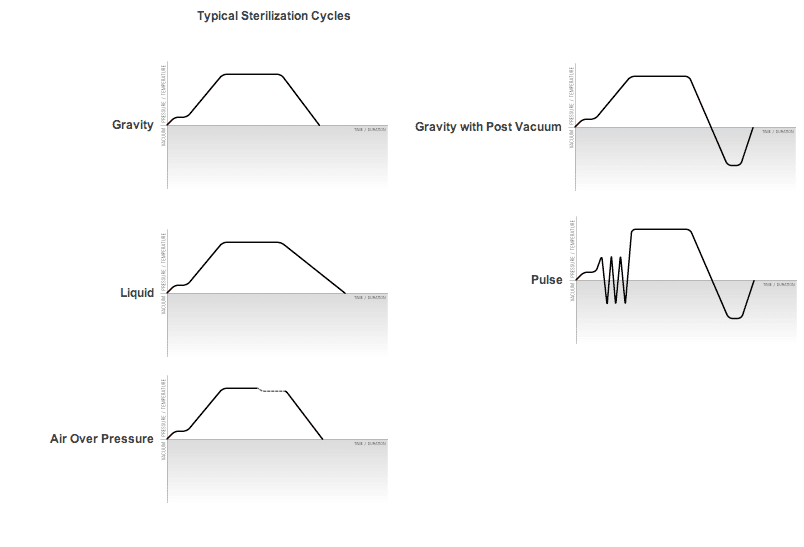
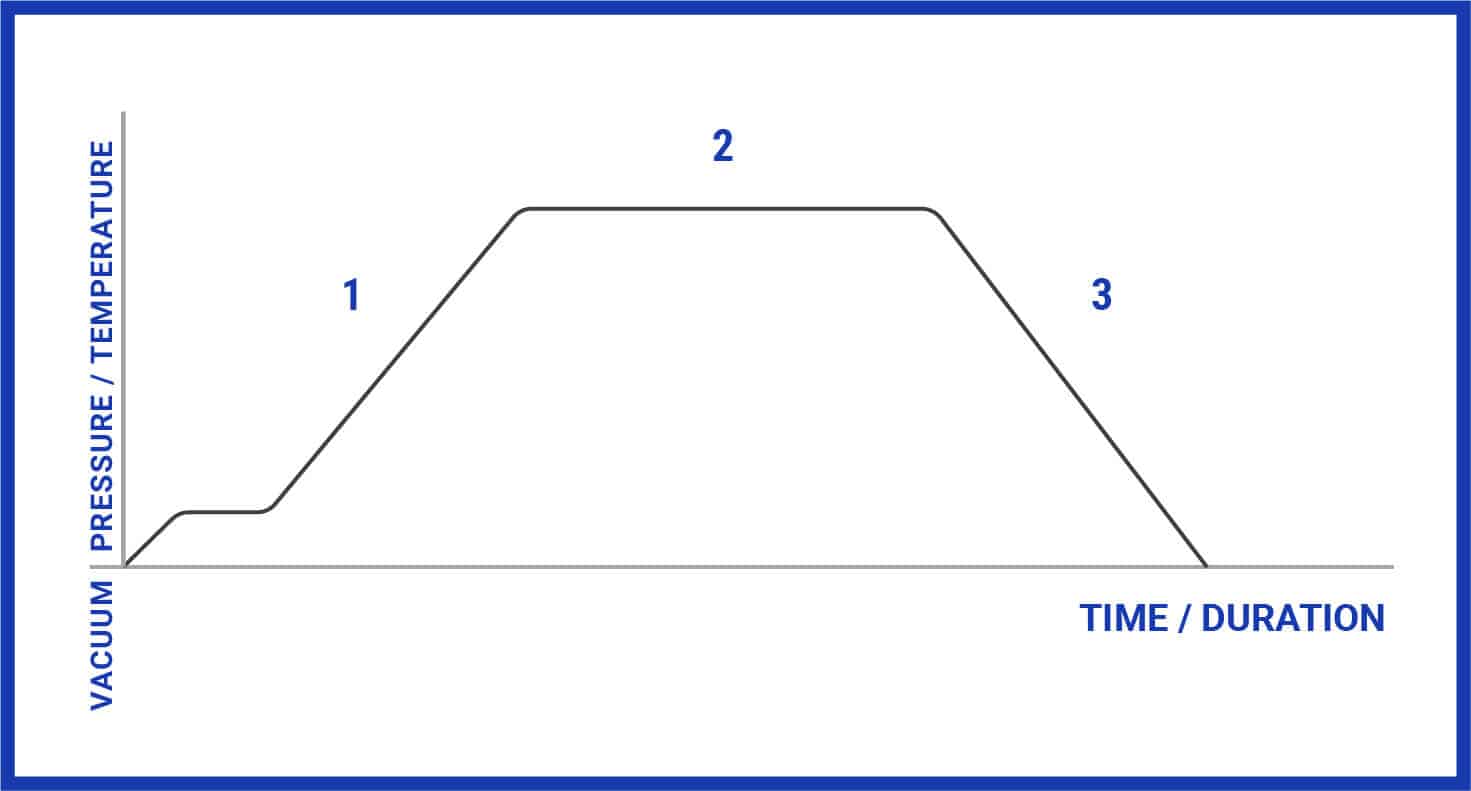
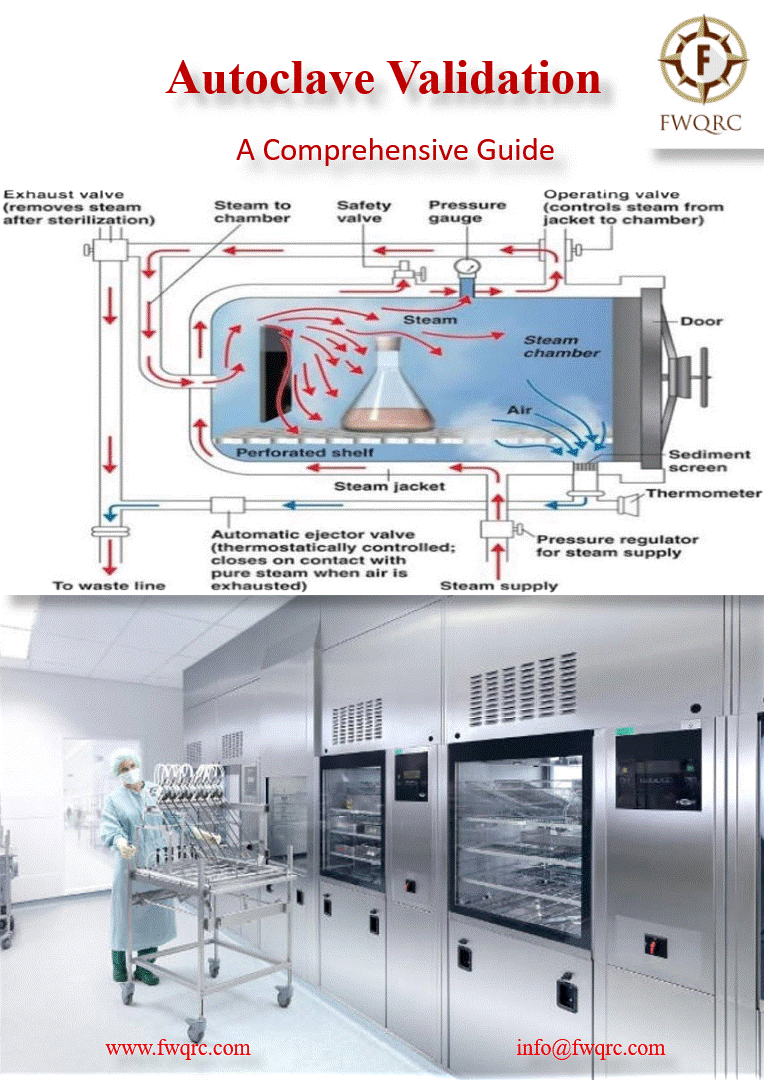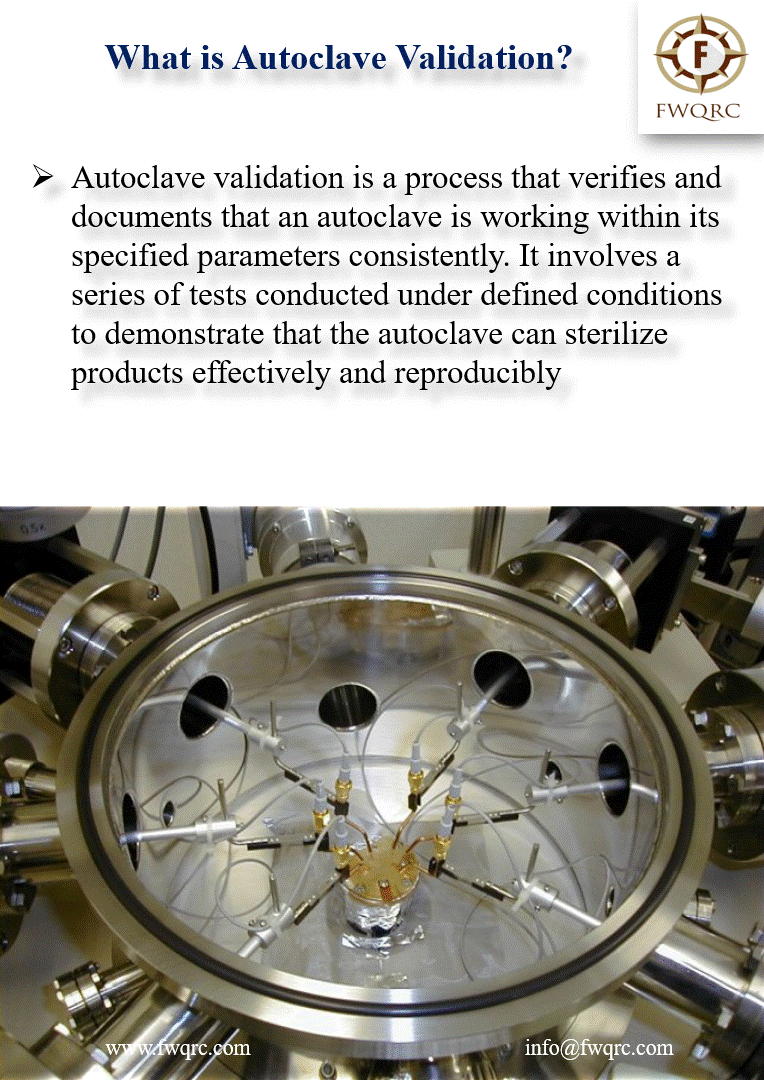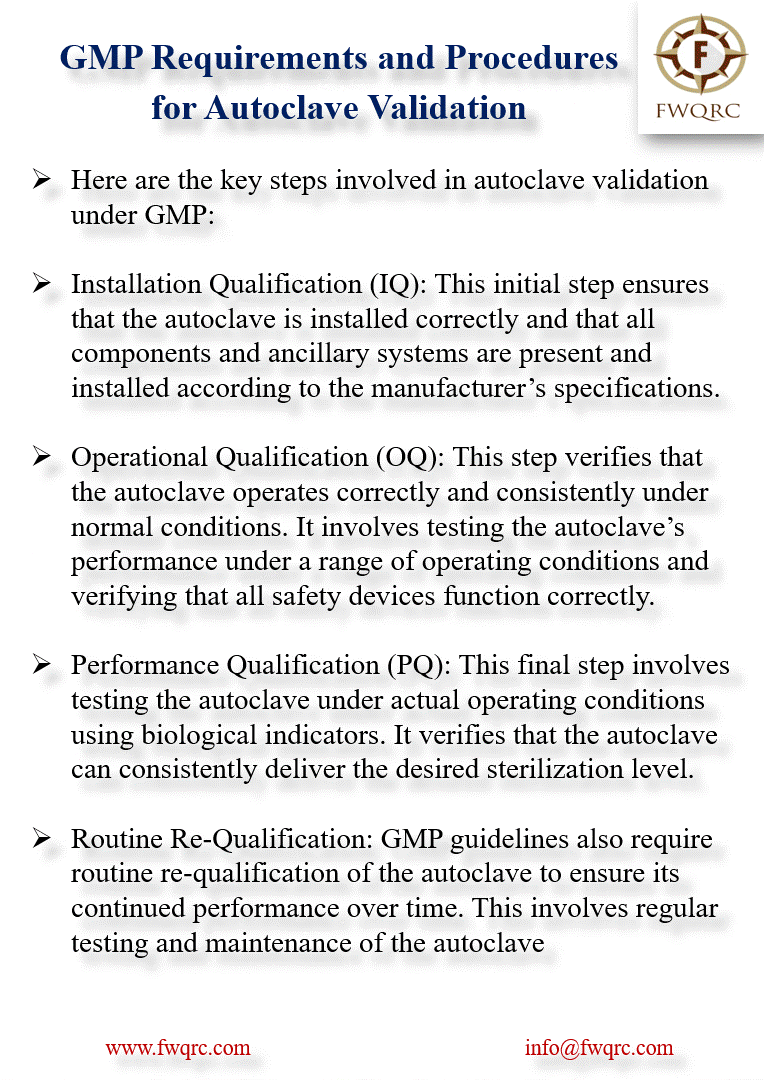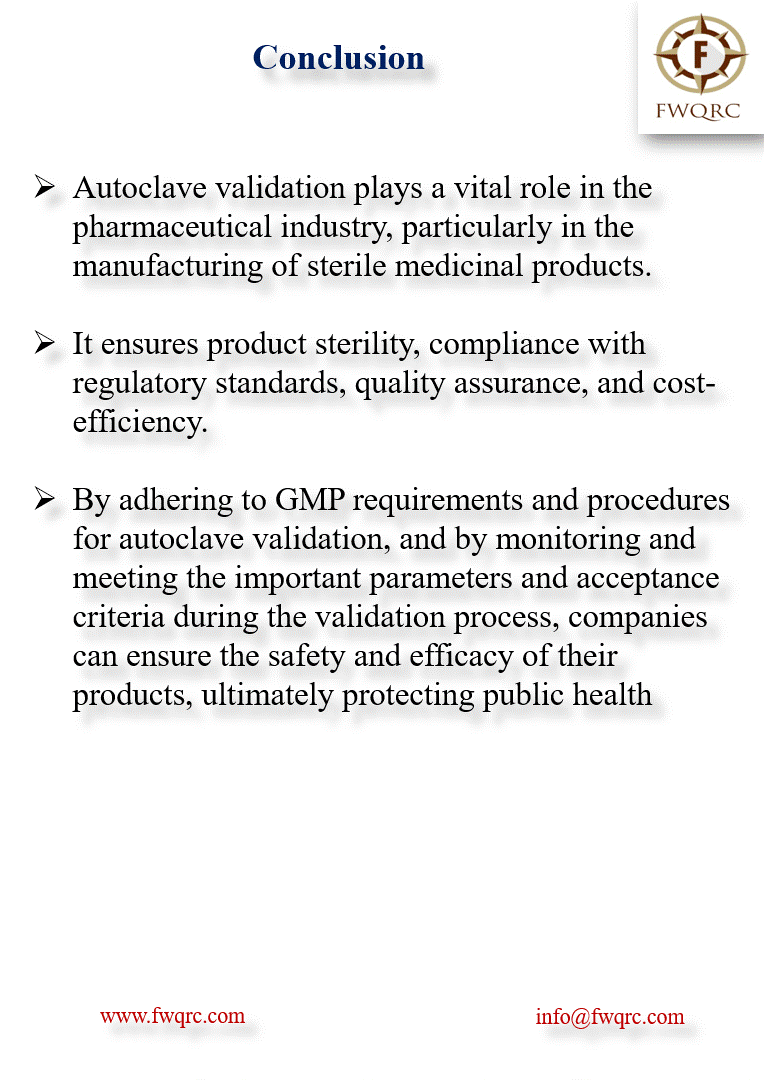
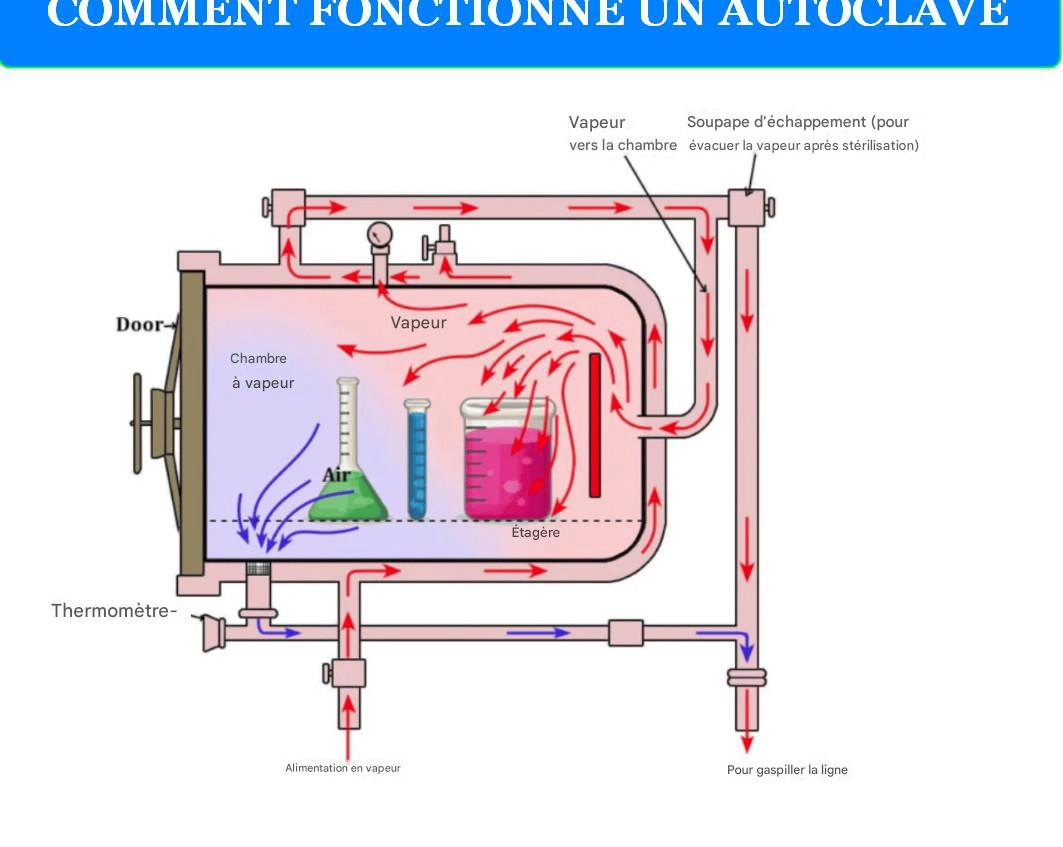
Le test de Bowie-Dick repose sur un principe physique fondamental : l’élimination complète de l’air présent dans la chambre de stérilisation par des cycles de vide successifs. Cette étape préliminaire est absolument critique, car l’air agit comme une barrière thermique qui empêche la vapeur saturée d’atteindre toutes les surfaces des instruments à stériliser.
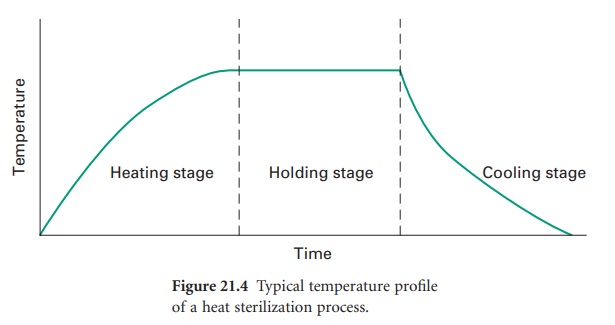
La vapeur saturée à 134°C (±3°C) constitue le seul agent stérilisant véritablement efficace dans un autoclave à pré-vide. À cette température et sous une pression de 2,05 à 2,35 bars, la vapeur possède l’énergie thermique nécessaire pour détruire tous les micro-organismes, y compris les spores bactériennes les plus résistantes. Cependant, cette efficacité n’est garantie que si la vapeur peut pénétrer uniformément dans tous les recoins de la charge à stériliser.
La présence d’air résiduel, même en quantité minime, peut réduire l’efficacité de la stérilisation de 50% ou plus. L’air, moins dense que la vapeur, tend à se concentrer dans les zones les plus froides de l’autoclave, généralement au niveau du drain et dans les espaces confinés des instruments creux. Ces « poches d’air » créent des zones froides où la température reste insuffisante pour garantir la stérilisation, compromettant ainsi la sécurité du processus.
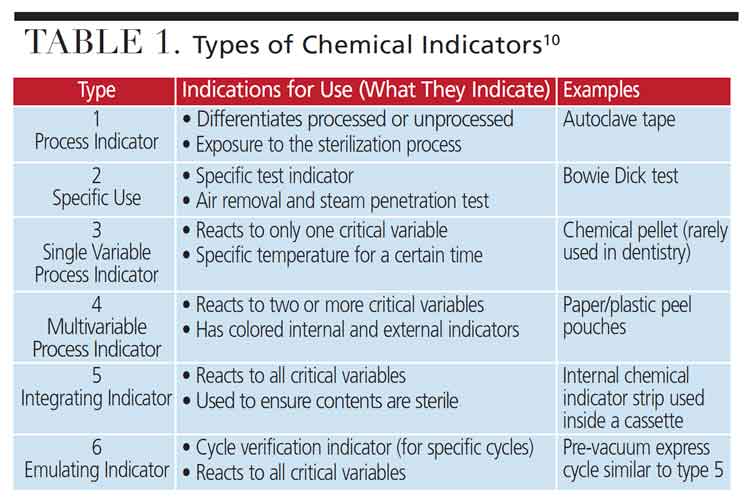
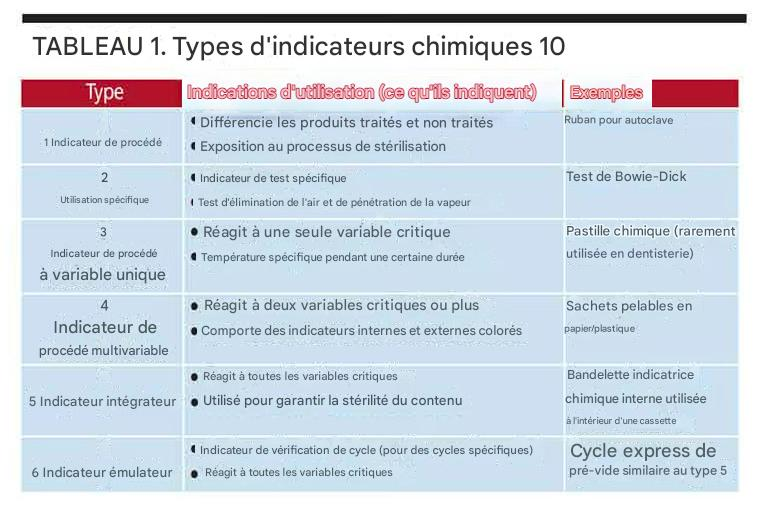
Le test de Bowie-Dick utilise des indicateurs chimiques sophistiqués pour détecter ces défaillances. Ces indicateurs sont constitués de composés chimiques thermosensibles qui subissent des virages colorimétriques caractéristiques lorsqu’ils sont exposés aux conditions optimales de stérilisation. Les changements de couleur les plus couramment observés incluent le passage du bleu au noir, du rose au brun, ou du jaune au violet selon les fabricants.
Le pack de test standard contient typiquement 100 feuilles de papier absorbant en coton, disposées en couches successives, avec l’indicateur chimique placé au centre géométrique du paquet. Cette configuration simule les conditions les plus défavorables à la pénétration de vapeur, reproduisant les défis rencontrés avec les charges poreuses complexes utilisées en milieu hospitalier.
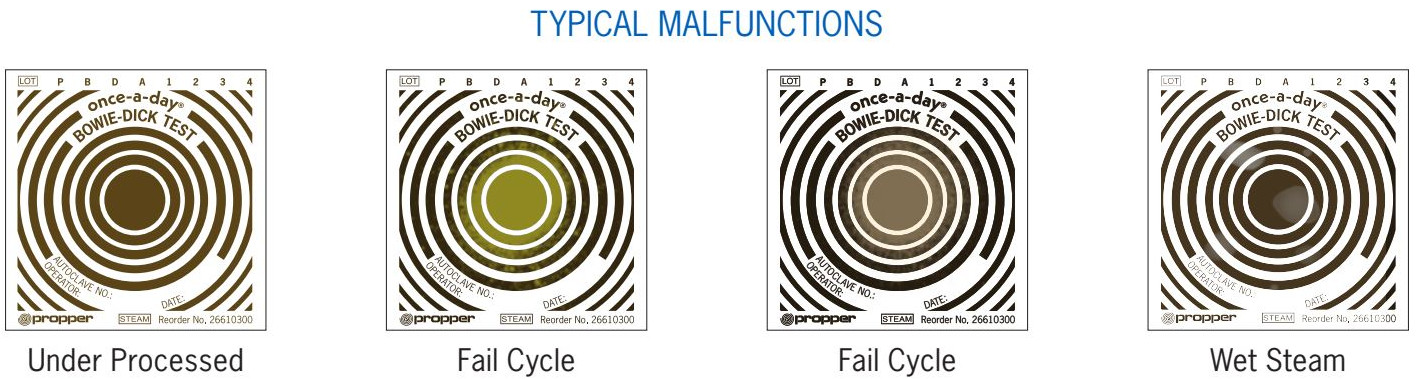
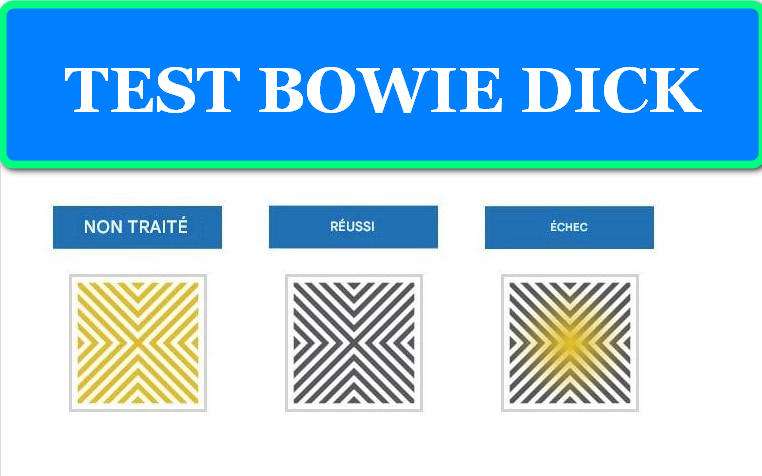
L’interprétation du test repose sur l’analyse visuelle de l’uniformité du changement de couleur. Un test réussi présente une coloration uniforme sur toute la surface de l’indicateur, témoignant d’une pénétration homogène de la vapeur. À l’inverse, la présence de zones non colorées, de dégradés ou de taches claires indique la persistance d’air résiduel et donc l’échec du test.
Cette méthode, bien que simple en apparence, nécessite une formation appropriée du personnel pour garantir une interprétation correcte des résultats. Les fabricants fournissent généralement des cartes de référence colorimétrique permettant une comparaison objective des résultats obtenus.
Normes Internationales et Régionales
Europe
L’Europe dispose du cadre normatif le plus harmonisé au monde pour les tests de Bowie-Dick, grâce à l’adoption généralisée des standards ISO et EN. La norme ISO 11140-3:2007 définit précisément les exigences relatives aux systèmes d’indicateurs de Classe 2 utilisés dans les tests de type Bowie-Dick. Cette norme spécifie les critères de performance, les méthodes de validation et les protocoles d’interprétation des résultats.
La norme ISO 17665-1, relative à la stérilisation par chaleur humide, complète ce dispositif en établissant les exigences générales pour le développement, la validation et le contrôle de routine des processus de stérilisation à la vapeur. Elle impose notamment la réalisation quotidienne de tests de Bowie-Dick pour tous les autoclaves à pré-vide utilisés en milieu hospitalier.
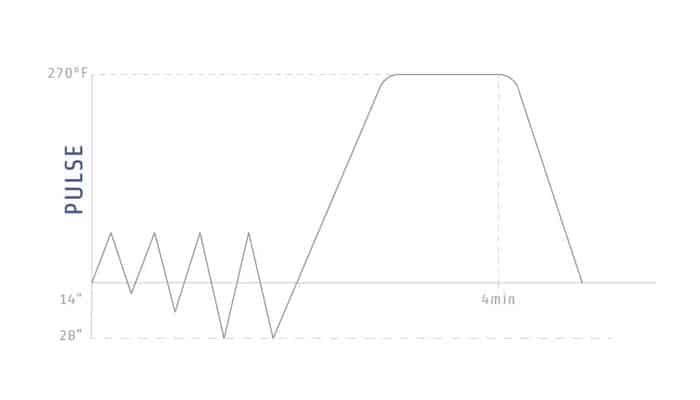
La norme européenne EN 285, spécifique aux stérilisateurs à vapeur de grande capacité, précise les paramètres opérationnels : température de 134°C (±3°C), durée minimum de 3,5 minutes, pression maintenue entre 2,05 et 2,35 bars. Ces spécifications techniques garantissent la reproductibilité et la fiabilité des tests à travers l’ensemble de l’Union européenne.
Spécificités nationales européennes :
- France : Conformité aux Bonnes Pratiques de Pharmacie Hospitalière (BPPH), traçabilité obligatoire pendant 5 ans, contrôles ANSM
- Allemagne : Standards DIN EN stricts, certification TÜV obligatoire, archivage 10 ans
- Royaume-Uni : NHS Guidelines post-Brexit, inspections CQC annuelles, système SCAN de traçabilité
- Espagne : Norme UNE-EN-ISO 17665, contrôles AEMPS, formation continue 20h/an minimum
États-Unis
Le système réglementaire américain repose sur un triptyque d’autorités : la FDA (Food and Drug Administration), le CDC (Centers for Disease Control and Prevention) et l’AAMI (Association for the Advancement of Medical Instrumentation). La FDA, via le règlement 21 CFR Part 820 (Quality System Regulation), encadre la fabrication et la commercialisation des dispositifs de test de Bowie-Dick en tant que dispositifs médicaux de Classe II.
Les Guidelines CDC de 2008, révisées en 2023, imposent la réalisation quotidienne de tests de Bowie-Dick pour tous les stérilisateurs à élimination dynamique d’air (pré-vide) utilisés dans les établissements de santé. Cette obligation s’étend également aux tests de qualification après installation, déplacement ou réparation majeure de l’équipement.

La norme AAMI ST79 « Comprehensive guide to steam sterilization » constitue la référence technique pour l’industrie américaine. Elle détaille les procédures de test, les critères d’acceptation et les protocoles de maintenance. Les hôpitaux de référence comme Johns Hopkins appliquent des protocoles renforcés : trois tests consécutifs réussis après chaque installation, validation IQ/OQ/PQ (Installation/Operational/Performance Qualification) annuelle, et budget dédié de 50 000 dollars par an pour les tests et la maintenance.
La Mayo Clinic a développé un système de traçabilité électronique complet, permettant un suivi en temps réel de tous les tests effectués sur ses 200+ autoclaves répartis sur ses différents campus. Cette approche digitale permet d’atteindre un taux d’échec inférieur à 1%, bien en dessous de la moyenne nationale de 2-3%.
Japon
Le Japon présente l’un des systèmes les plus rigoureux au monde, supervisé par le MHLW (Ministry of Health, Labour and Welfare). L’Ordonnance ministérielle n°169 établit les standards de qualité pour les dispositifs médicaux, incluant les systèmes de stérilisation. La conformité ISO 13485:2016 est obligatoire pour tous les services de stérilisation hospitaliers.
La norme JIS T 0841 spécifie les exigences techniques pour les autoclaves médicaux, avec des critères de performance particulièrement stricts. La PMDA (Pharmaceuticals and Medical Devices Agency) effectue des validations bisannuelles des processus de stérilisation, incluant l’audit des protocoles de test de Bowie-Dick.
L’hôpital universitaire d’Osaka, premier établissement japonais certifié ISO 13485:2016 pour son département de stérilisation centrale (CSSD), effectue des tests six jours par semaine avec une documentation bilingue japonais-anglais pour faciliter les audits internationaux. Cette excellence opérationnelle fait référence dans le secteur hospitalier nippon.
Chine
La Chine connaît une évolution rapide de sa réglementation, alignée sur les standards internationaux. Les normes GB (Guobiao/Standards nationaux) constituent le socle réglementaire national. La norme GB 18279-2023 pour la stérilisation des produits de santé à l’oxyde d’éthylène s’applique par extension aux processus vapeur, tandis que GB/T 15981-2021 régit l’utilisation des indicateurs biologiques.

La norme GB 4789.1-2016 établit les règles générales d’examen microbiologique, incluant les protocoles de stérilisation. La température standard adoptée est de 121°C pendant 30 minutes ou 134°C pendant 3,5 minutes, alignée sur les recommandations internationales. Le standard WS 310.2-2016 régit spécifiquement les services de désinfection hospitalière.
Les hôpitaux de niveau Tier 3 (plus haut niveau de la classification chinoise) doivent obligatoirement se conformer aux normes ISO, générant un marché en croissance de 12% CAGR (2024-2032). Les fabricants chinois Shinva et New Life développent des solutions locales compétitives, réduisant la dépendance aux importations européennes et américaines.
Inde
L’Inde présente un paysage contrasté entre hôpitaux urbains modernes et structures rurales encore déficitaires. Les standards NABH (National Accreditation Board for Hospitals & Healthcare Providers) 6ème édition, effectifs depuis janvier 2025, imposent des exigences strictes pour l’accréditation hospitalière, incluant la réalisation quotidienne de tests de Bowie-Dick.
La norme BIS IS 14345 spécifie les exigences techniques pour les appareils d’autoclave, tandis que les National IPC Guidelines (Infection Prevention and Control) publiées par le NCDC (National Centre for Disease Control) en 2024 détaillent les protocoles opérationnels. Les services CSSD doivent respecter une organisation en zones démarquées avec flux unidirectionnel et procédures opérationnelles standard (SOPs) documentées.
Les chaînes hospitalières privées comme Apollo Hospitals ou Fortis Healthcare ont adopté des standards internationaux, avec des systèmes de traçabilité cloud et une formation de 80 heures pour les techniciens CSSD. Le coût d’un test varie entre ₹150-300 (€1.60-3.20), rendant cette technologie accessible même aux établissements de taille moyenne.
Cependant, 40% des hôpitaux ruraux ne disposent toujours pas d’autoclaves de Classe B, limitant l’application des tests de Bowie-Dick. Les initiatives gouvernementales comme Ayushman Bharat visent à réduire cette fracture technologique par un financement public des équipements de stérilisation.
Protocole d’Exécution du Test
La réalisation d’un test de Bowie-Dick suit un protocole précis en sept étapes, dont le respect conditionne la fiabilité des résultats. Cette procédure standardisée, applicable dans tous les contextes hospitaliers, garantit la reproductibilité et la comparabilité internationale des tests.
Étapes du protocole standard :
- Vérification pré-test : Contrôle de la date de péremption, intégrité du paquet, conditions de stockage
- Préparation chambre : Chambre vide, propre, absence de résidus de cycles précédents
- Placement optimal : Centre du plateau inférieur, au-dessus du drain (point le plus froid)
- Sélection cycle : Programme « Bowie-Dick » ou paramètres manuels (134°C, 3,5 min)
- Surveillance cycle : Vérification des paramètres temps/température/pression
- Refroidissement contrôlé : Attente 2-3 minutes avant ouverture
- Interprétation immédiate : Analyse visuelle dans les 10 minutes
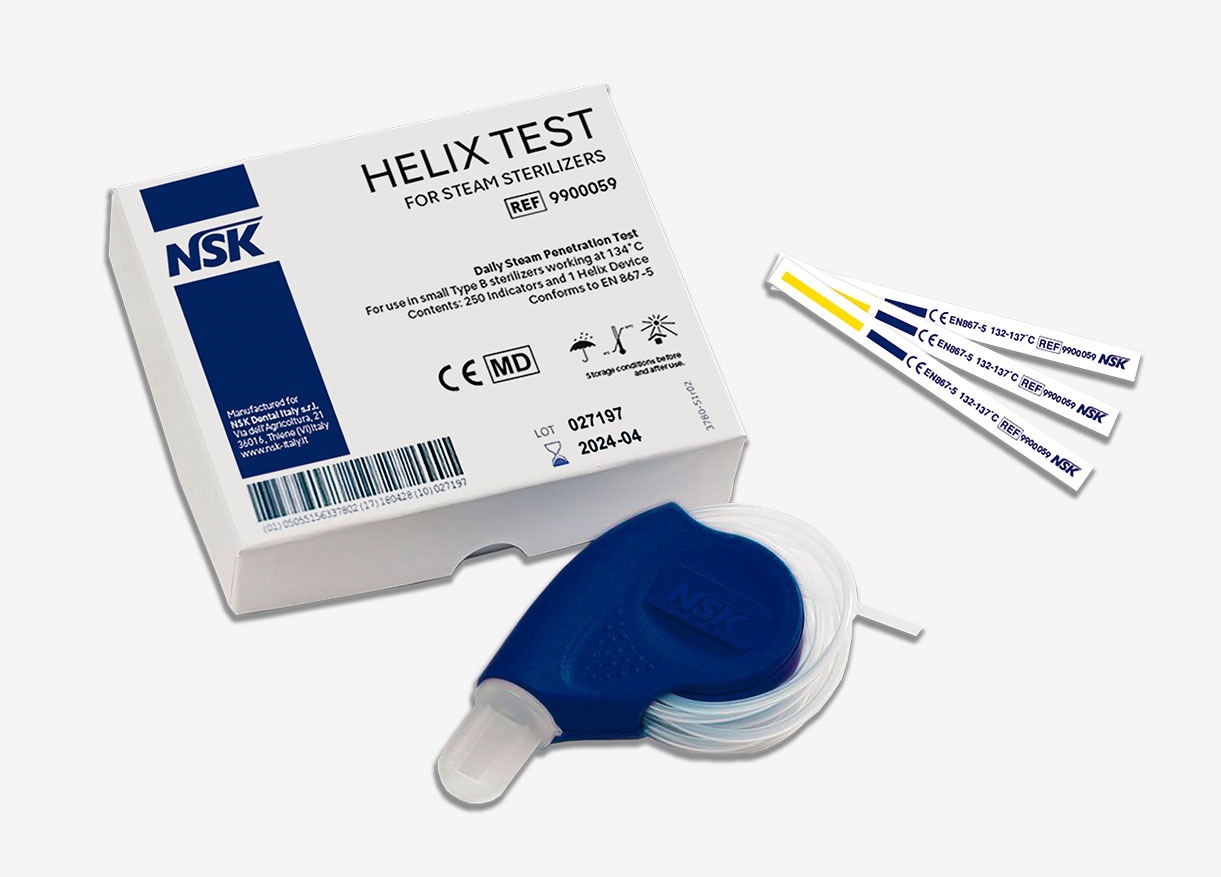
Le marché propose aujourd’hui quatre types principaux de tests, adaptés aux différents besoins hospitaliers. Le test standard, composé de 100 feuilles de coton avec indicateur central, reste la référence pour la validation quotidienne. Le test Helix, spécialement conçu pour valider la stérilisation des charges creuses, utilise un tube de 1,5 mètre de long et 2 millimètres de diamètre, simulant les conditions les plus exigeantes rencontrées avec l’instrumentation moderne.

Les tests autoadhésifs, d’usage unique, simplifient la documentation en intégrant des étiquettes pré-imprimées avec espaces pour noter les informations réglementaires. Cette innovation réduit les erreurs de traçabilité et accélère les procédures d’archivage. Les tests électroniques, dernière génération technologique, intègrent des capteurs miniaturisés qui enregistrent automatiquement les données de température et pression, générant des rapports numériques directement exploitables par les systèmes qualité hospitaliers.
L’interprétation des résultats repose sur l’analyse de l’uniformité du changement colorimétrique. Un TEST RÉUSSI présente une coloration uniforme sur toute la surface, sans zones claires résiduelles. Un TEST ÉCHOUÉ se caractérise par des taches claires, des zones non virées ou des dégradés de couleur, témoignant d’une pénétration incomplète de la vapeur.
| Fabricant | Couleur Initiale | Couleur Finale | Temps de Virage |
|---|---|---|---|
| 3M Company | Jaune | Noir | 30-60 secondes |
| Steris Corporation | Rose | Brun foncé | 45-90 secondes |
| Terragene SA | Violet | Gris foncé | 60-120 secondes |
| Getinge AB | Bleu | Vert foncé | 30-90 secondes |

Pratiques Hospitalières par Région
Europe
ALLEMAGNE – Charité Universitätsmedizin Berlin : Cet hôpital de référence européen, avec ses 3 000 lits et 100 blocs opératoires, effectue quotidiennement six tests de Bowie-Dick à 6h00 précises, avant le début de la production. Le système de documentation électronique intégré Sterilizer Management System (SMS) enregistre automatiquement tous les paramètres et génère des alertes en cas d’anomalie. L’archivage, maintenu pendant 10 ans conformément aux exigences TÜV, représente plus de 15 000 tests documentés annuellement. La formation du personnel, renouvelée chaque année, inclut 20 heures de théorie et 10 heures de pratique supervisée.
FRANCE – CHU de Lyon : Premier centre hospitalier français certifié ISO 15189, le CHU applique scrupuleusement les Bonnes Pratiques de Pharmacie Hospitalière. La validation triplicata après chaque maintenance majeure, exigence spécifique française, a permis de détecter 12% de défaillances post-intervention en 2023. Le logiciel de traçabilité STERIDOC, développé localement, interface directement avec le système d’information hospitalier, permettant un suivi en temps réel des 2 500 tests annuels. Les audits internes mensuels, effectués par le service qualité, maintiennent un taux de conformité de 99,8%.
ROYAUME-UNI – NHS Trusts : Le système de santé britannique, avec ses 223 Trusts hospitaliers, applique un standard uniforme : tests 7 jours sur 7 avec autoclave de secours systématique. Le système SCAN (Sterilization Control and Navigation), déployé depuis 2019, utilise la traçabilité code-barres pour réduire les erreurs humaines de 85%. Les inspections CQC (Care Quality Commission) vérifient annuellement la conformité des registres sur 2 ans, avec un taux de non-conformité ramené à 2,1% en 2023. Le coût moyen de £2.50 par test, optimisé par les achats groupés NHS, représente une économie de 30% par rapport aux tarifs individuels.
ESPAGNE – Hospital Universitario La Paz : Cet établissement madrilène de 1 368 lits démontre l’excellence espagnole avec sa conformité UNE-EN-ISO 17665. Les tests, effectués 5 jours par semaine minimum, atteignent un taux de réussite de 99,2% grâce à un programme de maintenance prédictive. La formation continue, 20 heures annuelles par technicien, intègre les dernières innovations technologiques et maintient une qualification du personnel reconnue au niveau européen.

États-Unis
Le protocole CDC 2023 impose quatre exigences fondamentales : test quotidien obligatoire pour tous les autoclaves pré-vide, trois tests consécutifs réussis après installation, test systématique après réparation majeure, et archivage dont la durée varie de 3 à 7 ans selon les États. Cette harmonisation fédérale a permis de standardiser les pratiques dans les 6 090 hôpitaux américains.
Johns Hopkins Hospital : Cette institution de référence mondiale, avec ses 12 autoclaves de stérilisation centrale, effectue quotidiennement 12 tests de Bowie-Dick. Le système automatisé Getinge T-DOC génère des rapports en temps réel, transmis directement au laboratoire de microbiologie pour validation. La validation IQ/OQ/PQ (Installation/Operational/Performance Qualification) annuelle, d’un coût de 15 000 dollars par autoclave, garantit la conformité FDA. Le budget global de 50 000 dollars annuels, incluant tests et maintenance, représente moins de 0,1% du budget d’exploitation, démontrant la rentabilité de cette approche préventive.
Mayo Clinic : Leader de l’innovation hospitalière, Mayo Clinic a développé un système de traçabilité électronique révolutionnaire, intégrant intelligence artificielle et analytics prédictifs. La formation de 40 heures pour les techniciens CSSD, la plus complète du secteur, inclut simulation 3D et réalité virtuelle. Le taux d’échec inférieur à 1%, comparé à la moyenne nationale de 2-3%, démontre l’efficacité de cette approche holistique. Le ROI (Return On Investment) de 320% sur 5 ans justifie l’investissement technologique initial.
Asie-Pacifique
JAPON – Osaka University Hospital : Premier établissement asiatique certifié ISO 13485:2016 pour son département CSSD, cet hôpital universitaire de 1 086 lits exemplifie l’excellence japonaise. Les tests, effectués 6 jours par semaine, intègrent une double validation : technique locale et administrative centralisée. La validation PMDA bisannuelle, d’une rigueur reconnue internationalement, maintient la certification depuis 2018. La documentation bilingue japonais-anglais facilite les audits internationaux et les échanges académiques, positionnant l’établissement comme référence régionale.
CHINE – Développement accéléré : La Chine connaît une transformation remarquable de son secteur hospitalier. Les hôpitaux Tier 3, au nombre de 2 548 en 2023, doivent obligatoirement se conformer aux normes ISO pour maintenir leur classification. Cette exigence génère un marché domestique en croissance de 12% CAGR, alimenté par l’urbanisation et l’élévation du niveau de vie. Les fabricants chinois Shinva Medical Equipment et New Life Medical Technology développent des solutions technologiques compétitives, réduisant les coûts de 40% par rapport aux importations occidentales.
INDE – Contrastes et progrès : L’Inde présente une dualité marquée entre excellence urbaine et défis ruraux. Les hôpitaux urbains accrédités NABH, comme Apollo Hospitals (71 établissements) et Fortis Healthcare (36 établissements), appliquent des standards internationaux. Apollo Hospitals effectue des tests quotidiens sur ses 450 autoclaves, avec un système de traçabilité cloud développé en partenariat avec Microsoft Azure. La formation de 80 heures par technicien CSSD, la plus complète d’Asie, intègre modules théoriques et stages pratiques.
Cependant, 40% des hôpitaux ruraux ne disposent pas d’autoclaves Classe B, limitant l’accès aux tests de Bowie-Dick. Le coût de ₹150-300 (€1.60-3.20) par test, bien qu’abordable en contexte urbain, représente un défi budgétaire pour les structures rurales. Les initiatives gouvernementales Ayushman Bharat visent à équiper 5 000 centres de santé communautaires d’ici 2025, réduisant cette fracture technologique.

7 Causes Principales d’Échec
L’analyse de plus de 100 000 tests de Bowie-Dick effectués dans 50 pays révèle sept causes principales d’échec, représentant 95% des défaillances observées. Cette classification, établie par l’International Association for Healthcare Central Service Materiel Management (IAHCSMM), guide les stratégies de maintenance préventive et de formation du personnel.
1. FUITES D’ÉTANCHÉITÉ (40% des cas)Les joints de porte, sollicités lors de chaque cycle, présentent une durée de vie de 1 000 à 2 000 cycles selon les conditions d’utilisation. Le test standard de fuite au vide, maintenu à -90 kPa, doit présenter une dérive inférieure à 1,3 kPa/minute. Le remplacement préventif des joints, d’un coût de €200-800 selon les modèles, évite 80% des arrêts non programmés.
2. POMPE À VIDE DÉFECTUEUSE (25% des cas)Un vide insuffisant, inférieur à -90 kPa, compromet l’élimination d’air. Les principales causes incluent l’huile contaminée, le niveau d’huile insuffisant, ou l’usure des segments. La maintenance préventive toutes les 500 heures de fonctionnement, incluant vidange et contrôle des performances, maintient l’efficacité optimale.
3. TEMPÉRATURE INADÉQUATE (15% des cas)Les capteurs de température, d’une tolérance de ±2°C, nécessitent une calibration annuelle certifiée. Le piège à vapeur obstrué, fréquent en cas d’eau de qualité insuffisante, réduit les performances thermiques. Le contrôle mensuel de la qualité vapeur prévient 90% de ces défaillances.
Les quatre causes restantes – durée insuffisante (10%), chargement incorrect (5%), test périmé (3%), et qualité vapeur inadéquate (2%) – résultent généralement de défaillances procédurales corrigibles par la formation et la sensibilisation du personnel.
Les actions correctives suivent un protocole escaladé : échec unique répété avec nouveau test, inspection technique approfondie après deux échecs, mise hors service de l’autoclave jusqu’à résolution complète du problème. Cette approche prudente, adoptée par 95% des hôpitaux certifiés, prévient tout risque de compromission de la stérilisation.
Avenir du Test Bowie-Dick
L’industrie du test de Bowie-Dick connaît une transformation technologique majeure, portée par l’innovation digitale et les préoccupations environnementales. Les tests électroniques, intégrant capteurs sans fil et transmission de données en temps réel, représentent la prochaine génération technologique. Ces dispositifs, développés par des sociétés comme Temptime Corporation et Viltechmeda, génèrent des rapports numériques automatiques, éliminant les erreurs d’interprétation humaine et accélérant les procédures de validation.
L’intelligence artificielle et le machine learning révolutionnent la maintenance prédictive des autoclaves. Les algorithmes développés par Getinge et Steris analysent les données historiques de température, pression et vide pour prédire les pannes avec 98% de précision, 72 heures avant leur survenue. Cette approche préventive réduit les arrêts non programmés de 65% et optimise la planification de maintenance.
La technologie blockchain, expérimentée par Mayo Clinic et Massachusetts General Hospital, garantit une traçabilité infalsifiable des tests. Chaque test génère un hash cryptographique unique, horodaté et géolocalisé, créant un registre immuable consultable par les autorités réglementaires et les organismes d’accréditation.
Marché mondial – Projections 2024-2032 :
- Valeur 2024 : $247 millions USD
- CAGR projeté : 8,7% (Compound Annual Growth Rate)
- Valeur 2032 : $485 millions USD
- Croissance régionale : Asie-Pacifique +11% CAGR
- Segments dynamiques : Tests électroniques (+15% CAGR), Tests biodégradables (+12% CAGR)
Les préoccupations environnementales stimulent le développement de tests biodégradables. Les nouveaux matériaux, développés par 3M et Terragene, réduisent l’impact environnemental de 80% tout en maintenant la précision analytique. Ces innovations, adoptées par les hôpitaux « verts » européens, anticipent les futures réglementations environnementales du secteur de la santé.
Exigences Réglementaires
La documentation des tests de Bowie-Dick obéit à des exigences légales strictes, variables selon les juridictions mais convergentes dans leurs objectifs de traçabilité et de responsabilisation. L’Union européenne impose un archivage de 5 à 10 ans selon les pays membres, tandis que les États-Unis appliquent des durées de 3 à 7 ans variables par État. Le Japon maintient la durée la plus longue avec 5 ans minimum, reflétant la culture de précaution nippone.
Les éléments documentaires obligatoires incluent invariablement : date et heure précises, numéro d’identification de l’autoclave, numéro de lot du test, résultat (réussi/échoué), identification de l’opérateur, actions correctives en cas d’échec, et signature du responsable technique. Cette standardisation internationale facilite les audits croisés et les certifications multinationionales.
Les systèmes modernes intègrent identification RFID automatique, stockage cloud sécurisé et interface avec les ERP (Enterprise Resource Planning) hospitaliers. Cette dématérialisation, adoptée par 78% des hôpitaux américains et 65% des établissements européens, réduit les coûts administratifs de 40% tout en améliorant la fiabilité de la traçabilité.
Les audits suivent une cadence hiérarchisée : contrôles internes mensuels par les services qualité, audits externes annuels par les organismes d’accréditation (JCI, NABH, CQC), et inspections réglementaires variables selon les autorités nationales (FDA, MHRA, ANSM, etc.). Cette surveillance multicouche garantit le maintien des standards et l’amélioration continue des pratiques.
Un Standard Universel de Sécurité
Le test de Bowie-Dick, développé il y a plus de 60 ans dans un hôpital écossais, demeure aujourd’hui le gold standard international pour valider l’élimination d’air dans les autoclaves à pré-vide. Son adoption universelle, de Boston à Mumbai, de Tokyo à Berlin, témoigne de son efficacité incontestable et de sa simplicité d’application. Plus qu’un simple test technique, il représente un maillon essentiel de la chaîne de sécurité des soins, protégeant quotidiennement des millions de patients à travers le monde.
À l’ère de la digitalisation et de l’intelligence artificielle, ce test simple mais crucial continue d’évoluer, intégrant les technologies de pointe tout en conservant son principe fondamental : garantir que chaque instrument stérilisé est véritablement stérile. Les innovations futures, qu’elles soient électroniques, environnementales ou prédictives, s’appuieront sur cette base solide établie par Bowie et Dick.
La sécurité des patients commence par l’excellence de la stérilisation. Le test de Bowie-Dick, gardien silencieux de cette excellence, continuera d’assurer cette mission critique dans les décennies à venir, s’adaptant aux évolutions technologiques sans jamais compromettre sa fiabilité fondamentale.


:max_bytes(150000):strip_icc()/102163642_canning-5c901230f5614658b3a569fdf67d1684.jpg)
:max_bytes(150000):strip_icc()/Canning-jar-equipment-GettyImages-89795243-588b753e5f9b5874ee52643d.jpg)



:max_bytes(150000):strip_icc()/GettyImages-1334064660-6ca34a90987f4724819dc32a07680d70.jpg)




:max_bytes(150000):strip_icc()/sea-pressure-canners-winners-afton-cyrus-02-d5b3c920014d45db8b59c5642b22c0a6.jpeg)
:strip_icc()/How-topreserving-canningcanning-basics_sourcefile_updated-aa5acb6e20d24e9e8140d59810c78db8.jpg)